Différence entre la stabilité thermodynamique et cinétique
Le différence clé entre la stabilité thermodynamique et cinétique est que La stabilité thermodynamique fait référence à l'état des produits, tandis que la stabilité cinétique fait référence à l'état des réactifs.
La stabilité thermodynamique et cinétique est deux termes chimiques importants décrivant des systèmes avec des réactions chimiques. La stabilité thermodynamique est la stabilité de l'état énergétique le plus bas d'un système tandis que la stabilité cinétique est la stabilité de l'état énergétique le plus élevé d'un système. De plus, l'état thermodynamique décrit un état d'équilibre d'un système, tandis qu'un état cinétique décrit la réactivité d'un système.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la stabilité thermodynamique
3. Qu'est-ce que la stabilité cinétique
4. Comparaison côte à côte - stabilité thermodynamique vs cinétique sous forme tabulaire
5. Résumé
Qu'est-ce que la stabilité thermodynamique?
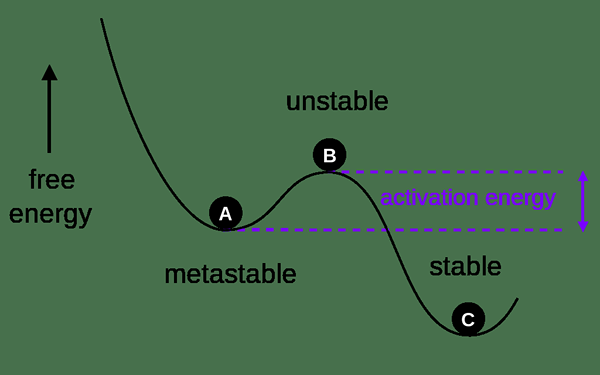
La stabilité thermodynamique est la stabilité de l'état énergétique le plus bas d'un système. Il est également connu sous le nom de stabilité chimique en général. L'état d'énergie le plus bas d'un système est l'endroit où le rendement optimal du produit est obtenu. Cela signifie que la stabilité thermodynamique est obtenue lorsque le système arrive à un état d'équilibre. Parfois, cette stabilité se produit lorsqu'il y a un équilibre dynamique dans lequel les atomes et les molécules individuels ont tendance à changer leur forme, en gardant le changement global à zéro point.

Figure 01: Stabilité des produits à l'état d'équilibre
L'opposé de la stabilité thermodynamique est la «stabilité cinétique», qui décrit la réactivité d'un système plutôt que l'état d'équilibre de ce système.
Qu'est-ce que la stabilité cinétique?
La stabilité cinétique est la stabilité de l'état énergétique le plus élevé d'un système. Cela signifie; La stabilité cinétique se produit lorsqu'il y a un pourcentage de réactif optimal dans le système. En effet. La stabilité cinétique d'un système est donc liée à la réactivité des réactifs. De plus, les réactifs nécessitent généralement une entrée d'énergie pour déplacer la réaction de la stabilité cinétique à la stabilité thermodynamique.
Quelle est la différence entre la stabilité thermodynamique et cinétique?
La stabilité thermodynamique et cinétique est des termes chimiques importants en chimie physique. La principale différence entre la stabilité thermodynamique et cinétique est que la stabilité thermodynamique fait référence à l'état des produits, tandis que la stabilité cinétique se réfère à l'état des réactifs. Habituellement, les réactifs d'une réaction ont une énergie élevée par rapport au niveau d'énergie des produits. Et c'est la raison pour laquelle les réactifs ont tendance à se convertir en produits à faible énergie afin de se stabiliser.
Les réactions chimiques nécessitent généralement une entrée d'énergie pour déplacer le système de la stabilité cinétique à la stabilité thermodynamique où des produits optimaux sont produits. Par conséquent, le terme thermodynamique se réfère à l'état d'équilibre d'un système, tandis que le terme cinétique se réfère à la réactivité d'un système. Parfois, la stabilité thermodynamique donne la stabilité d'une réaction d'équilibre ou d'une réaction non équilibrée.
Le tableau suivant résume la différence entre la stabilité thermodynamique et cinétique.

Résumé - Stabilité thermodynamique vs cinétique
La stabilité thermodynamique et cinétique est des termes chimiques importants en chimie physique. La stabilité thermodynamique est la stabilité de l'état énergétique le plus bas d'un système tandis que la stabilité cinétique est la stabilité de l'état énergétique le plus élevé d'un système. La principale différence entre la stabilité thermodynamique et cinétique est que la stabilité thermodynamique fait référence à l'état des produits, tandis que la stabilité cinétique se réfère à l'état des réactifs. En règle générale, un système nécessite une certaine énergie d'entrée afin de déplacer le système de la stabilité cinétique à la stabilité thermodynamique par la réactivité des réactifs.
Référence:
1. Anthony, jour. «Stabilité cinétique." École de cristallographie, Birbeck University, 1996, disponible ici.
2. «Stabilité thermodynamique." Un aperçu | Sujets ScienceDirect, Disponible ici.
Image gracieuseté:
1. «Stabilité thermodynamique en» par Woudloper - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


