Différence entre la tension superficielle et l'action capillaire
Différence clé - Surface Tension vs action capillaire
La tension en surface et l'action capillaire sont les propriétés physiques des substances liquides. Ce sont des propriétés macroscopiques des liquides. Le différence clé entre la tension superficielle et l'action capillaire est que, La tension en surface est mesurée comme la force appliquée sur une certaine longueur du liquide donné par l'unité N / M (Newton par mètre) tandis que l'action capillaire est mesurée comme la hauteur de la colonne liquide qui est tirée vers le haut, contre la gravité donnée par l'unité M (compteur).
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la tension de surface
3. Quelle est l'action capillaire
4. Relation entre la tension de surface et l'action capillaire
5. Comparaison côte à côte - Tension en surface vs action capillaire sous forme tabulaire
6. Résumé
Qu'est-ce que la tension de surface?
La tension de surface est un phénomène dans lequel la surface d'un liquide, où le liquide est en contact avec le gaz, agit comme une mince feuille élastique. Le terme tension de surface n'est utilisé que lorsque le liquide est en contact avec un gaz (Ex: lorsqu'il est ouvert à l'atmosphère normale). Le terme «tension d'interface» est utilisé pour la couche entre deux liquides.
Les attractions entre différentes espèces chimiques font que les molécules liquides s'unissent ensemble. Les molécules liquides à la surface du liquide sont attirées par les molécules au milieu du liquide. C'est un type de cohésion. Mais l'attraction entre les molécules liquides et les molécules d'air (ou les forces adhésives) est négligeable. Par conséquent, cette couche de surface de molécules liquides agit comme une membrane élastique. La couche de surface des molécules liquides est sous tension car il n'y a pas de forces d'attraction suffisantes pour équilibrer les forces cohésives agissent sur eux, donc cette condition est appelée tension de surface.

Figure 01: Les forces d'attraction sur les molécules liquides à la surface du liquide
Formule pour le calcul de la tension de surface
Tension de surface (γ) = F / D
Ici, f est la force de surface et d est la longueur le long de laquelle la force de surface agit sur. Par conséquent, la mesure de la tension de surface est donnée par l'unité N / M (Newton par mètre).C'est l'unité SI pour la mesure de la tension de surface.
Quelle est l'action capillaire?
L'action capillaire est la capacité d'un liquide à s'écouler dans des espaces étroits sans l'aide ou en opposition aux forces externes comme la gravité. Il peut être observé comme un liquide dessinant à travers un tube capillaire dans la direction ascendante.
L'action capillaire se produit en raison des forces intermoléculaires entre les molécules liquides et la surface du tube capillaire. Par conséquent, cela se produit en raison des forces d'adhésion. Lorsque le diamètre du tube est suffisamment petit, le liquide monte à travers le tube en raison des forces adhésives et cohésives. Les forces cohésives (forces d'attraction entre des molécules similaires) provoquent des molécules.
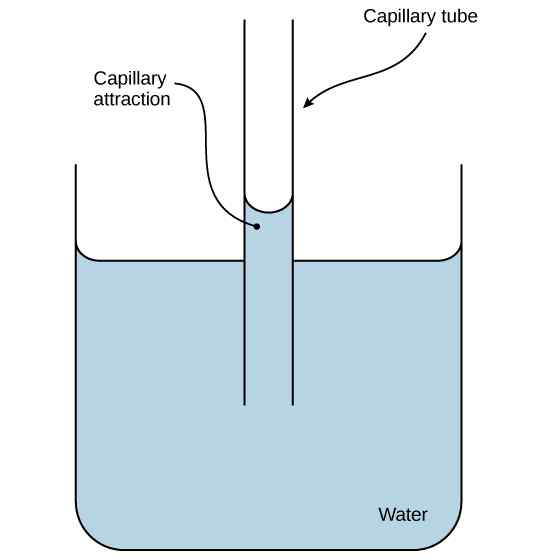
Lorsqu'un tube capillaire est placé dans un liquide, un ménisque se forme au bord du tube. Ensuite, en raison des forces d'adhésion entre les molécules liquides et la paroi du tube, le liquide est tiré jusqu'à ce que la force gravitationnelle agisse sur cette quantité de liquide suffisante pour surmonter la force adhésive. Ensuite, les molécules liquides sont tirées en raison de la cohésion.

Figure 02: Action capillaire - un modèle
L'action capillaire est courante chez les plantes. Les récipients xylèmes sont des tubes capillaires qui peuvent dessiner de l'eau avec des nutriments dissous vers le haut. Cela répond à l'exigence d'eau et de nutriments par les branches et les feuilles des grandes plantes.
Quelle est la relation entre la tension de surface et l'action capillaire?
L'action capillaire crée une colonne liquide dans un tube capillaire. La hauteur de la colonne liquide peut être déterminée par l'équation donnée ci-dessous.
Formule pour le calcul de la hauteur de la colonne liquide
h = 2γcosθ / ρgr
Dans ce,
- H est la hauteur de la colonne liquide,
- γ est la tension en surface du liquide (l'unité est n / m),
- θ est l'angle de contact entre le liquide et la paroi du tube,
- ρ est la densité du liquide, g est l'accélération due à la gravité (l'unité est kg / m3),
- R est le rayon du tube (M).
Quelle est la différence entre la tension superficielle et l'action capillaire?
Tension de surface vs action capillaire | |
| La tension de surface est un phénomène dans lequel la surface d'un liquide, où le liquide est en contact avec le gaz, agit comme une mince feuille élastique. | L'action capillaire est la capacité d'un liquide à s'écouler dans des espaces étroits sans l'aide, ou même en opposition aux forces externes comme la gravité. |
| Théorie | |
| La tension en surface est la force à la surface d'un liquide exposé à l'air. | L'action capillaire est le flux d'un liquide contre une force externe sans aucune aide. |
| La mesure | |
| La tension en surface est mesurée comme la force appliquée à une certaine longueur du liquide donné par l'unité N / M (Newton par mètre). | L'action capillaire est mesurée comme la hauteur de la colonne liquide qui est tirée vers le haut, contre la gravité donnée par l'unité M (mètre). |
Résumé - Surface Tension vs action capillaire
La tension en surface et l'action capillaire sont deux types de propriétés microscopiques des liquides. La différence entre la tension en surface et l'action capillaire est que, la tension de surface est mesurée comme la force appliquée sur une certaine longueur du liquide donné par l'unité N / M (Newton par mètre) tandis que l'action capillaire est mesurée comme la hauteur de la colonne liquide qui est dessiné vers le haut, contre la gravité donnée par l'unité m (mètre).
Référence:
1.Jones, Andrew Zimmerman. «Qu'est-ce que la tension de surface? Définition et expériences."Thoughtco. Disponible ici
2.Perlman, USGS Howard. "Capillarité.”Action capillaire, de l'USGS Water-Science School. Disponible ici
3."Capillarité.»Wikipedia, Wikimedia Foundation, 28 février. 2018. Disponible ici
Image gracieuseté:
1.'Wassermoleküleintöpfchen'By User: Booyabazooka - Propre travaux, (domaine public) via Commons Wikimedia
2.'Figure 02 02 05'By CNX OpenStax, (CC par 4.0) via Commons Wikimedia


