Différence entre le fluorure de sodium et le fluorure de calcium

Différence clé - fluorure de sodium vs fluorure de calcium
Le fluorure de sodium et le fluorure de calcium sont deux minéraux de fluorure des éléments du groupe I et du groupe II du tableau périodique. Bien qu'ils existent naturellement sous forme de minéraux, ils sont également produits commercialement pour des applications industrielles. Mais, La forme naturelle du fluorure de sodium est relativement rare et le fluorure de calcium est très abondant. Cela peut être considéré comme le différence clé entre le fluorure de sodium et le fluor du calcium. Bien qu'ils soient tous deux des fluorures contenant des solides cristallins, leurs applications industrielles varient considérablement; Ils sont utilisés à diverses fins.
Qu'est-ce que le fluorde de sodium?
Le fluorure de sodium est un composé chimique ionique incolore, inorganique, avec la formule moléculaire naf. Comme le chlorure de sodium, il se dissout dans l'eau donnant Na+ et f- séparément.
NAF (s) → N / A+ (aq) + f- (aq)
Le fluorure de sodium existe naturellement en tant que minéral appelé «villiimite», qui est relativement rare et il peut être trouvé dans les roches de syénite pluton.
Le chlorure de sodium est l'une des sources d'ions fluorures les plus utilisées dans de nombreuses applications industrielles, car il est moins cher et moins hygroscopique que le fluorure de potassium (KF).

Villiamumite
Qu'est-ce que le fluor du calcium?
Le fluorure de calcium est un composé solide chimique ionique blanc, insoluble dans l'eau avec la formule moléculaire CAF2. Il est également connu sous le nom spath fluor, et il existe naturellement en tant que fluorite minérale et possède une coloration profonde en raison de ses impuretés. Le minéral de fluorite peut être trouvé à de nombreux endroits, et il est utilisé comme précurseur de HF. Mais, certains processus industriels nécessitent un floride de calcium pur, sans impuretés. Ainsi, CAF de haute pureté2 est produit industriellement en utilisant du carbonate de calcium et du fluor à l'hydrogène.
Caco3 + 2 HF → CAF2 + CO2 + H2O

Fluorure de calcium
Quelle est la différence entre le fluorure de sodium et le fluorure de calcium?
Structure chimique du fluorure de sodium et du fluorure de calcium
Le fluorure de sodium:
Le fluorure de sodium est un cristal ionique qui cristallise dans un motif cube. Dans sa structure, les deux na+ et f- Contient des sites de coordination octaédrique, et son espacement du réseau est approximativement égal à 1662 h. Cette longueur est assez plus petite que celle du chlorure de sodium.
Fluorure de calcium:
Le fluorure de calcium existe naturellement sous forme de fluorite et il cristallise un motif cube. Californie2+ sert de centres à huit coordonnés et est situé dans une boîte pour huit F- centres. Chaque f- Le centre est coordonné à quatre ca2+ centres. Généralement, les cristaux parfaitement emballés sont incolores, mais le minéral possède une couleur profonde en raison des centres F.
La structure d'une cellule unitaire de CAF2 (fluorite) est illustré ci-dessous.
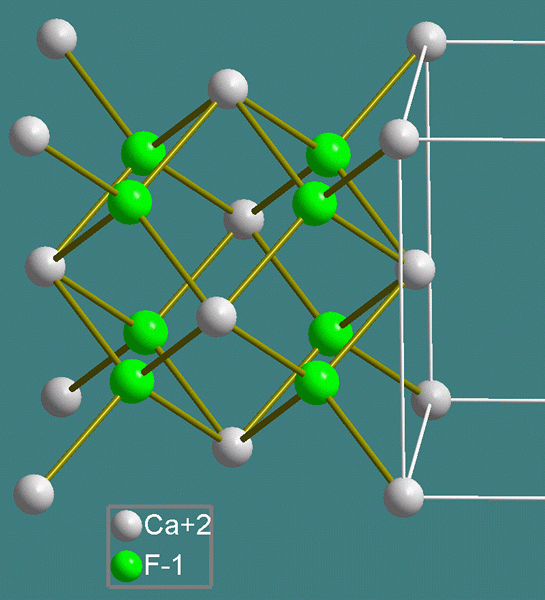
Utilisation du fluorure de sodium et du fluorure de calcium
Le fluorure de sodium:
Le fluorure de sodium est largement utilisé dans un large éventail d'applications industrielles, y compris l'industrie médicale et chimique. Dans les applications médicales, il est utilisé dans l'imagerie médicale et dans le traitement de l'ostéoporose. Dans l'industrie chimique, il est utilisé dans les processus de synthèse et d'extraction en métallurgie, en tant qu'agent de nettoyage et comme poison à l'estomac pour les insectes d'alimentation des plantes.
Il est également utilisé dans le traitement de l'eau. Il est ajouté à l'eau potable dans la fluoration de l'eau pour augmenter le niveau de fluor dans l'eau. Dans certains pays, il est ajouté à certains produits alimentaires.
Fluorure de calcium:
À la fois, CAF à l'origine naturelle et commercialement2 sont tout aussi importants dans de nombreuses applications industrielles. Il est naturellement présent dans le minéral de fluorite, et c'est la principale source de processus de fabrication du fluorure d'hydrogène. La réaction entre la fluorite minérale et l'acide sulfurique concentré produit un fluor d'hydrogène.
Caf2 + Cong2DONC4 → Caso4 (solide) + 2 hf
De plus, il est utilisé pour produire des composants optiques en raison de ses propriétés spéciales. Il est transparent sur un large éventail de fréquences; De ultraviolet (UV) à infrarouge (IR), un faible indice de réfraction et l'insolubilité dans l'eau. Il est utilisé pour fabriquer des fenêtres et des objectifs utilisés dans les systèmes d'imagerie thermique, la spectroscopie et les lasers excimères.
Image gracieuseté: «Villiamumite dans le fluorure de sodium de syénite de nephéline…» par Dave Dyet - Shutterstone.com, teinture.com - propre travail (domaine public) via Commons Wikimedia «Calcium Floride» (domaine public) via Commons Wikimedia «Sodium Floride» par Benjah-Bmm27 - Propre travaux (domaine public) via Commons Wikimedia «Structure cristalline de la fluorite» par matériaux scientist à l'anglais wikipedia (CC BY-SA 3.0) via Commons Wikimedia

