Différence entre le bisulfite de sodium et le métabisulfite de sodium
Le différence clé entre le bisulfite de sodium et le métabisulfite de sodium est que Le bisulfite de sodium n'a qu'un seul atome de soufre et trois oxygènes, et l'anion bisulfite est monovalent tandis que le métabisulfite de sodium a deux atomes de soufre, cinq oxygènes et l'anion est divalent.
Le bisulfite de sodium et le métabisulfite de sodium sont des sels de sodium. Nous utilisons principalement ces produits chimiques comme conservateurs, désinfectants et additifs alimentaires.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le bisulfite de sodium
3. Qu'est-ce que le métabisulfite de sodium
4. Comparaison côte à côte - Bisulfite de sodium vs métabisulfite de sodium sous forme tabulaire
5. Résumé
Qu'est-ce que le bisulfite de sodium?
Le bisulfite de sodium est le composé ayant la formule chimique nahso3. Il a une masse molaire de 104 g de mol-1. De plus, il existe comme un solide blanc, et lorsqu'il est sous forme liquide, il agit comme un liquide corrosif. Le point de fusion du solide est 150 oC. De plus, la forme solide de ce composé est soluble dans l'eau.
En raison de la capacité de donner des protons, il est légèrement acide. De plus, l'atome de soufre dans ce composé est à l'état d'oxydation +4. Nous pouvons préparer le bisulfite de sodium en bouillonnant le dioxyde de dioxyde de gaz en eau gazéifiée. Il libèrera du dioxyde de gaz de soufre lorsqu'il réagira avec des conditions acides légères. Nous pouvons utiliser ce composé en chimie organique à des fins de purification. Il forme un adduit bisulfite avec un aldéhyde, qui est en forme solide. Par conséquent, nous pouvons précipiter l'aldéhyde à partir d'une solution en faisant de celui-ci un adduit de bisulfite, puis peut régénérer le groupe aldéhyde en éliminant le bisulfite. De plus, le bisulfite de sodium est utile en tant qu'agent réducteur léger, agent de décoloration dans la synthèse organique. Surtout, lorsque le bisulfite de sodium réagit avec l'oxygène gazeux, il se transforme en bisulfate de sodium.
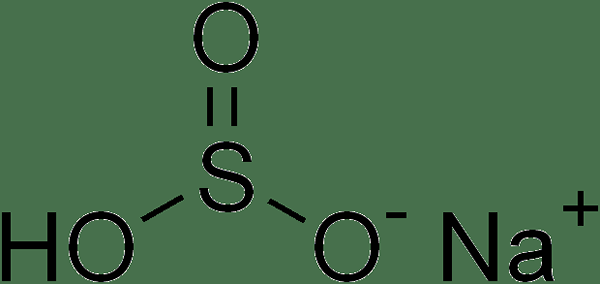
Figure 01: Structure chimique du bisulfite de sodium
Parmi les différents usages de ce composé, un plus notable utilise comme additif alimentaire. Là, il joue un rôle clé dans la production de vin. Plus tôt, les gens utilisaient du bisulfite de sodium pour les jus de fruits. Ensuite, le dioxyde de soufre en recule, et il aidera à désinfecter le liquide en tuant des moules, des bactéries, des germes et d'autres organismes indésirables. De plus, il est essentiel de préserver le vin dans le stockage. Le but principal de l'ajout de bisulfite de sodium comme additif alimentaire est due à sa capacité à fonctionner comme un inhibiteur des bactéries.
Qu'est-ce que le métabisulfite de sodium?
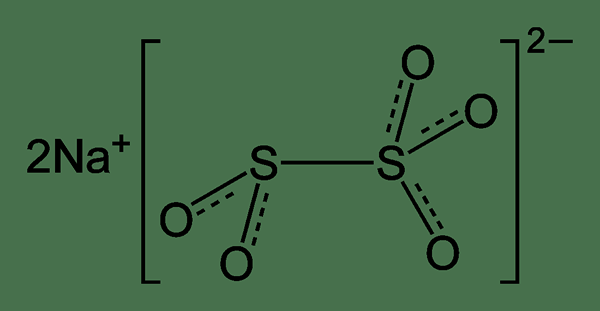
Le métabisulfite de sodium est le composé avec une formule chimique na2S2O5. Nous l'appelons aussi comme du pyrosulfite de sodium. Le poids moléculaire de cette molécule est de 190 g mol-1. De plus, c'est un sel de sodium d'un ion divalent. Plus important encore, ce composé montre la stabilisation de la résonance dans son anion. Là, les deux atomes d'oxygène chargés négativement se lient à chaque atome de soufre, qui permet aux anions de former des structures de résonance.

Figure 02: métabisulfite de sodium
De plus, le métabisulfite de sodium est une poudre cristalline blanche avec le point de fusion 150 oC. De plus, cela est librement soluble dans l'eau et peut libérer du dioxyde de gaz soufre. Le métabisulfite de sodium est utile en tant qu'agent conservateur et désinfectant comme le bisulfite de sodium.
Quelle est la différence entre le bisulfite de sodium et le métabisulfite de sodium?
Le bisulfite de sodium est le composé ayant la formule chimique nahso3 et le métabisulfite de sodium est le composé avec une formule chimique na2S2O5. La principale différence entre le bisulfite de sodium et le métabisulfite de sodium est que le bisulfite de sodium n'a qu'un seul atome de soufre et trois atomes d'oxygène, et que l'anion bisulfite est monovalent tandis que le métabisulfite de sodium a deux atomes de soufre, cinq atomes d'oxygène et l'anion est divalent, il a deux atomes de soufre, cinq atomes d'oxygène et l'anion est divalent, deux atomes de soufre, cinq atomes d'oxygène et l'anion est divalent, deux atomes de soufre, cinq atomes d'oxygène et l'anion est divalent, deux atomes de soufre, cinq atomes d'oxygène et l'anion est divalent, deux atomes de soufre, cinq atomes d'oxygène, et l'anion est divalent a.
De plus, le sulfite de sodium donne moins de sulfite que le métabisulfite de sodium, lorsque nous le dissolvons dans l'eau. C'est donc une différence entre le bisulfite de sodium et le métabisulfite de sodium. Plus de différences sont présentées dans l'infographie de la différence entre le bisulfite de sodium et le métabisulfite de sodium.
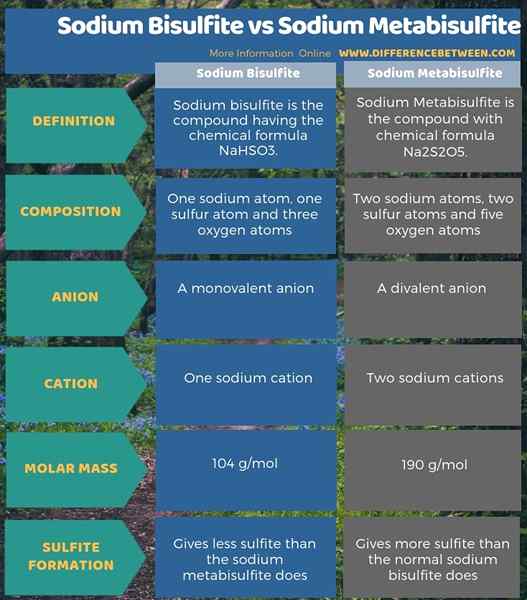
Résumé - Bisulfite de sodium vs métabisulfite de sodium
Le bisulfite de sodium est un additif alimentaire ayant un numéro E222. Le métabisulfite de sodium est également un additif alimentaire, et le nombre est E223. Cependant, ce sont deux composés différents. La principale différence entre le bisulfite de sodium et le métabisulfite de sodium est que le bisulfite de sodium n'a qu'un seul atome de soufre et trois oxygènes, et que l'anion bisulfite est monovalent tandis que le métabisulfite de sodium a deux atomes de soufre, cinq oxygènes et l'anion est divalent, divalent.
Référence:
1. "Le métabisulfite de sodium.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine. Disponible ici
2. "Bisulfite de sodium.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine. Disponible ici
Image gracieuseté:
1.«Sodium Bisulfite» par Edgar181 - Propre travaux, (domaine public) via Commons Wikimedia
2.«Sodium-Metabisulfite-2d» (domaine public) via Commons Wikimedia


