Différence entre les réactions SN1 et SN2

Différence clé - Réactions SN1 vs SN2
Les réactions SN1 et SN2 sont des réactions de substitution nucléophile et le plus souvent trouvé en chimie organique. Les deux symboles SN1 et SN2 se réfèrent à deux mécanismes de réaction. Le symbole SN signifie «substitution nucléophile». Même si SN1 et SN2 sont dans la même catégorie, ils ont de nombreuses différences, notamment le mécanisme de réaction, les nucléophiles et les solvants ont participé à la réaction, et les facteurs affectant l'étape de détermination de la vitesse. Le différence clé entre les réactions SN1 et SN2 est que Sn1 Les réactions ont plusieurs étapes alors que Sn2 Les réactions n'ont qu'une étape.
Que sont les réactions SN1?
Dans les réactions SN1, 1 indique que l'étape de détermination de la vitesse est unimoléculaire. Ainsi, la réaction a une dépendance de premier ordre à l'électrophile et à la dépendance d'ordre zéro à l'égard des nucléophiles. Un carbocation est formé comme intermédiaire dans cette réaction et ce type de réactions se produit généralement dans les alcools secondaires et tertiaires. Les réactions SN1 ont trois étapes.
- Formation du carbocation en supprimant le groupe de départ.
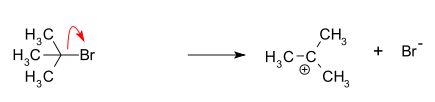
- La réaction entre le carbocation et le nucléophile (attaque nucléophile).
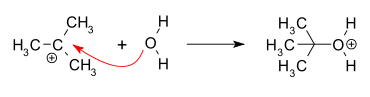
- Cela ne se produit que lorsque le nucléophile est un composé neutre (un solvant).
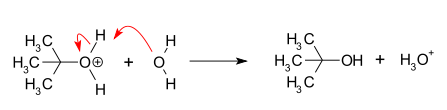
Que sont les réactions SN2?
Dans les réactions SN2, une liaison est rompue et une liaison se forme simultanément. En d'autres termes, cela implique le déplacement du groupe de départ par un nucléophile. Cette réaction se produit très bien dans les halogénures d'alkyle méthyle et primaires tandis que très lentement dans les halogénures d'alkyle tertiaires car l'attaque arrière est bloquée par des groupes volumineux.
Le mécanisme général des réactions SN2 peut être décrit comme suit.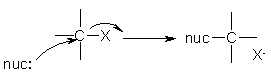
Quelle est la différence entre les réactions SN1 et SN2?
Caractéristiques des réactions SN1 et SN2:
Mécanisme:
Réactions SN1: Sn1 Les réactions ont plusieurs étapes; Il commence par l'élimination du groupe de départ, entraînant un carbocation puis l'attaque par le nucléophile.
Réactions SN2: Sn2 Les réactions sont des réactions à pas unique où les nucléophiles et le substrat sont impliqués dans l'étape de détermination de la vitesse. Par conséquent, la concentration du substrat et celle du nucléophile affectera à l'étape de détermination du taux.
Barrières de la réaction:
Réactions SN1: La première étape des réactions SN1 consiste à éliminer le groupe de départ pour donner un carbocation. La vitesse de la réaction est proportionnelle à la stabilité du carbocation. Par conséquent, la formation du carbocation est la plus grande barrière dans les réactions SN1. La stabilité du carbocation augmente avec le nombre de substituants et la résonance. Les carbocations tertiaires sont les carbocations les plus stables et les primaires sont les moins stables (tertiaire> secondaire> primaire).
Réactions SN2: L'obstruction stérique est la barrière de SN2 Réactions car elle passe par une attaque arrière. Cela ne se produit que si les orbitales vides sont accessibles. Lorsque plus de groupes sont attachés au groupe de départ, cela ralentit la réaction. Ainsi, la réaction la plus rapide se produit dans la formation de carbocations primaires tandis que le plus lent est dans les carbocations tertiaires (plus rapide du primaire> Secondary> Tertiaire-slowest).
Nucléophile:
Réactions SN1: Sn1Les réactions nécessitent des nucléophiles faibles; Ce sont des solvants neutres tels que le ch3OHH2O, et ch3Ch2OH.
Réactions SN2: Sn2 Les réactions nécessitent de forts nucléophiles. En d'autres termes, ce sont des nucléophiles chargés négativement comme Asch3O-, CN-, Rs-, N3- et ho-.
Solvant:
Réactions SN1: Les réactions SN1 sont favorisées par les solvants protiques polaires. Les exemples sont l'eau, les alcools et les acides carboxyliques. Ils peuvent également agir comme les nucléophiles pour la réaction.
Réactions SN2: Les réactions SN2 se déroulent bien dans des solvants aprotiques polaires tels que l'acétone, le DMSO et l'acétonitrile.
Définitions:
Nucléophile: Une espèce chimique qui donne une paire d'électrons à un électrophile pour former une liaison chimique par rapport à une réaction.
Électrophile: réactif attiré par les électrons, ils sont des espèces chargées positivement ou neutres ayant des orbitales vacantes qui sont attirées par un centre riche en électrons.
Références: Master Organic Chemistry - Comparaison des réactions SN1 et SN2 réactions Portale de chimie organique - Substitution nucléophile (SN1N2)

