Différence entre pyrrole pyridine et pipéridine
Le différence clé entre pyrrole pyridine et pipéridine est leur basicité. Le pyrrole est le moins basique et la pyridine est modérément basique, tandis que la pipéridine est la plus basique.
Le pyrrole, la pyridine et la pipéridine sont des composés organiques ayant des atomes d'azote dans leurs structures chimiques. Ces composés sont des composés de base (en face de l'acide).
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que Pyrrole
3. Qu'est-ce que la pyridine
4. Qu'est-ce que la pipéridine
5. Comparaison côte à côte - pyrrole pyridine vs pipéridine sous forme tabulaire
6. Résumé
Qu'est-ce que Pyrrole?
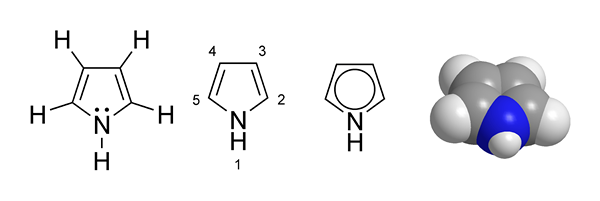
Pyrrole est un composé organique ayant une structure annulaire à cinq membres avec la formule chimique C4H4NH. Il s'agit d'un composé hétérocyclique ayant un atome d'azote contribuant à la formation de la structure de l'anneau, ainsi que quatre autres atomes de carbone. Pyrrole est un liquide volatil et incolore à température ambiante. Lors de l'exposition à l'air normal, le liquide de pyrrole s'assombrit facilement, ce qui provoque la nécessité de le purifier avant d'utiliser. Nous pouvons faire la purification par distillation immédiatement avant utilisation. De plus, ce liquide a une odeur de noisette.

Contrairement à d'autres anneaux hétérocycliques à cinq membres tels que le furan et le thiophène, ce composé a un dipôle dans lequel le côté positif de l'anneau est à l'hétéroatom (-NH le groupe porte la charge positive). De plus, c'est un composé faiblement basique.
Pyrrole existe dans la nature comme dérivés de pyrrole. Par exemple, la vitamine B12, les pigments biliaires tels que la bilirubine, les porphyrines, etc., sont des dérivés pyrroles. Cependant, ce composé est légèrement toxique. À l'échelle industrielle, nous pouvons synthétiser le pyrrole via le traitement du furan avec de l'ammoniac. Mais cette réaction nécessite également un catalyseur solide.
Qu'est-ce que la pyridine?
La pyridine est un composé organique ayant la formule chimique C5H5N. C'est un composé hétérocyclique. La structure de la pyridine ressemble à la structure du benzène, où un groupe méthyle est remplacé par un atome d'azote. De plus, la pyridine est un composé alcalin faible, et il existe à l'état liquide où il se produit comme un liquide visqueux. En dehors de cela, la pyridine est incolore et a une odeur de poisson distinctive. De plus, ce liquide est soluble dans l'eau et est très inflammable.
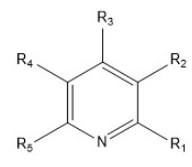
La pyridine est une substance diamagnétique. La structure de la molécule de pyridine est un hexagone. Dans cette molécule, la liaison C-N est plus courte que les liaisons C-C. La pyridine cristallise dans le système cristallin orthorhombique. Cependant, la molécule de pyridine est une structure déficiente en électrons due à la présence d'un atome d'azote plus électronégatif. Par conséquent, il a tendance à subir des réactions de substitution aromatique électrophile. Une autre raison de cette capacité est la présence d'une paire d'électrons solitaires sur l'atome d'azote.
En ce qui concerne les applications de la pyridine, il est principalement utile comme composant en pesticide, comme solvant polaire basique, comme le réactif Karl Fischer dans la synthèse organique, etc.
Qu'est-ce que la pipéridine?
La pipéridine est un composé organique ayant la formule chimique (ch2)5NH. Ce composé se produit comme une structure cyclique à six membres qui est hétérocyclique. Dans cette structure, il existe un atome d'azote en tant que membre de la structure cyclique en plus des cinq atomes de carbone. Par conséquent, c'est une amine hétérocyclique. La pipéridine apparaît comme un liquide incolore et a une odeur d'amine. De plus, la pipéridine est miscible avec de l'eau, et sa solution aqueuse a une acidité élevée.
L'ancienne méthode de production de la pipéridine était la réaction entre la pipérine et l'acide nitrique. Cependant, nous pouvons le produire à l'échelle industrielle via la réaction d'hydrogénation de la pyridine. Ce processus est généralement effectué sur un catalyseur de disulfure de molybdène. De plus, nous pouvons obtenir de la pipéridine en réduisant la pyridine via un processus de réduction de bouleau modifié à l'aide de sodium dans l'éthanol. Cependant, nous pouvons obtenir directement de la pipéridine en l'extraction de poivre noir.
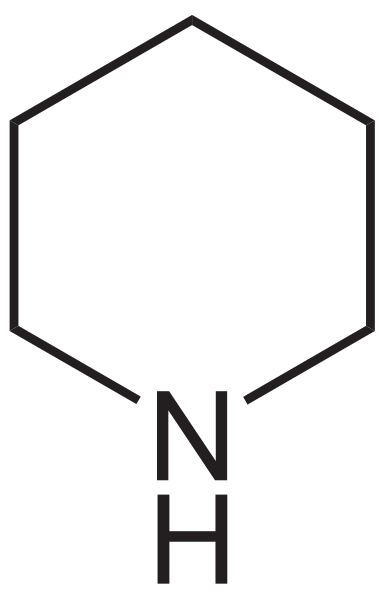
Lorsque l'on considère la structure chimique de la pipéridine, il a une conformation de chaise similaire au cyclohexane. Il y a deux conformations de chaise différentes de ce composé. L'un a la liaison N-H en position axiale tandis que l'autre confirmation l'a en position équatoriale.
La pipéridine est une amine secondaire. Il est largement utilisé pour convertir les cétones en énamines. Ces énamines peuvent être utilisées pour la réaction d'alkylation en énamine de cigogne. De plus, la pipéridine est utile comme solvant et comme base. Dans les industries, la pipéridine est utile pour la production de tétrasulfure de dipipéridinyl dithiuram (un accélérateur pour la vulcanisation du soufre du caoutchouc).
Quelle est la différence entre la pyrrole pyridine et la pipéridine?
Le pyrrole, la pyridine et la pipéridine sont des composés organiques. La principale différence entre la pyrrole pyridine et la pipéridine est que le pyrrole est le moins basique et la pyridine est modérément basique, tandis que la pipéridine est la plus basique.
L'infographie suivante résume les différences entre la pyrrole pyridine et la pipéridine sous forme tabulaire.

Résumé - Pyrrole vs pyridine vs pipéridine
Le pyrrole, la pyridine et la pipéridine sont des composés organiques ayant des atomes d'azote dans leurs structures chimiques. Ces composés sont des composés de base. La principale différence entre le pyrrole, la pyridine et la pipéridine est que le pyrrole est le moins basique, et la pyridine est modérément basique, tandis que la pipéridine est la plus basique.
Référence:
1. «Pipéridine - Utilisations majeures." U.S. Bibliothèque nationale de médecine, National Institutes of Health, disponible ici.
Image gracieuseté:
1. «Pyrrole» (CC BY-SA 3.0) via Commons Wikimedia
2. «Pyridine» par Valgerdur Anna - ChemDraw Professional 16.0 (CC BY-SA 4.0) via Commons Wikimedia
3. «Pipéridine» par Neurotiker - Propre travaux (domaine public) via Commons Wikimedia


