Différence entre l'isomérisme de position et le métaméririsme
Différence clé - Position Isomérisme vs métaméririsme
L'isomérisme peut être défini comme l'existence de composés chimiques ayant la même formule structurelle mais différentes arrangements spatiaux. Cela signifie que les isomères ont le même nombre d'atomes dans chaque élément, mais leur arrangement est différent. Les isomères sont principalement classés en deux groupes nommés isomères structurels et stéréoisomères. Les isomères structurels sont à nouveau divisés en trois groupes en tant qu'isomères de chaîne, des isomères de position et des isomères de groupes fonctionnels. Les métamères sont également un type d'isomères structurels, mais ils ne sont pas couramment trouvés. La principale différence entre l'isomérisme de position et le métaméririsme est que, Dans l'isomérisme de position, le groupe fonctionnel est attaché à différentes positions tandis que, dans le métaméririsme, différents groupes alkyles sont attachés au même groupe fonctionnel.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'isomérisme de position
3. Qu'est-ce que le métaméririsme
4. Comparaison côte à côte - Position Isomérisme vs métamerisme
5. Résumé
Qu'est-ce que l'isomérisme de position?
L'isomérisme de position peut être défini comme le «mouvement» du groupe fonctionnel dans la molécule. Cela signifie que seule la position du groupe fonctionnel est modifiée dans ce type d'isomérisme. Le nombre d'atomes de carbone, la formule moléculaire, la structure de la squelette du carbone et le nombre de groupes fonctionnels sont les mêmes pour les isomères en position isomérisme. Mais ce type d'isomérisme est absent dans les composés ayant des groupes finaux comme les acides carboxyliques, les aldéhydes, etc. Puisque ces groupes ne peuvent pas être positionnés au milieu d'une chaîne de carbone.
Par exemple, le bromure de propyle et le bromure d'isopropyle sont des isomères de position. Dans le bromure de propyle, le groupe fonctionnel est -BR et il est attaché à l'extrémité de la chaîne de carbone tandis que dans le bromure d'isopropyle, le groupe -BR est attaché à l'atome de carbone moyen de la chaîne de carbone.

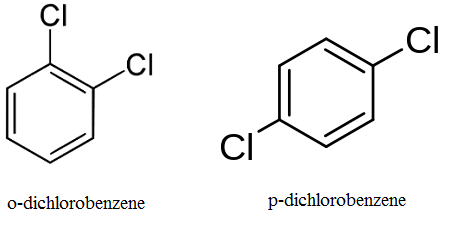
Figure 01: Positionner l'isomérisme dans l'o-dichlorobenzène et le p-dichlorobenzène
Qu'est-ce que le métaméririsme?
Dans le cas du métaméririsme, les types de groupes alkyle sur les côtés des groupes fonctionnels différeront les uns des autres. C'est une distribution inégale des atomes de carbone. Le métaméririsme appartient à la même série homologue, ce qui signifie que le nombre d'atomes de carbone peut être augmenté progressivement pour obtenir des isomères différents. Par conséquent, les structures ne diffèrent que par le nombre de ch2 groupes dans la chaîne carbone principale.
Les groupes alkyle sont toujours attachés aux côtés d'un atome divalent comme l'oxygène ou le sulfure, ou les groupes alkyle peuvent être attachés à un groupe divalent tel que -nh-. Le métaméririsme est rarement trouvé en raison de ces limitations. Par conséquent, la plupart des composés trouvés dans le métaméririsme sont des éthers et des amines.
Par exemple, l'éther diéthylique et l'éther méthyl propyl sont des métamères. Ici, le groupe fonctionnel est éther et l'atome divalent est l'atome d'oxygène. L'éther diéthylique a deux groupes éthyliques tandis que l'éther de méthyl propyle a un méthyle et un groupe propyl sur les côtés de l'atome d'oxygène.
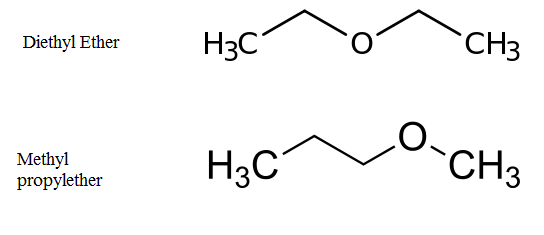
Figure 02: métaméririsme dans l'éther méthyl propyl et éther diéthylique
Quelle est la différence entre l'isomérisme de position et le métamerisme?
Positionner l'isomérisme vs métaméririsme | |
| Dans l'isoméririsme de position, la position du groupe fonctionnel diffère. | Dans le métaméririsme, le type de groupe alkyle attaché au groupe fonctionnel diffère. |
| Nombre d'isomères | |
| L'isomérisme de position montre un certain nombre d'isomères qui ne diffèrent que par la position du groupe fonctionnel | Le métaméririsme a un nombre limité d'isomères en raison de ses limites telles que les groupes alkyle qui ne sont attachés qu'aux atomes ou groupes divalents. |
| Groupes fonctionnels spécifiques | |
| L'isomérisme de position ne peut pas être vu dans les composés n'ayant que des groupes finaux aldéhyde, carboxylique. | Le métaméririsme ne peut être vu que dans des éthers ou d'autres composés contenant des atomes divalents. |
| Groupes alkyles | |
| Les mêmes groupes alkyles sont attachés aux groupes fonctionnels dans les isomères d'isomérisme de position. | Différents groupes alkyles sont attachés au groupe fonctionnel dans le métaméririsme. |
| Série | |
| Cela appartient à une série non homologue. | Cela appartient à une série homologue |
Résumé - Position Isomérisme vs métaméririsme
La principale différence entre l'isomérisme de position et le métaméririsme est que, dans l'isomérisme de position, l'emplacement du groupe fonctionnel est modifié tandis que, dans le métaméririsme, le type de groupes alkyle dans les côtés du groupe fonctionnel est modifié.
Référence:
1. Carey, F. UN. & Sundberg, R. J., 2007. Chimie organique avancée. 5e ed. Charlottesville: Springer.
2. «Principes de base en chimie organique: isoméririsme structurel.”Projet d'enseignement ouvert. N.p., n.d. la toile. 25 mai 2017.
3. Vardhan, V. Aditya. «L'isomérisme dans les composés organiques.”Aidchimie. N.p., n.d. la toile. 25 mai 2017. .
Image gracieuseté:
1. «1,2-dichlorobenzène» du versement original était Sbrool à Anglais Wikipedia - (Domaine public) via Commons Wikimeida
2. Domaine public "O-dichlorobenzène") via Commons Wikimedia
3. «Diéthylether» par Gaussianer - propre travail, domaine public) via Commons Wikimedia
4. «1-méthoxypropane 200» par Emeldir (talk) - propre travail (domaine public) via Commons Wikimedia


