Différence entre élément polyvalent et ion polyatomique
Le différence clé entre l'élément polyvalent et l'ion polyatomique est que Les éléments polyvalents ont plus d'une valence tandis que les ions polyatomiques ont plus d'un atome qui sont liés de manière covalente.
Le préfixe «Poly-» fait référence à «beaucoup». En d'autres termes, si nous nommons quelque chose en utilisant ce préfixe, cela signifie qu'il y a plus d'une de cette chose. Par exemple, le polyvalent signifie plus d'une valence et polyatomique signifie plus d'un atome.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce qu'un élément polyvalent
3. Qu'est-ce qu'un ion polyatomique
4. Comparaison côte à côte - élément polyvalent vs ion polyatomique sous forme tabulaire
5. Résumé
Qu'est-ce qu'un élément polyvalent?
L'élément polyvalent est un élément chimique ayant plus d'une valence. En d'autres termes, ces éléments chimiques impliquent dans la formation de liaisons chimiques en utilisant différents nombres d'électrons. Un synonyme de ce terme est «élément multivalent». Certains exemples sont comme ci-dessous:
- Le fer montre deux états d'oxydation sous forme de fer (II) et de fer (III). Cela signifie que le fer peut montrer deux valences.
- Le cuivre montre deux états d'oxydation comme cuivre (I) et cuivre (II). Le cuivre peut éliminer un électron ou deux électrons lors de la formation d'une liaison chimique.
- Le chrome montre que le chrome (II), (iii) et (vi) les états d'oxydation.
Qu'est-ce qu'un ion polyatomique?
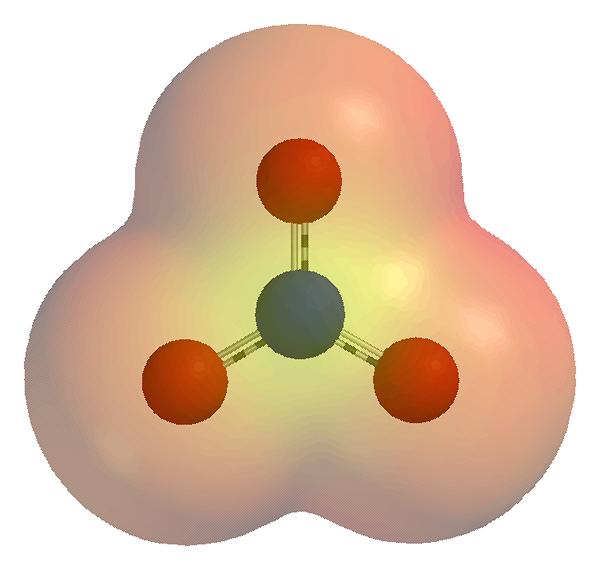
L'ion polyatomique est une espèce chimique qui a une charge et plus d'un atome. Cela peut être chargé positivement (cation) ou chargé négativement (anion). En revanche, les atomes uniques ayant une charge sont des ions monoatomiques.

Figure 01: un diagramme montrant l'ion polyatomique
Lors de la dénomination de tels composés, il y a deux règles que nous devons obéir. Premièrement, nous devons utiliser le préfixe «bi-» s'il y a de l'hydrogène dans la formule chimique et nommer l'ion en fonction du nombre d'atomes d'oxygène présents dans l'ion. Par exemple, l'anion carbonate est un ion polyatomique (CO32-) Et lorsque nous y ajoutons un atome d'hydrogène, nous appelons le bicarbonate ionique (HCO3-). La deuxième règle de nomenclature considère le nombre d'atomes d'oxygène présents dans l'ion, i.e. CLO2- est le chlorite et le clochard3- est chlorate.
Quelle est la différence entre l'élément polyvalent et l'ion polyatomique?
La principale différence entre l'élément polyvalent et l'ion polyatomique est que les éléments polyvalents ont plus d'une valence tandis que les ions polyatomiques ont plus d'un atome qui sont liés de manière covalente. Lorsque l'on considère la théorie derrière ces termes, le polyvalent signifie qu'il utilise plus d'un électron en formation de liaisons chimiques tandis que le polyatomique signifie qu'il utilise plus d'un atome pour former un ion.
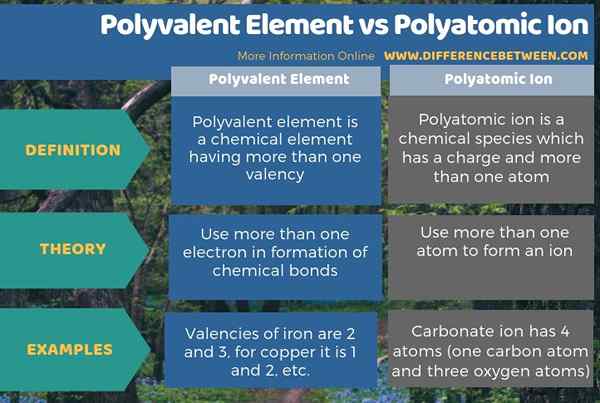
Résumé - Élément polyvalent vs ion polyatomique
Fondamentalement, la principale différence entre l'élément polyvalent et l'ion polyatomique est que les éléments polyvalents ont plus d'une valence tandis que les ions polyatomiques ont plus d'un atome qui sont liés de manière covalente les uns aux autres.
Référence:
1. Helmenstine, Anne Marie, Ph.D. «Ion polyatomique: définition et exemples."Thoughtco, Jan. 12, 2019, disponible ici.
Image gracieuseté:
1. «Nitrate-ion-elpot» par Benjah-Bmm27 - propre travail (domaine public) via Commons Wikimedia


