Différence entre l'oxygénation et l'oxydation
Le différence clé entre l'oxygénation et l'oxydation est que le L'oxygénation implique essentiellement l'oxygène moléculaire alors que l'oxydation n'implique pas nécessairement l'oxygène.
Bien que les deux termes oxygénation et oxydation semblent similaires, ce sont deux termes distincts. En effet, le processus d'oxygénation nécessite la présence d'oxygène, mais le processus d'oxydation peut survenir.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'oxygénation
3. Qu'est-ce que l'oxydation
4. Comparaison côte à côte - oxygénation vs oxydation sous forme tabulaire
5. Résumé
Qu'est-ce que l'oxygénation?
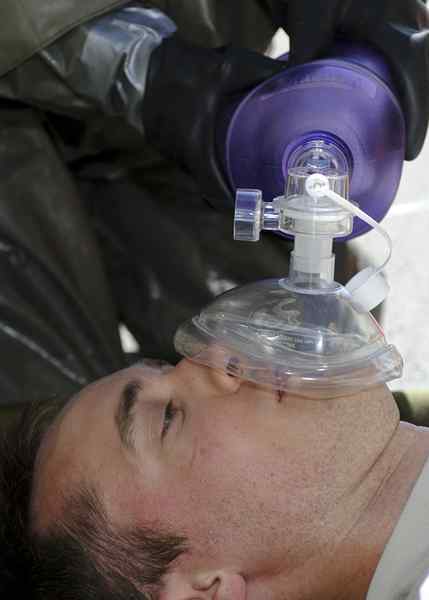
L'oxygénation est l'ajout d'oxygène moléculaire à tout système. Par exemple, le processus de traitement d'un patient atteint d'oxygène se réfère également à l'oxygénation. En chimie, nous utilisons ce terme principalement pour indiquer l'ajout d'oxygène moléculaire à une espèce chimique tels que les métaux de transition dans la formation de composés de coordination.

Figure 01: Donner de l'oxygène à un patient peut se référer à l'oxygénation
Dans ces complexes de coordination, l'oxygène moléculaire agit comme un ligand qui se lie à un métal de transition. La plupart du temps, ces complexes forment de manière réversible. Cela signifie; Nous pouvons éliminer l'oxygène moléculaire du complexe si nous modifions les conditions de réaction.
Qu'est-ce que l'oxydation?
L'oxydation est le processus d'augmentation du nombre d'oxydation d'espèces chimiques. Cependant, il existe trois définitions distinctes pour ce terme; L'ajout d'oxygène, l'élimination de l'hydrogène ou la perte d'électrons signifie l'oxydation. Mais, toutes ces définitions ont des exceptions à différentes occasions. Ainsi, nous utilisons la définition ci-dessus comme définition générale pour toutes les occasions.
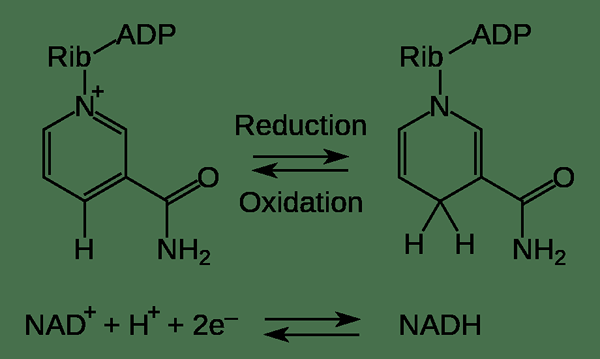
Figure 02: une réaction redox
L'oxydation est un type de réaction redox. Une réaction redox a essentiellement deux réactions parallèles; Réactions d'oxydation et réactions de réduction. Ces réactions impliquent toujours le transfert d'électrons entre deux espèces chimiques. De plus, les espèces chimiques qui subissent l'oxydation libèrent toujours des électrons tandis que les espèces chimiques qui subissent une réduction obtiendront toujours ces électrons. Par conséquent, la libération d'électrons fait plus de protons qui n'ont pas d'électrons pour neutraliser leur charge. Ainsi, l'élimination des électrons augmentera le nombre d'oxydation des espèces chimiques.
Quelle est la différence entre l'oxygénation et l'oxydation?
L'oxygénation est l'ajout d'oxygène moléculaire à tout système alors que l'oxydation est le processus d'augmentation du nombre d'oxydation d'une espèce chimique. Par conséquent, la principale différence entre l'oxygénation et l'oxydation est que l'oxygénation implique essentiellement l'oxygène moléculaire alors que l'oxydation n'implique pas nécessairement l'oxygène. De plus, nous utilisons le terme oxygénation pour désigner l'ajout d'oxygène moléculaire à une espèce chimique telle que le métal de transition ou le traitement d'un patient atteint d'oxygène tandis que le terme oxydation fait référence à l'augmentation du nombre d'oxydation d'une espèce chimique.
L'infographie ci-dessous tabule la différence entre l'oxygénation et l'oxydation comme une comparaison latérale.

Résumé - Oxygénation vs oxydation
Les deux termes l'oxygénation et l'oxydation peuvent se référer à l'ajout d'oxygène, mais pas toujours. De plus, le terme oxydation se réfère parfois aux processus qui se produisent en l'absence totale d'oxygène. Par conséquent, la principale différence entre l'oxygénation et l'oxydation est que l'oxygénation implique essentiellement l'oxygène moléculaire alors que l'oxydation n'implique pas nécessairement de l'oxygène.
Référence:
1. Nabili, Siamak n. «Qu'est-ce que la polycythémie vera? Symptômes, espérance de vie, traitement et causes.”Medicinenet. Disponible ici
2. «Redox.»Wikipedia, Wikimedia Foundation, 6 octobre. 2018. Disponible ici
Image gracieuseté:
1.”2000916137" par Airman St Class Anania TekurioreLelieond (CC0) via la base de l'Air Force Ellsworth
2.«Réduction de l'oxydation du NAD» par FvasConcellos (domaine public) via Commons Wikimedia


