Différence entre la désamination oxydative et non oxydante
Le différence clé entre la désamination oxydative et non oxydante est que le La désamination oxydative se produit via l'oxydation des acides aminés du groupe amino tandis que la désamination non oxydante se produit via des réactions autres que l'oxydation.
La désamination est, comme son nom le décrit, l'élimination d'un groupe amine de toute molécule. Ce sont des réactions chimiques catalysées par des enzymes de la désaminase. Dans notre corps, ce type de réactions se produit dans le foie et parfois aussi dans le rein (ex: désamination du glutamate dans les reins). Là, le groupe d'amine retiré se convertit en ammoniac et excrété de notre corps. De plus, il y a quatre réactions principales qui se produisent en tant que réactions de désamination; Ce sont l'oxydation, la réduction, l'hydrolyse et les réactions intramoléculaires. Parmi ceux-ci, à l'exception de l'oxydation, d'autres réactions sont des réactions non oxydantes.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la désamination oxydative
3. Qu'est-ce que la désamination non oxydante
4. Comparaison côte à côte - désamination oxydante vs non oxydante sous forme tabulaire
5. Résumé
Qu'est-ce que la désamination oxydative?
La désamination oxydative est le processus d'élimination d'un groupe amine d'une molécule par oxydation. Ce type de réactions se produit en grande partie dans le foie et les reins. Il s'agit de la génération d'acides alpha-céto et de quelques autres produits oxydés de groupes amine. Cette réaction est très importante dans le catabolisme des acides aminés. Il forme un produit catabolisé à partir d'acides aminés. Le sous-produit de cette réaction est l'ammoniac qui est un sous-produit toxique. Ici, le groupe amine se convertit en ammoniac. Et puis, cet ammoniac se transforme en urée et excrété de notre corps.

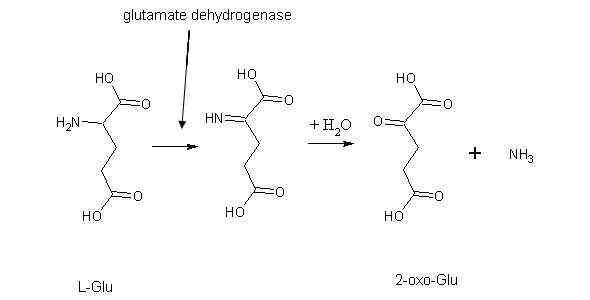
Figure 01: Déamination oxydative du glutamate
La plupart du temps, l'acide glutamique ou le glutamate est le principal réactif de ce type de réactions. Parce que l'acide glutamique est le produit final de nombreuses réactions de transamination qui se produisent dans nos cellules. De plus, l'enzyme impliquée dans cette réaction est le glutamate déshydrogénase. Cette enzyme catalyse le transfert d'un groupe amino à un groupe d'acide alpha-céto. De plus, il y a une autre enzyme qui implique ce type de réactions. C'est l'enzyme de monoamine oxydase qui catalyse la désamination via l'ajout d'oxygène.
Qu'est-ce que la désamination non oxydante?
La désamination non oxydante est le processus d'élimination d'un groupe amine d'une molécule via différentes réactions autres que l'oxydation. Nous l'appelons «désamination directe» sans oxydation. Ces réactions comprennent la réduction, l'hydrolyse et les réactions intramoléculaires. Cependant, cette réaction implique également la production d'ammoniac de sous-produit toxique des acides aminés. De plus, les acides aminés les plus courants qui subissent ce type de réactions sont la sérine, la thréonine, la cystéine et l'histidine. De même, les enzymes les plus courantes impliquées dans cette réaction sont les déshydratases, les lyases et les hydrolases amides.
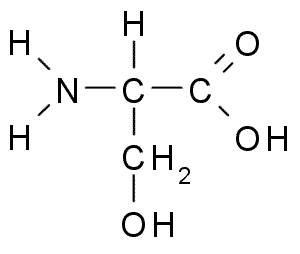
Figure 02: sérine qui subit une désamination non oxydante
La désamination de réduction se produit via la réduction du groupe amine en un acide gras. La désamination hydrolytique implique la conversion du groupe amine en groupe d'acide hydroxy. D'après la réaction intramoléculaire, le groupe amine se convertit en un groupe d'acides gras insaturés. À titre d'exemple, les enzymes de déshydratase peuvent convertir la sérine en pyruvate et en ammoniac et également convertir la thréonine en alpha-cétobutyrate et l'ammoniac.
Quelle est la différence entre la désamination oxydative et non oxydante?
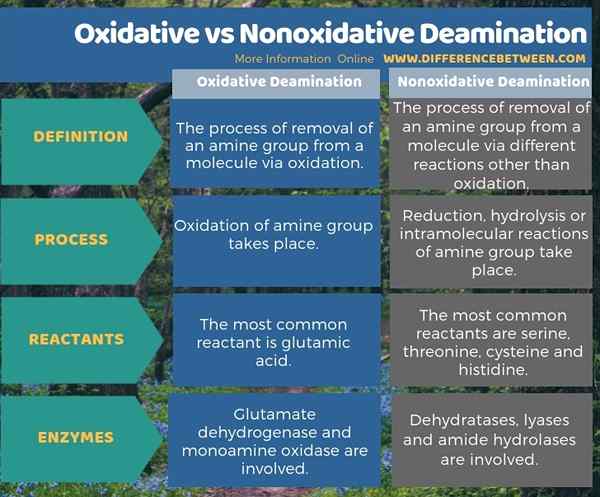
La désamination est l'élimination d'un groupe amine d'une molécule. Ainsi, en désamination, le groupe amine se convertit en différents autres produits en fonction du type de réaction qu'il subit. La principale différence entre la désamination oxydative et non oxydante est que la désamination oxydative se produit via l'oxydation des acides aminés du groupe amino tandis que la désamination non oxydante se produit via des réactions autres que l'oxydation. En raison de cette différence, les réactions chimiques impliquées dans ces processus sont également différentes les unes des autres. C'est-à-dire que la désamination oxydative implique l'oxydation tandis que la désamination non oxydante implique une réduction, une hydrolyse ou des réactions intramoléculaires. De plus, une autre différence significative entre la désamination oxydative et non oxydante est dans les enzymes impliquées dans ces réactions. C'est-à-dire que la glutamate déshydrogénase et la monoamine oxydase impliquent dans le processus oxydatif tandis que les déshydratases, les lyases et les hydrolases amides impliquent dans le processus non oxydant comme des enzymes.
L'infographie ci-dessous décrit la différence entre la désamination oxydative et non oxydante sous forme tabulaire.
Résumé - Oxydatif vs désamination non oxydante
La désamination est la libération de l'ammoniac via la désamination d'un groupe amine. Il existe deux principaux types de désamination oxydative et non oxydante. La désamination non oxydante comprend des réactions autres que l'oxydation telles que la réduction, l'hydrolyse et les réactions intramoléculaires. Par conséquent, la principale différence entre la désamination oxydative et non oxydante est que la désamination oxydative se produit via l'oxydation des acides aminés du groupe amino tandis que la désamination non oxydante se produit via des réactions autres que l'oxydation.
Référence:
1. «Désamination oxydative.»Wikipedia, Wikimedia Foundation, 24 avril. 2018. Disponible ici
2. Ahmed, Minhaz. «Transdéamination et désamination.”LinkedIn Slideshare, 24 avril. 2014. Disponible ici
Image gracieuseté:
1.«Déamination oxydative» par Tomas Drab - propre travail, (domaine public) via Commons Wikimedia
2.«Sérine» (CC BY-SA 3.0) via Commons Wikimedia


