Différence entre le diagramme orbital et la configuration d'électrons
Le différence clé entre le diagramme orbital et la configuration électronique est que Le diagramme orbital montre les électrons dans les flèches, indiquant la rotation des électrons. Mais, la configuration d'électrons ne montre pas de détails sur la rotation des électrons.
Le diagramme orbital montre la disposition des électrons donnés par la configuration d'électrons. La configuration d'électrons donne les détails sur la distribution des électrons à travers les orbitales de l'atome. Mais, le diagramme orbital montre également la rotation des électrons. C'est la différence de base entre le diagramme orbital et la configuration d'électrons.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le diagramme orbital
3. Qu'est-ce que la configuration d'électrons
4. Comparaison côte à côte - Diagramme orbital vs configuration d'électrons sous forme tabulaire
6. Résumé
Qu'est-ce que le diagramme orbital?
Le diagramme orbital est un type de diagramme qui montre la distribution des électrons dans les orbitales d'un atome et indique la rotation de ces électrons. C'est un type de notation qui montre quelles orbitales sont remplies et lesquelles sont partiellement remplies. Ici, nous utilisons des flèches pour représenter les électrons. La direction de la pointe de flèche (vers le haut ou vers le bas) indique la rotation de l'électron.
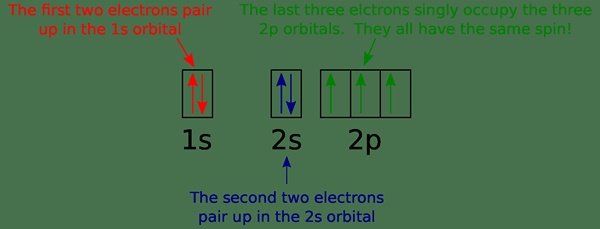
Figure 01: Diagramme orbital pour l'azote
Une orbitale peut avoir un maximum de deux électrons. Selon le principe d'exclusion de Pauli, deux électrons dans le même atome ne peuvent pas avoir le même numéro de numéro quantique. Cela signifie, même si tous les autres nombres quantiques sont les mêmes, le nombre quantique de spin est différent. Les deux électrons de la même orbitale ont une rotation opposée. L'image ci-dessus montre un exemple de diagramme orbital.
Qu'est-ce que la configuration d'électrons?
La configuration des électrons est un moyen de disposer les électrons d'un atome en montrant la distribution de ces électrons à travers les orbitales. Plus tôt, la configuration d'électrons a été développée en utilisant le modèle bohr de l'atome. Ceci est précis pour les petits atomes avec moins d'électrons, mais lorsque vous envisagez de grands atomes avec un grand nombre d'électrons, nous devons utiliser la théorie quantique pour la détermination de la distribution d'électrons.
Selon la mécanique quantique, une coque d'électrons est l'état de plusieurs électrons partageant le même numéro quantique principal, et nous nommons la coque en utilisant le nombre donné pour le niveau d'énergie et le type d'orbital que nous considérons, E.g., 2S fait référence à l'orbital S de la coquille d'électrons du 2e niveau d'énergie. De plus, il existe un motif qui décrit le nombre maximum d'électrons qu'un coque d'électrons peut contenir. Ici, ce nombre maximum dépend du nombre quantique azimutal, L. De plus, les valeurs l = 0, 1, 2 et 3 se réfèrent respectivement aux orbitales S, P, D et F. Le nombre maximum d'électrons qu'un shell peut contenir = 2 (2L + 1). Par conséquent, nous pouvons développer le tableau suivant;
| Orbital | Nombre maximum d'électrons 2 (2L + 1) |
| L = 0 est l'orbital s | 2 |
| L = 1 est l'orbital p | 6 |
| L = 2 est d orbital | dix |
| L = 3 est f orbital | 14 |

Lorsque vous envisagez la notation de la configuration d'électrons, nous devons utiliser la séquence des nombres quantiques. Par exemple, la configuration électronique de l'atome d'hydrogène est 11. Ici, cette notation indique que les atomes d'hydrogène ont un électron dans l'orbitale S de la première coque d'électrons. Pour le phosphore, la configuration d'électrons est 122s22p63s23p3. Cela signifie; L'atome de phosphore a 3 coquilles d'électrons remplies de 15 électrons.
Quelle est la différence entre le diagramme orbital et la configuration d'électrons?
Le diagramme orbital montre la disposition des électrons donnés par la configuration d'électrons. La principale différence entre le diagramme orbital et la configuration d'électrons est que le diagramme orbital montre les électrons dans les flèches indiquant la rotation des électrons. Pendant ce temps, la configuration des électrons ne montre pas de détails sur la rotation des électrons. De plus, dans le modèle de notation, les diagrammes orbitaux utilisent des flèches pour représenter les électrons, tandis que la configuration des électrons indique des électrons à l'aide de nombres.
Vous trouverez ci-dessous un résumé de la différence entre le diagramme orbital et la configuration d'électrons.
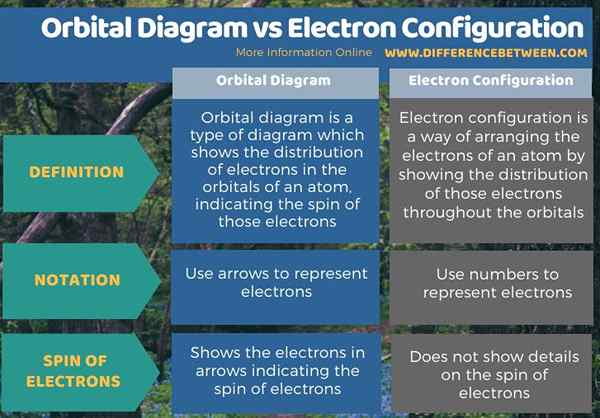
Résumé - Diagramme orbital vs configuration d'électrons
La principale différence entre le diagramme orbital et la configuration d'électrons est que le diagramme orbital montre les électrons dans les flèches indiquant le rotation des électrons, tandis que la configuration des électrons ne montre pas de détails sur le rotation des électrons.
Référence:
1. "1.4: Configuration électronique et diagrammes orbitaux.”Chemistry LibreTexts, LibreTexts, 26 septembre. 2019, disponible ici.
Image gracieuseté:
1. «Orbital Diagram Nitrogen» par CK-12 Foundation (Raster), Adrignola (vecteur) - Fichier: High School Chemistry.PDF, page 327 (domaine public) via Commons Wikimedia
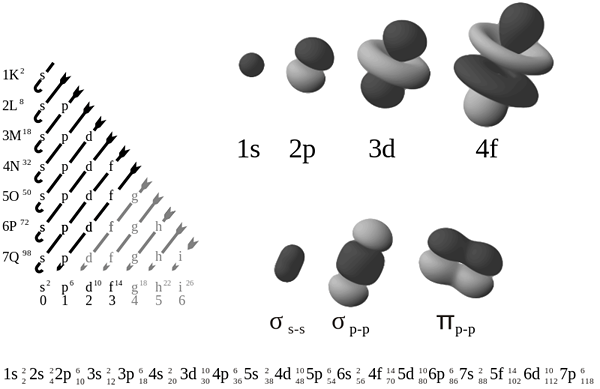
2. «Orbitales électroniques» par Patricia.Fidi - propre travail par Patricia.Fidi et Lt Paul - originaire de PL: Grafika: Orbitale.PNG, Auteur PL: Wikipedysta: Chemmix.Cette image vectorielle non spécifiée W3C a été créée avec Inkscape (domaine public) via Commons Wikimedia


