Différence entre l'acide nitrique et l'acide nitreux
Le différence clé entre l'acide nitrique et l'acide nitreux est que La molécule d'acide nitrique contient trois atomes d'oxygène liés à un atome d'azote central tandis que la molécule d'acide nitreux contient deux atomes d'oxygène liés à un atome d'azote central.
Les acides nitriques et nitreux sont des acides inorganiques d'azote. Ces deux acides contiennent des atomes d'azote, d'oxygène et d'hydrogène.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acide nitrique
3. Qu'est-ce que l'acide nitreux
4. Comparaison côte à côte - acide nitrique vs acide nitreux sous forme tabulaire
5. Résumé
Qu'est-ce que l'acide nitrique?
L'acide nitrique a la formule chimique HNO3. C'est un acide très corrosif et dangereux. De plus, il peut avoir une nature chimique diluée ou concentrée. Quoi qu'il en soit, il a des molécules d'acide nitrique dissous dans l'eau. La réaction entre le dioxyde d'azote et l'eau forme de l'acide nitrique. Il existe deux types d'acide nitrique: l'acide nitrique fumant et l'acide nitrique concentré.
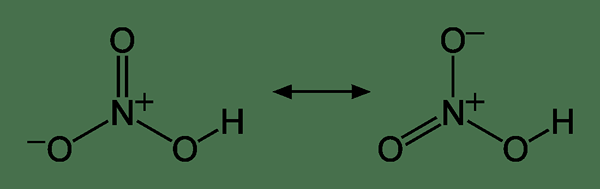
Figure 01: Structures de résonance de la molécule d'acide nitrique
L'acide nitrique fumant est un grade commercial d'acide nitrique qui a une concentration très élevée et une densité élevée. Il contient 90 à 99% HNO3. Nous pouvons préparer ce liquide en ajoutant un dioxyde d'azote excessif à l'acide nitrique. Il forme un liquide furieux incolore, jaunâtre ou brunâtre qui est très corrosif. Par conséquent, cette solution acide a des molécules gazeuses en combinaison avec l'eau; Il n'y a pas d'eau dedans. La fumée de cet acide s'élève de la surface de l'acide; Cela conduit à son nom, «fumeur». La formule chimique de ce composé est HNO3-XNON2.
L'acide nitrique concentré est simplement une solution contenant plus d'acide nitrique dans moins d'eau. Cela signifie que la forme concentrée de cet acide contient une quantité moins d'eau par rapport à la quantité de solutés. À l'échelle commerciale, 68% ou plus est considéré comme un acide nitrique concentré. De plus, la densité de cette solution est 1.35 g / cm3. Cette grande concentration ne produit pas de fumées, mais la concentration très élevée de cet acide peut dégager des fumées de couleur blanche. Nous pouvons produire ce liquide en réagissant au dioxyde d'azote avec de l'eau.
Qu'est-ce que l'acide nitreux?
L'acide nitreux est un acide inorganique ayant la formule chimique HNO2. C'est un acide faible et un acide monoprotique. Cet acide se produit dans l'état de solution, en phase gazeuse et sous forme de sel de nitrile. Cet acide est utile pour fabriquer des sels de diazonium qui sont des réactifs dans les réactions de couplage azoïque pour donner des colorants azo.

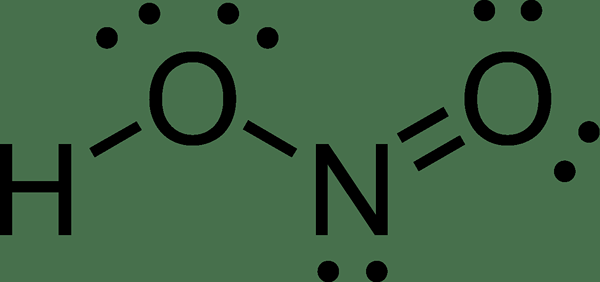
Figure 02: Structure de l'acide nitreux
Les solutions d'acide nitreux apparaissent en couleur bleu pâle. La base conjuguée de cet acide est l'ion nitrile. Dans sa phase gazeuse, l'acide nitreux est dans la géométrie plane, et il peut adopter à la fois des formes CIS et trans. L'isomère trans prédominait à température ambiante, et il est stable que l'isomère cis.
L'acide nitreux peut être préparé par l'acidification des solutions aqueuses de nitrite de sodium avec un acide minéral. Nous pouvons effectuer le processus d'acidification à des températures de glace, et le HNO2 est consommé in situ. Les molécules d'acide nitreux libres sont instables et ont tendance à se décomposer rapidement. De plus, nous pouvons produire de l'acide nitreux en dissolvant le trioxyde de dinitrogen dans l'eau.
Quelle est la différence entre l'acide nitrique et l'acide nitreux?
L'acide nitrique et l'acide nitreux sont des acides inorganiques contenant des atomes d'azote. La principale différence entre l'acide nitrique et l'acide nitreux est que la molécule d'acide nitrique contient trois atomes d'oxygène liés à un atome d'azote central tandis que la molécule d'acide nitreux contient deux atomes d'oxygène liés à un atome d'azote central.
De plus, une différence facilement identifiable entre l'acide nitrique et l'acide nitreux est que l'acide nitrique est un liquide fumant incolore, jaune pâle ou rouge tandis que l'acide nitreux est une solution de couleur bleu pâle. En plus de cela, l'acide nitrique est un acide fort que l'acide nitreux.
Ci-dessous infographie tabule les différences entre l'acide nitrique et l'acide nitreux.
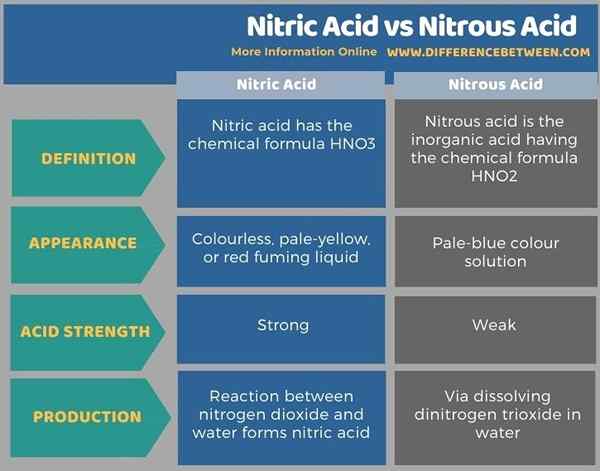
Résumé - acide nitrique vs acide nitreux
L'acide nitrique et l'acide nitreux sont des acides inorganiques contenant des atomes d'azote. La principale différence entre l'acide nitrique et l'acide nitreux est que la molécule d'acide nitrique contient trois atomes d'oxygène liés à un atome d'azote central tandis que la molécule d'acide nitreux contient deux atomes d'oxygène liés à un atome d'azote central.
Référence:
1. Acide nitreux. (n.d.). ScienceDirect. Récupéré le 13 octobre 2020, disponible ici.
Image gracieuseté:
1. «Nitric-acid-résonance-a» par Ben Mills - propre travail (domaine public) via Commons Wikimedia
2. «Nitrous Acid ACSV» par Calvero - Propre travaux (domaine public) via Commons Wikimedia


