Différence entre le lithium et les autres métaux alcalins
Le différence clé entre le lithium et les autres métaux alcalins est que le Le lithium est le seul métal alcali qui peut réagir avec de l'azote tandis que les autres métaux alcalins ne peuvent subir aucune réaction avec l'azote.
Les métaux alcalins sont les éléments du groupe 1 du tableau périodique des éléments. Cependant, il exclut l'hydrogène car il a des propriétés non métalliques. Par conséquent, les éléments chimiques que nous pouvons nommer en tant que métaux alcalins comprennent le lithium, le sodium, le potassium, le rubidium, le césium et le francium. Bien que le lithium soit membre de ce groupe, il a des propriétés exceptionnelles que les autres métaux alcalins tels que la capacité de réagir avec l'azote gazeux.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le lithium
3. Que sont les autres métaux alcalins
4. Comparaison côte à côte - lithium vs d'autres métaux alcalins sous forme tabulaire
5. Résumé
Qu'est-ce que le lithium?
Le lithium est un métal alcali. Selon la théorie du Big Bang de la création de la Terre, le lithium ainsi que l'hydrogène et l'hélium sont les principaux éléments chimiques produits aux premiers stades de la création mondiale. Le poids atomique de cet élément est 6.941, et la configuration électronique est [il] 2s1. De plus, il appartient au bloc S car il se trouve dans le groupe 1 du tableau périodique et les points de fusion et d'ébullition de cet élément sont 180.50 ° C et 1330 ° C respectivement. Il apparaît dans une couleur blanche argentée, et si nous brûlons ce métal, il donne une flamme de couleur cramoisi.

Figure 01: Lithium Metal
Ce métal est très léger et doux. Par conséquent, nous pouvons le couper simplement en utilisant un couteau. De plus, il peut flotter sur l'eau, entraînant une réaction chimique explosive. Ce métal a des propriétés uniques que d'autres métaux alcalins n'ont pas. Par exemple, c'est le seul métal alcali. C'est le plus petit élément parmi les autres membres de ce groupe. De plus, il a le moins de densité parmi les métaux solides.
Que sont les autres métaux alcalins?
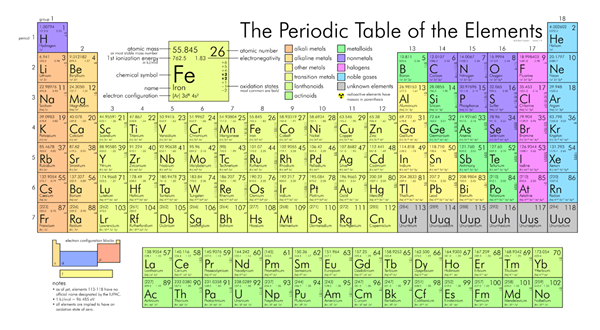
Les métaux alcalins sont les éléments chimiques du groupe 1 du tableau périodique des éléments à l'exception de l'hydrogène. Ainsi, les membres de ces groupes qui entrent dans cette catégorie sont le lithium, le sodium, le potassium, le rubidium, le césium et le francium. La raison pour laquelle nous les nommons en tant que métaux alcalins est qu'ils forment des composés alcalins.

Figure 02: Métaux alcalins en couleur rouge
Lorsqu'ils envisagent leur configuration d'électrons, ils ont leur électron le plus externe dans une orbitale S; Par conséquent, ils sont dans le bloc S du tableau périodique. L'espèce chargée la plus stable qu'ils forment est le cation monovalent.
Quelle est la différence entre le lithium et les autres métaux alcalins?
Le lithium est un métal alcali. La principale différence entre le lithium et les autres métaux alcalins est que le lithium est le seul métal alcali. De plus, le lithium ne peut pas former un anion tandis que d'autres métaux alcalins peuvent former des anions.
L'infographie ci-dessous tabule la différence entre le lithium et les autres métaux alcalins en comparaison côte à côte.
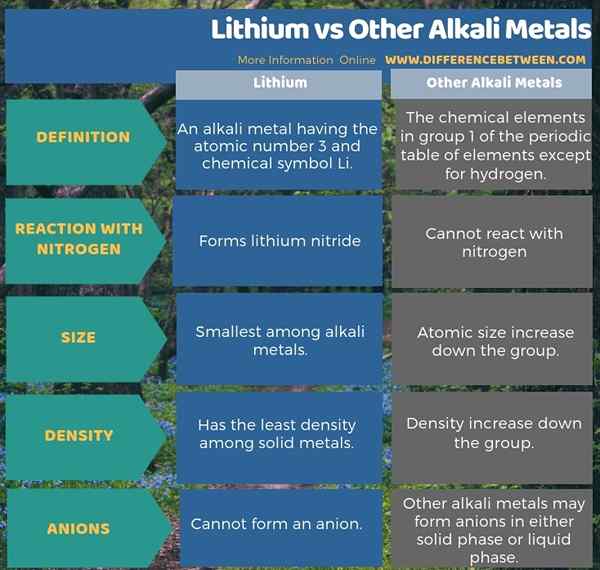
Résumé - Lithium vs d'autres métaux alcalins
Le lithium est membre du groupe de métaux alcalins. La principale différence entre le lithium et les autres métaux alcalins est que le lithium est le seul métal alcali.
Référence:
1. "Lithium.»Wikipedia, Wikimedia Foundation, 30 septembre. 2018. Disponible ici
2. «Métal alcalin.»Wikipedia, Wikimedia Foundation, 11 septembre. 2018. Disponible ici
Image gracieuseté:
1.«Lithium Paraffin» par Tomihahndorf (domaine public) via Commons Wikimedia
2.«Tableau périodique des éléments» d'ici 2012 - son propre travail (domaine public) via Commons Wikimedia


