Différence entre isopropyle et éthanol

Isopropyl vs éthanol
Les molécules organiques sont des molécules qui se composent de carbones. Les molécules organiques sont la molécule la plus abondante des êtres vivants sur cette planète. Les principales molécules organiques dans les êtres vivants comprennent les glucides, les protéines, les lipides et les acides nucléiques. Les acides nucléiques comme l'ADN contiennent des informations génétiques des organismes. Les composés en carbone comme les protéines font des composants structurels de notre corps, et ils constituent des enzymes qui catalysent toutes les fonctions métaboliques. Il existe des preuves pour prouver que des molécules carboniques comme le méthane existaient dans l'atmosphère même il y a plusieurs milliards d'années. Non seulement nous sommes composés de molécules organiques, mais il existe de nombreux types de molécules organiques autour de nous aussi que nous utilisons tous les jours à différentes fins.
Les vêtements que nous portons sont composés de molécules organiques naturelles ou synthétiques. Beaucoup de matériaux de nos maisons sont également biologiques. L'essence, qui donne de l'énergie aux automobiles et autres machines, est biologique. La plupart des médicaments que nous prenons, les pesticides et les insecticides sont composés de molécules organiques. Ainsi, les molécules organiques sont associées à presque tous les aspects de nos vies. Par conséquent, un sujet distinct en tant que chimie organique a évolué pour en savoir plus sur ces composés. Les molécules organiques sont largement classées comme composés aliphatiques et aromatiques. Ils peuvent également être classés comme des branches ou non ramifiés. Une autre catégorisation est basée sur le type de groupes fonctionnels qu'ils ont. Dans cette catégorisation, les molécules organiques sont divisées en alcanes, alcènes, alcyne, alcools, éther, amine, aldéhyde, cétone, acide carboxylique, ester, amide et haloalcanes.
Isopropyle
Le groupe propyl est un groupe d'hydrocarbures avec trois atomes de carbone. Il a sept atomes d'hydrogène connectés aux atomes de carbone, et l'ensemble du groupe est un substituant d'une molécule organique. Propyl a la formule de -ch2 Ch2 Ch3. L'isopropyl a la même formule, mais la connectivité est un peu différente. C'est donc comme une forme isomère constitutionnelle du groupe propyle. L'isopropyl a la structure suivante.
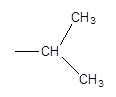
Dans la nomenclature IUPAC, il est nommé Propan-2-yl. Le groupe isopropyle n'est pas stable seul. Il est lié à une autre partie et forme une molécule complète et stable. Par exemple, l'alcool isopropylique peut être pris.
Éthanol
L'éthanol est un simple alcool avec la formule moléculaire de C2H5OH. C'est un liquide clair et incolore avec une odeur caractéristique. De plus, l'éthanol est un liquide inflammable. Le point de fusion de l'éthanol est de -114.1 oC, et le point d'ébullition est 78.5 oC. L'éthanol est polaire en raison de la différence d'électronégativité entre l'oxygène et l'hydrogène dans le groupe -OH. De plus, en raison du groupe -OH, il a la capacité de former des liaisons hydrogène.
L'éthanol est utilisé comme boisson. Selon le pourcentage d'éthanol, il existe différents types de boissons telles que le vin, la bière, le whisky, le brandy, l'arrack, etc. L'éthanol peut être facilement obtenu par le processus de fermentation du sucre à l'aide de l'enzyme zymase. Cette enzyme se présente naturellement dans la levure, donc dans la respiration anaérobie, la levure peut produire de l'éthanol. L'éthanol est toxique pour le corps, et il est converti en acétaldéhyde dans le foie, qui est également toxique. En dehors d'une boisson, l'éthanol peut être utilisé comme antiseptique pour nettoyer les surfaces des micro-organismes, et il est principalement utilisé comme carburant et additif de carburant dans les véhicules. L'éthanol est miscible avec de l'eau, et il sert également de bon solvant.
Isopropyl vs éthanol
- L'éthanol est une molécule organique et l'isopropyle n'est qu'une partie de la molécule organique.
- L'éthanol est stable et l'isopropyle n'est pas stable.
- L'isopropyl a trois atomes de carbone et l'éthanol n'a que deux atomes de carbone.
- L'isopropyle est un hydrocarbure. Dans l'éthanol, il y a un atome d'oxygène au lieu de l'hydrogène et du carbone.


