Différence entre les acides aminés hydrophobes et hydrophiles
Le différence clé entre les acides aminés hydrophobes et hydrophiles Les acides aminés hydrophobes sont non polaires tandis que les acides aminés hydrophiles sont polaires.
Les acides aminés sont les éléments constitutifs des protéines. Une protéine est une molécule de polymère géante qui est une composante essentielle de tous les organismes vivants. De plus, les acides aminés sont principalement dans deux types en tant qu'acides aminés essentiels et non essentiels. De plus, nous pouvons les classer comme des acides aminés hydrophiles et hydrophobes, selon leur nature physicochimique. Ils sont différents les uns des autres principalement en fonction de la polarité.
CONTENU
1. Aperçu et différence clé
2. Que sont les acides aminés hydrophobes
3. Que sont les acides aminés hydrophiles
4. Comparaison côte à côte - acides aminés hydrophobes vs hydrophiles sous forme tabulaire
5. Résumé
Que sont les acides aminés hydrophobes?
Les acides aminés hydrophobes sont un type d'acides aminés de nature non polaire. De même, le nom «hydrophobe» dérive car il n'interagit pas avec l'eau («hydro» - l'eau). L'eau est un solvant polaire. Étant donné que ces acides aminés sont non polaires, ils ne peuvent pas se dissoudre dans l'eau.

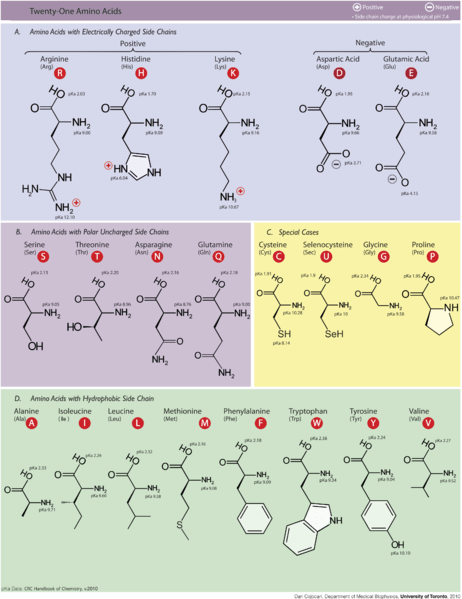
Figure 01: acides aminés essentiels
Par conséquent, la nature hydrophobe de ces composés se produit en raison des chaînes latérales qu'ils ont dans leur structure chimique. Un acide aminé a la formule générale dans laquelle un atome de carbone central est attaché avec un atome d'hydrogène, un groupe carboxyle, un groupe amine et un groupe latéral (groupe R). Ce groupe R peut être simplement un atome (atome d'hydrogène) ou une longue chaîne latérale. Ainsi, si la chaîne latérale est très longue et se compose principalement d'atomes de carbone et d'hydrogène, ils sont hydrophobes. De plus, ils ont de petits moments dipolaires. Par conséquent, ils ont tendance à se repousser de l'eau.
De plus, les acides aminés hydrophobes parmi les acides aminés essentiels sont les suivants.
- Glycine
- Alanine
- Valine
- Leucine
- Isoleucine
- Proline
- Phénylalanine
- Méthionine
- Tryptophane
Que sont les acides aminés hydrophiles?
Les acides aminés hydrophiles sont un type d'acides aminés de nature polaire. Le nom «hydrophile» dérive car il attire de l'eau. Puisque l'eau est un solvant polaire et que ces acides aminés sont également polaires, ils peuvent se dissoudre dans l'eau.
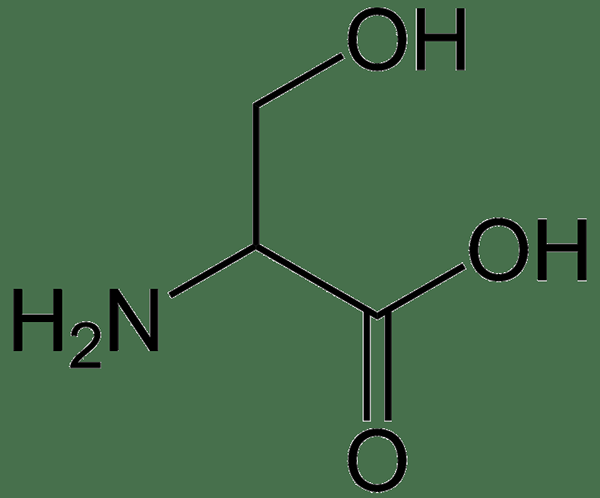
Figure 02: Acides aminés hydrophiles: sérine
Les acides aminés hydrophiles contiennent soit des chaînes latérales courtes ou une chaîne latérale avec des groupes hydrophiles. Habituellement, ces acides aminés se produisent à la surface des molécules de protéines, et elles ont de grands moments dipolaires. Par conséquent, ils ont tendance à attirer de l'eau.
De plus, les principaux acides aminés hydrophiles et hydrophiles sont les suivants:
- Sérine
- Thréonine
- Cystéine
- Asparagine
- Glutamine
- Tyrosine
Quelle est la différence entre les acides aminés hydrophobes et hydrophiles?
Les acides aminés hydrophobes sont un type d'acides aminés qui ont une nature non polaire tandis que les acides aminés hydrophiles sont un type d'acides aminés dans lesquels ont une nature polaire. Par conséquent, c'est la principale différence entre les acides aminés hydrophobes et hydrophiles. De plus, les acides aminés hydrophobes ont de longues chaînes latérales avec principalement des atomes de carbone et d'hydrogène tandis que les acides aminés hydrophiles ont des chaînes latérales courtes ou une chaîne latérale avec des groupes hydrophiles. Comme autre différence importante entre les acides aminés hydrophobes et hydrophiles, ceux hydrophobes se produisent au centre des protéines tandis que les acides aminés hydrophiles sont à la surface.
L'illustration ci-dessous montre une description détaillée de la différence entre les acides aminés hydrophobes et hydrophiles.
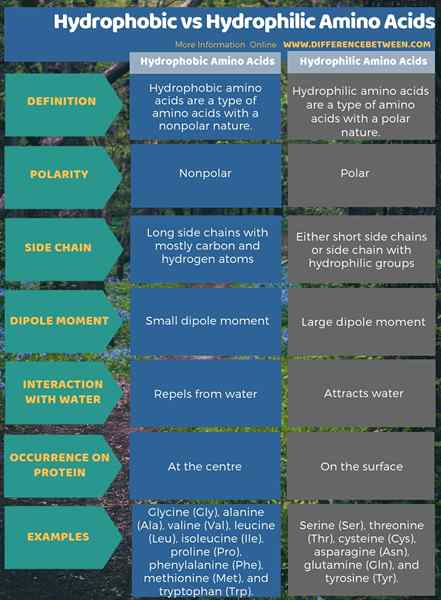
Résumé - Acides aminés hydrophobes vs hydrophiles
En bref, les acides aminés sont les éléments constitutifs des protéines. De plus, selon la polarité, il existe deux types en tant qu'acides aminés hydrophiles et hydrophobes. La principale différence entre les acides aminés hydrophobes et hydrophiles est que les acides aminés hydrophobes sont non polaires tandis que les acides aminés hydrophiles sont polaires.
Référence:
1. Reddy, Michael K. "Acide aminé.»Encyclopædia Britannica, Encyclopædia Britannica, Inc., 30 octobre. 2018. Disponible ici
Image gracieuseté:
1.«Amino Acides» par Dan Cojocar (CC By-SA 3.0) via Commons Wikimedia
2.«Serine Simple» de Sten André - Propre travaux, (domaine public) via Commons Wikimedia


