Différence entre le donneur de liaison hydrogène et l'accepteur
Le différence clé entre le donneur de liaison hydrogène et l'accepteur est que Le donneur de liaison hydrogène contient l'atome d'hydrogène qui participe à la formation de liaison hydrogène tandis que l'accepteur de liaison hydrogène contient des paires d'électrons solitaires.
Une liaison hydrogène est une liaison faible entre deux molécules résultant d'une attraction électrostatique entre un proton dans une molécule et un atome électronégatif dans l'autre. Ces deux composés qui participent à la formation de liaisons hydrogène sont appelés donneurs de liaison hydrogène et accepteur.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le donneur de liaison hydrogène
3. Qu'est-ce que l'accepteur de liaison hydrogène
4. Comparaison côte à côte - donneur de liaison hydrogène vs accepteur sous forme tabulaire
5. Résumé
Qu'est-ce que le donneur de liaison hydrogène?
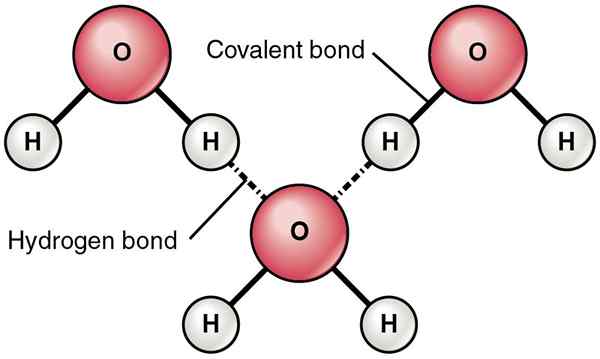
Le donneur de liaison hydrogène est le composé chimique qui contient des protons à donner. Ici, les protons sont des atomes d'hydrogène. Le donneur de liaison hydrogène doit contenir ces atomes d'hydrogène liés de manière covalente à lui-même. Par exemple, l'eau a deux atomes d'hydrogène attachés à l'atome d'oxygène directement via des liaisons chimiques covalentes. Par conséquent, il peut former des liaisons hydrogène avec d'autres molécules.

Figure 01: liaisons hydrogène entre les molécules d'eau
Bien que les aldéhydes et les cétones contiennent des atomes d'hydrogène, ils n'ont pas d'atomes d'hydrogène directement liés aux atomes d'oxygène. Par conséquent, ce ne sont pas des donneurs de liaisons hydrogène.
Qu'est-ce que l'accepteur de liaison hydrogène?
L'accepteur de la liaison hydrogène est le composé chimique qui contient les paires d'électrons solitaires qui participent à la formation de liaison hydrogène. Ce composé doit contenir un atome plus électronégatif (plus électronégatif que l'hydrogène) avec des paires d'électrons solitaires. Ensuite, il peut attirer des protons d'un donateur. De plus, les atomes électronégatifs généralement impliqués dans la liaison hydrogène sont l'oxygène, l'azote et le fluor.
Quelle est la différence entre le donneur de liaison hydrogène et l'accepteur?
Une liaison hydrogène se forme entre un donneur d'hydrogène et l'accepteur. La principale différence entre le donneur de liaison hydrogène et l'accepteur est que le donneur de liaison hydrogène contient l'atome d'hydrogène qui participe à la formation de liaison hydrogène tandis que l'accepteur de liaison hydrogène contient des paires d'électrons solitaires. Une autre différence entre le donneur de liaison hydrogène et l'accepteur est que le donneur de liaison hydrogène doit contenir des atomes d'hydrogène directement liés au composé via des liaisons covalentes tandis que l'accepteur de liaison hydrogène doit contenir un atome plus électronégatif tel que l'oxygène, l'azote et le fluor, qui contiennent des paires d'électrons solitaires.

Résumé - donneur de liaison hydrogène vs accepteur
Fondamentalement, une liaison hydrogène est une liaison qui se forme entre un donneur d'hydrogène et l'accepteur. La principale différence entre le donneur de liaison hydrogène et l'accepteur est que le donneur de liaison hydrogène contient l'atome d'hydrogène qui participe à la formation de liaison hydrogène tandis que l'accepteur de liaison hydrogène contient des paires d'électrons solitaires.
Référence:
1. «Liaison hydrogène.”Chemistry LibreTexts, LibreTexts, 5 juin 2019, disponible ici.
Image gracieuseté:
1. «210 liaisons hydrogène entre les molécules d'eau-01» par OpenStax College - Anatomy & Physiology, Connexions Web Site. 19 juin 2013 (CC par 3.0) via Commons Wikimedia


