Différence entre le gramme équivalent et le poids équivalent
Le différence clé entre le poids équivalent et le poids équivalent est que Gram Equivalent décrit que la masse d'un équivalent est donnée dans l'unité de Gram tandis que le poids équivalent décrit la masse d'un équivalent dans n'importe quelle unité de mesure.
Le poids équivalent et équivalent en gramme sont deux termes utilisés en chimie générale pour les calculs chimiques. Ces termes ont également des utilisations en chimie analytique (dans une analyse volumétrique et gravimétrique) et en chimie en polymère.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'équivalent Gram
3. Qu'est-ce que le poids équivalent
4. Comparaison côte à côte - réaction de poids équivalent en gramme vs en poids équivalent sous forme tabulaire
5. Résumé
Qu'est-ce que l'équivalent Gram?
L'équivalent en gramme est la masse d'un équivalent dans l'unité de Grams. Il décrit la masse en grammes d'un élément, d'un groupe ou d'un composé. Cependant, ce terme est différent du terme de poids équivalent basé sur l'unité de mesure. En effet, la masse peut être mesurée en différentes unités et un équivalent signifie toute partie considérée. Ensuite, la masse de cette partie est exprimée dans l'unité de mesure pour la masse de ce matériau particulier.
Qu'est-ce que le poids équivalent?
Le poids équivalent fait référence à la masse d'un équivalent d'un matériau considéré. Il peut être utilisé avec un élément, un groupe d'éléments ou un composé. De plus, ce terme peut être défini comme la masse d'une substance connue qui peut combiner ou déplacer une quantité fixe d'une autre substance. Par exemple, le poids équivalent d'un élément est la masse qui se combine avec ou déplace 1.008 grammes d'hydrogène, 8.0 grammes d'oxygène ou 35.5 grammes de chlore. Ces valeurs sont obtenues en divisant la masse atomique de la valeur de valence la plus courante; e.g. Un poids équivalent en ce qui concerne l'oxygène est obtenu par 16 gmol-1/ 2 = 8.0g.
Cependant, pour les réactions acides-base, le poids équivalent fait référence à la masse qui réagit avec une mole d'ions hydrogène. L'unité de poids équivalent est l'unité de masse. Par conséquent, ce n'est pas une valeur sans dimension. Le plus souvent, le gramme est l'unité utilisée pour mesurer le poids équivalent. À l'origine, la valeur du poids équivalent est déterminée expérimentalement. Mais, nous pouvons le calculer en utilisant également les masses molaires. Par exemple, le poids équivalent peut être calculé en divisant la masse molaire des charges électriques positives ou négatives formées à partir de la dissolution du composé.

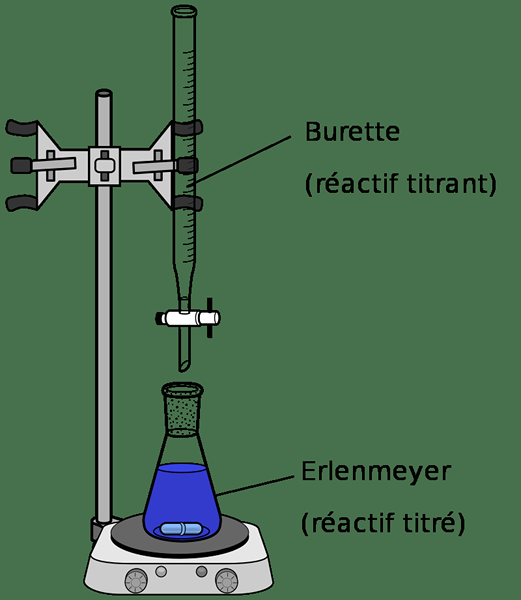
Figure 1: Un titrage acide-base (les calculs de ces techniques de titrage utilisent les poids équivalents des acides et des bases pour éviter les difficultés de calculs)
Dans les calculs chimiques généraux, nous pouvons déterminer le poids équivalent en divisant la masse molaire de la substance souhaitée à partir du nombre de moles d'ions hydrogène produits par ce composé lors de la dissolution dans l'eau. Par exemple, la masse molaire d'acide sulfurique est de 98 g / mol. Il produit deux moles d'ions hydrogène lors de la dissolution. Par conséquent, le poids équivalent est de 98/2 = 49GEQ-1.
Quelle est la différence entre le poids équivalent et le poids équivalent?
Le poids équivalent et équivalent en gramme sont des termes importants que nous utilisons dans les calculs chimiques. La principale différence entre le poids équivalent et le poids équivalent est que l'équivalent gram.
L'infographie ci-dessous résume la différence entre le poids équivalent et le poids équivalent.

Résumé - Gram équivalent vs poids équivalent
Le poids équivalent et équivalent en gramme sont des termes importants que nous utilisons dans les calculs chimiques. La principale différence entre le poids équivalent et le poids équivalent est que l'équivalent gram.
Référence:
1. "Poids équivalent.”OpenStax CNX, disponible ici.
2. "Poids équivalent.»Wikipedia, Wikimedia Foundation, 29 déc. 2019, disponible ici.
Image gracieuseté:
1. «Acid-Base-Titration-Fr» par Mehingher - Syrabas-Titringing.SVG (CC BY-SA 4.0) via Commons Wikimedia


