Différence entre les dihalides géminales et vicinale
Le différence clé entre les dihalides géminaux et vicinale est que Les dihalides géminales ont les deux groupes d'alidé.
Les termes geminaux et vicinaux sont utilisés avec des composés chimiques ayant des substituts. Ces termes distinguent les composés en fonction de l'emplacement des substituts par rapport aux autres.
CONTENU
1. Aperçu et différence clé
2. Quels sont les dihalides geminaux
3. Quels sont les dihalides vicinaux
4. Comparaison côte à côte - Dihalides geminaux vs vicinaux sous forme tabulaire
5. Résumé
Quels sont les dihalides geminaux?
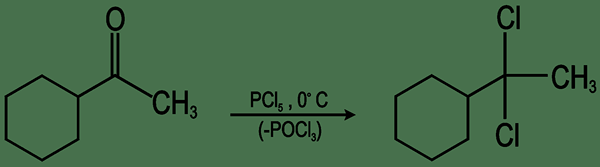
Les dihalides géminales sont des composés organiques contenant deux groupes d'halogénures attachés au même atome de carbone. Les halogénures sont les anions des atomes halogènes. Un halogène est un atome de tout élément chimique du groupe 7 du tableau périodique. Lorsque les deux groupes d'halogénures sont attachés au même atome de carbone, il rend le composé Achiral à ce point de carbone (ne montre aucune images miroir non superprimables).

Figure 01: Formation d'un dihalide geminal
De plus, l'hybridation de cet atome de carbone est soit SP2 ou SP3 car à part les deux groupes d'halogénures, il peut y avoir un ou deux atomes de carbone ou d'hydrogène liés à cet atome de carbone particulier. La géométrie autour de ce centre de carbone est soit planaire trigonale (si l'hybridation de l'atome de carbone est SP2) ou tétraédrique (si l'hybridation est SP3). Le nom général des dihalides géminaux est le dihalide d'alkylidène.
Quels sont les dihalides vicinaux?
Les dihalides vicinale sont des composés organiques ayant deux groupes d'halogénure attachés à deux atomes de carbone adjacents du même composé chimique. Le groupe halogénure peut être l'un des anions formés à partir des halogènes. Lorsque les deux groupes d'halogénures sont attachés au même atome de carbone, il est possible que le composé soit chiral s'il n'y a pas deux groupes similaires sont attachés au même carbone.
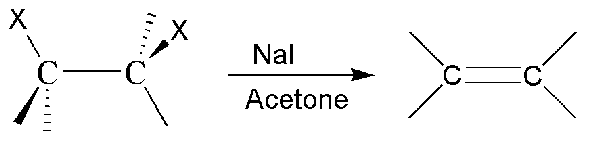
Figure 02: Formation d'un dihalide vicinal
De plus, l'hybridation du composé autour de ces deux atomes de carbone adjacentes peut être SP, SP2 ou SP3, selon le type de liaisons covalentes autour d'eux. Par exemple, s'il y a une triple liaison entre deux atomes de carbone, le composé a une hybridation SP et la géométrie autour des atomes de carbone est linéaire). De même, s'il y a une double liaison entre ces deux atomes de carbone portant les groupes d'halogénures, ce sont des atomes de carbone hybridés SP2, et la géométrie qui les entoure est planaire trigonal.
Quelle est la différence entre les dihalides géminales et vicinale?
La principale différence entre les dihalides geminaux et vicinale est que les dihalides géminales ont les deux groupes d'alidé.
Lorsque les deux groupes d'halogénures sont attachés au même atome de carbone, il rend le composé Achiral à ce point de carbone (ne montre aucune images miroir non superprimables). Lorsque les deux groupes d'halogénures sont attachés au même atome de carbone, il est possible que le composé soit chiral s'il n'y a pas deux groupes similaires sont attachés au même carbone.
Dans les dihalides géminaux, l'hybridation de l'atome de carbone portant les groupes d'halogénures est soit SP2 ou SP3 car à part les deux groupes d'halogénures, il peut y avoir un ou deux atomes de carbone ou d'hydrogène liés à cet atome de carbone particulier. Dans les dihalides vicinaux, l'hybridation du composé autour de deux atomes de carbone adjacents portant les groupes halogénures peut être SP, SP2 ou SP3, selon le type de liaisons covalentes autour d'eux.

Résumé - Dihalides geminaux vs vicinaux
Les termes geminaux et vicinaux sont utilisés avec des composés chimiques ayant des substituts. Ces termes distinguent les composés en fonction de l'emplacement des substituts par rapport les uns aux autres. La principale différence entre les dihalides geminaux et vicinale est que les dihalides géminales ont les deux groupes d'alidé.


