Différence entre les réactions du premier et du deuxième ordre
Le différence clé entre les réactions du premier et du deuxième ordre est que La vitesse des réactions du premier ordre dépend de la première puissance de la concentration du réactif dans l'équation de vitesse alors que la vitesse de réactions du second ordre dépend de la deuxième puissance du terme de concentration dans l'équation de vitesse.
L'ordre d'une réaction est la somme des pouvoirs auxquels les concentrations de réactifs sont soulevées dans l'équation de la loi. Il existe plusieurs formes de réactions selon cette définition; réactions d'ordre zéro (ces réactions ne dépendent pas de la concentration de réactifs), des réactions de premier ordre et des réactions du second ordre.
CONTENU
1. Aperçu et différence clé
2. Quelles sont les réactions de premier ordre
3. Quelles sont les réactions de second ordre
4. Comparaison côte à côte - réactions des premières contre le second ordre sous forme tabulaire
5. Résumé
Quelles sont les réactions de premier ordre?
Les réactions du premier ordre sont des réactions chimiques dont la vitesse de réaction dépend de la concentration molaire de l'un des réactifs impliqués dans la réaction. Par conséquent, selon la définition ci-dessus de l'ordre de réaction, la somme des pouvoirs auxquels les concentrations de réactifs sont augmentées dans l'équation de la loi sur la vitesse seront toujours 1. Il peut y avoir un seul réactif qui participe à ces réactions. Alors la concentration de ce réactif détermine la vitesse de la réaction. Mais parfois, il y a plus d'un réactif qui participe à ces réactions, puis l'un de ces réactifs déterminera la vitesse de la réaction.
Considérons un exemple afin de comprendre ce concept. Dans la réaction de décomposition de n2O5, il forme non2 et o2 gaz comme produits. Puisqu'il n'a qu'un seul réactif, nous pouvons écrire la réaction et l'équation de vitesse comme suit.
2n2O5 (g) → 4NO2 (g) + O2 (g)
Taux = k [n2O5 (g)]]m
Ici k est la constante de vitesse pour cette réaction et m est l'ordre de la réaction. Par conséquent, à partir des déterminations expérimentales, la valeur de m est 1. Ainsi, c'est une réaction de premier ordre.
Quelles sont les réactions de second ordre?
Les réactions du second ordre sont des réactions chimiques dont la vitesse de réaction dépend de la concentration molaire de deux des réactifs ou de la deuxième puissance d'un réactif impliqué dans la réaction. Par conséquent, selon la définition ci-dessus de l'ordre de réaction, la somme des pouvoirs auxquels les concentrations de réactifs sont augmentées dans l'équation de la loi sur la vitesse seront toujours 2. S'il y a deux réactifs, la vitesse de réaction dépendra de la première puissance de la concentration de chaque réactif.

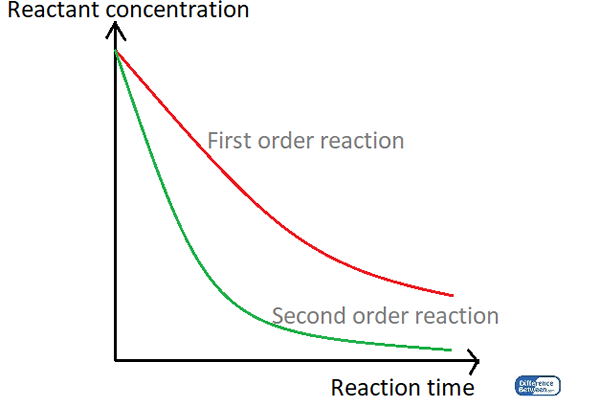
Figure 01: Un graphique comparant les deux types d'ordre de réaction en utilisant leur temps de réaction et la concentration de réactif.
Si nous augmentons la concentration d'un réactif de 2 fois (s'il y a deux réactifs dans l'équation de vitesse), alors le taux de réaction augmente de 4 fois. Par exemple, considérons la réaction suivante.
2A → P
Ici, A est un réactif et P est le produit. Ensuite, s'il s'agit d'une réaction de deuxième ordre, l'équation de vitesse de cette réaction est la suivante.
Taux = k [a]2
Mais pour une réaction avec deux réactifs différents tels que suit;
A + B → P
Taux = k [a]1[B]1
Quelle est la différence entre les réactions du premier et du deuxième ordre?
Les réactions du premier ordre sont des réactions chimiques dont la vitesse de réaction dépend de la concentration molaire de l'un des réactifs impliqués dans la réaction. Par conséquent, si nous augmentons la concentration de réactif de 2 fois, le taux de réaction augmente de 2 fois. Les réactions du second ordre sont des réactions chimiques dont la vitesse de réaction dépend de la concentration molaire de deux des réactifs ou de la deuxième puissance d'un réactif impliqué dans la réaction. Par conséquent, si nous augmentons la concentration de réactif de 2 fois, le taux de réaction augmente de 4 fois. L'infographie ci-dessous présente la différence entre les réactions du premier et du deuxième ordre sous forme tabulaire.

Résumé - Réactions des premières contre le second ordre
Il existe trois principaux types de réactions selon l'ordre de la réaction; Réactions de commande, de premier ordre et de deuxième ordre. La principale différence entre les réactions du premier et du deuxième ordre est que la vitesse d'une réaction de premier ordre dépend de la première puissance de la concentration de réactive dans l'équation de vitesse alors que la vitesse d'une réaction du second ordre dépend de la deuxième puissance du terme de concentration dans le équation de taux.
Référence:
1. LibreTexts. «Méthodes de détermination de l'ordre de réaction.”Chemistry LibreTexts, LibreTexts, 5 juin 2017. Disponible ici


