Différence entre énantiotopique et diastéréotopique

Le différence clé entre énantiotopique et diastéréotopique L'énantiotopique à terme fait référence à la capacité de former un centre chiral, tandis que le terme diastéréotopique fait référence à la capacité de former un diastéréomère.
La topicité en chimie est la relation stéréochimique entre les substituants et la structure parentale à laquelle ces substituants sont attachés. Il existe différents types de topicité en fonction de la relation telle que hétérotopique, homotopique, énantiotopique et diastéréotopique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'énantiotopique
3. Qu'est-ce que le diastéréotopique
4. Comparaison côte à côte - énantiotopique vs diastéréotopique sous forme tabulaire
5. Résumé
Qu'est-ce que l'énantiotopique?
L'énantiotopique est un terme qui décrit un phénomène où deux substituants dans une molécule sont remplacés par d'autres atomes, formant un composé chiral. Par conséquent, c'est un terme stéréochimique. Le remplacement qui peut se produire dans ce type de réactifs peut former des énantiomères. Considérons un exemple afin de comprendre le sens de ce terme.
La molécule de butane a deux atomes d'hydrogène attachés à chacun des deuxième et troisième atomes de carbone. Si nous considérons un atome de carbone, disons le deuxième atome de carbone, il y a deux atomes d'hydrogène attachés à ce centre de carbone, et nous pouvons remplacer l'un de ces atomes d'hydrogène par un autre atome tel que le brome, qui peut générer des énantiomères, E.g. (R) -2-bromobutane. De même, le remplacement de l'autre atome d'hydrogène par du brome donnera l'énantiomère de (R) -2-bromobutane, qui est (S) -2-bromobutane. Les structures sont les suivantes:
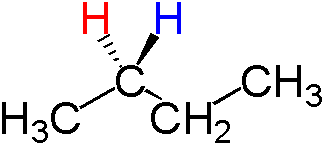
Figure 01: Structure du butane
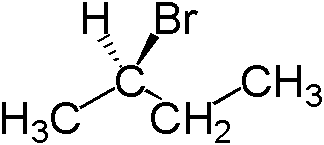
Figure 02: Structure de (R) -2-bromobutane
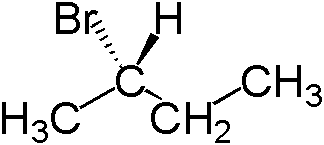
Figure 03: Structure de (s) -2-bromobutane
Habituellement, les groupes de substituants énantiotopiques sont identiques et indiscernables les uns des autres, sauf dans les composés chiraux. Par exemple, normalement les atomes d'hydrogène du carbone moyen de la molécule d'éthanol (CH3CH2OH) sont énantiotopiques, mais ceux-ci peuvent devenir diastéréotopiques si la molécule est combinée avec un centre chiral (e.g. conversion en ester).
Qu'est-ce que le diastéréotopique?
Le diastéréotopique est un terme qui décrit un phénomène où deux substituants dans une molécule sont remplacés par d'autres atomes, formant des diastéréomères. Par conséquent, c'est un terme stéréochimique. Les groupes de substituants diastéréotopiques sont souvent identiques mais pas toujours. De plus, ces groupes identiques sont généralement attachés au même atome de la molécule ayant au moins un centre chiral. Par exemple, dans la structure de (S) -2-bromobutane ci-dessus, les atomes d'hydrogène du troisième atome de carbone sont diastéréotopiques.
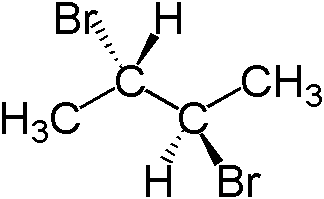
Figure 04: Structure de (2S, 3R) -2,3-Dibromobutane
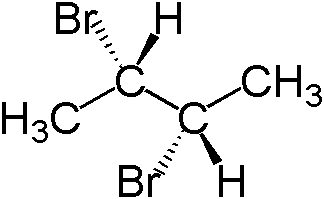
Figure 05: Structure de (2s, 3s) -2,3-dibromobutane
Les diagrammes ci-dessus indiquent que le remplacement de l'un de ces atomes d'hydrogène par un autre atome tel qu'un atome de brome peut se former (2S, 3R) -2,3-dibromobutane et le remplacement de l'autre atome d'hydrogène par un atome de brome forme le diastéréomer de ( 2s, 3r) -2,3-dibromobutane, qui est (2s, 3s) -2,3-dibromobutane.
Quelle est la différence entre l'énantiotopique et le diastéréotopique?
L'énantiotopique et le diastéréotopique sont deux types de topicité dans les composés chimiques. Ces deux types de topicité diffèrent les uns des autres en fonction du produit final qu'ils donnent lorsque les atomes sont remplacés par d'autres atomes. La principale différence entre l'énantiotopique et le diastéréotopique est que le terme énantiotopique fait référence à la capacité de former un centre chiral, tandis que le terme diastéréotopique se réfère à la capacité de former un diastéréomère.
L'infographie ci-dessous montre plus de détails sur la différence entre l'énantiotopique et le diastéréotopique.

Résumé - énantiotopique vs diastéréotopique
L'énantiotopique et le diastéréotopique sont deux types de topicité dans les composés chimiques. La principale différence entre l'énantiotopique et le diastéréotopique est que le terme énantiotopique fait référence à la capacité de former un centre chiral tandis que le terme diastéréotopique se réfère à la capacité de former un diastéréomère.
Référence:
1. «Diastéréotopique énantiotopique homotopique et hétérotopique.”Chemistryteps, disponible ici.
Image gracieuseté:
1. «Enantiotopic1» par Edgar181 - Propre travaux (domaine public) via Commons Wikimedia
2. «Enantiotopic3» par Edgar181 - Propre travaux (domaine public) via Commons Wikimedia
3. «Enantiotopic2» par Edgar181 - Propre travaux (domaine public) via Commons Wikimedia
4. «Diastéreotopic3» par Edgar181 - propre travail, domaine public) via Commons Wikimedia
5. «Diastéreotopic2» par Edgar181 - propre travail, domaine public) via les communes Wikimedia


