Différence entre Disodium EDTA et Tetrasodium EDTA
Le clé différence Entre Disodium EDTA et Tetrasodium EDTA est que Disodium edta a un pH inférieur à 7 tandis que le tétrasodium edta a un pH supérieur à 7.
EDTA est un agent chélatant. Par conséquent, il a le potentiel de se lier avec des ions métalliques tels que le calcium et le magnésium. L'EDTA représente l'acide éthylènediaminetraacétique. Il en résulte une séquestration des ions métalliques. En conséquence, l'EDTA se lie aux ions métalliques et forme un complexe EDTA stable EDTA. De plus, il existe deux formes d'EDTA, à savoir Disodium EDTA et Tetrasodium EDTA. Les deux types sont des sels de sodium d'EDTA. Disodium EDTA contient 2 cations de sodium tandis que le tétrasodium EDTA contient 4 cations de sodium par molécule.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que Disodium Edta
3. Qu'est-ce que Tetrasodium Edta
4. Similitudes entre Disodium EDTA et Tetrasodium EDTA
5. Comparaison côte à côte - Disodium edta vs tétrasodium edta sous forme tabulaire
6. Résumé
Qu'est-ce que Disodium Edta?
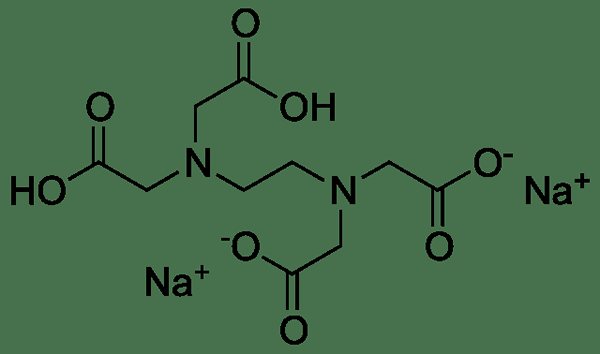
Disodium edta est une forme d'EDTA avec deux cations sodium. C'est un agent chélatant en métal lourd et présent comme une poudre sèche. La structure générale de l'EDTA contient quatre atomes d'oxygène chargés négativement. Sur les quatre, deux atomes d'oxygène de l'EDTA restent combinés avec deux cations de sodium pour former un Disodium EDTA. Par conséquent, Disodium EDTA est un sous-produit synthétisé de l'EDTA. Sa masse moléculaire est d'environ 336.2 g / mol.
L'éthylènediamine, le formaldéhyde et le cyanure de sodium participent à la synthèse de l'EDTA. Par conséquent, le cyanure de sodium est la source d'ions sodium présents dans Disodium EDTA. Le pH de Disodium EDTA varie entre 4-6. Cependant, il ne dépasse pas pH 7.

Figure 01: Disodium EDTA
Disodium EDTA est ajouté en concentrations infimes aux produits cosmétiques, y compris des shampooings pour augmenter la durée de conservation et les propriétés moussantes. Par conséquent, Disodium EDTA est présent dans les produits que nous utilisons dans nos vies quotidiennes telles que les shampooings, les colorants capillaires, les gels de douche, les lotions, etc. Il a également une utilisation en thérapeutique clinique telle que la thérapie de chélation et l'anticoagulation. De plus, Disodium EDTA est également un bon conservateur.
Qu'est-ce que Tetrasodium Edta?
Tetrasodium edta est une forme d'EDTA avec quatre cations sodium. Les quatre atomes d'oxygène chargés négativement de l'EDTA sont liés à quatre cations de sodium pour former le composé de tétrasodium EDTA. Semblable à Disodium EDTA, Tetrasodium EDTA est un sous-produit du processus de synthèse EDTA. La masse molaire de Tetrasodium EDTA est 380.1 g / mol. C'est un composé incolore disponible à la fois en poudre sèche et en liquide. Tetrasodium edta est légèrement soluble dans l'éthanol. Son pH varie de 10 à 11.
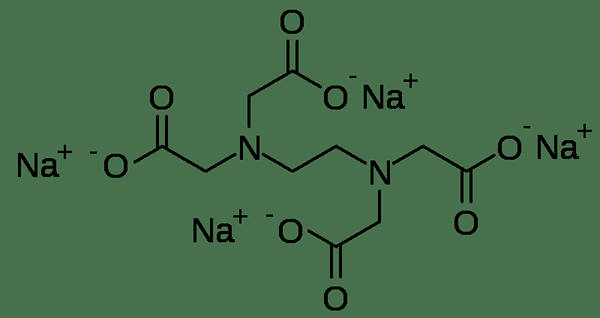
Figure 02: Tetrasodium EDTA
Tetrasodium edta est appliqué à l'échelle industrielle comme adoucisseur d'eau et conservateur. Semblable à Disodium EDTA, il a une utilisation dans la fabrication de produits de cosmétiques et de soins personnels. Tetrasodium EDTA a un potentiel plus élevé dans la séquestration des ions métalliques. Il se lie aux ions métalliques et empêche la réaction des ions métalliques avec d'autres ingrédients du produit. Par conséquent, l'ajout de celui-ci augmente la durée de conservation du produit.
Quelles sont les similitudes entre Disodium EDTA et Tetrasodium EDTA?
- Les deux composés sont des sels de sodium d'EDTA et sont des sous-produits du processus de synthèse EDTA.
- Ils sont utilisés comme conservateurs, produits de soins personnels et cosmétiques.
- De plus, Disodium EDTA et Tetrasodium EDTA entraînent une séquestration des ions métalliques.
Quelle est la différence entre Disodium EDTA et Tetrasodium EDTA?
Disodium EDTA et Tetrasodium EDTA sont deux formes d'EDTA. La principale différence entre Disodium EDTA et Tetrasodium EDTA est la valeur de pH de chaque composé. Le pH de Disodium EDTA varie entre 4 et 6 tandis que le pH du tétrasodium EDTA varie entre 10 et 11. De plus, Disodium EDTA a deux atomes de sodium tandis que le tétrasodium EDTA a quatre atomes de sodium. Ainsi, c'est aussi une différence entre Disodium EDTA et Tetrasodium EDTA.
De plus, nous pouvons également identifier une différence entre Disodium EDTA et Tetrasodium EDTA en fonction de leurs masses moléculaires. La masse moléculaire de Disodium EDTA est 336.2 g / mol tandis que la masse moléculaire du tétrasodium edta est 380.1 g / mol.

Résumé - Disodium edta vs tetrasodium edta
L'EDTA est l'acide éthylènediaminetraacétique. Il en résulte une séquestration des ions métalliques. Il se lie aux ions métalliques et forme un complexe EDTA stable EDTA. En conséquence, les deux formes de l'EDTA sont Disodium EDTA et Tetrasodium EDTA. La principale différence entre Disodium EDTA et Tetrasodium EDTA est que Disodium EDTA a un pH inférieur à 07 tandis que Tetrasodium EDTA a un pH supérieur à 07. De plus, Disodium EDTA contient 2 cations de sodium tandis que le tétrasodium EDTA contient 4 cations de sodium par molécule. Les deux composés sont des sels de sodium d'EDTA et sont des sous-produits du processus de synthèse EDTA. Ainsi, cela résume la différence entre Disodium EDTA et Tetrasodium EDTA.
Référence:
1. Amara. «Disodium Edta: ce que vous devez savoir •.”Bamboocore Fitness, 20 novembre. 2018. Disponible ici
2. «EDTA: utilisations, effets secondaires, interactions, dosage et avertissement.»WebMD, WebMD. Disponible ici
Image gracieuseté:
1.«Disodium Edta» par Andel (Talk) - Propre travaux, (domaine public) via Commons Wikimedia
2.«Tetrasodium Edta» par l'utilisateur: Edgar181 - propre travail, (domaine public) via Commons Wikimedia


