Différence entre la dilution et la concentration
Le différence clé entre la dilution et la concentration est que La dilution fait référence à l'ajout de plus de solvant alors que la concentration se réfère à l'élimination du solvant.
Les concepts de dilution et de concentration sont très significatifs dans l'étude des solutions en chimie. Par conséquent, la quantité de soluté dans un solvant décide des propriétés d'une solution et cette quantité restant la même; Nous pouvons faire une solution «diluée» ou «concentrée» en ajoutant du solvant et en supprimant une partie du solvant de la solution. Ainsi, dans l'analyse chimique, nous devons modifier la concentration d'une solution souvent dans différentes applications.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la dilution
3. Qu'est-ce que la concentration
4. Comparaison côte à côte - dilution vs concentration sous forme tabulaire
5. Résumé
Qu'est-ce que la dilution?
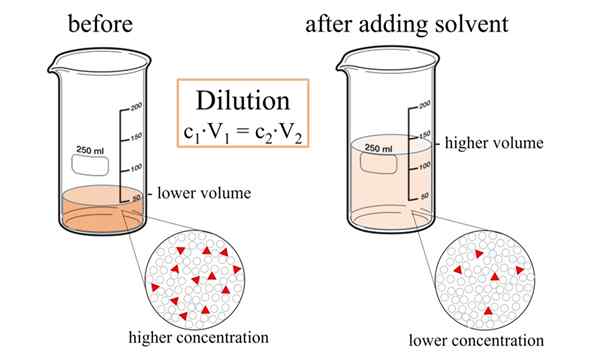
La dilution est le processus de diminution de la concentration de solutés dans une solution en ajoutant plus de solvant. Ainsi, nous pouvons réduire la quantité de solutés présents dans un volume unitaire de la solution. Si nous nous référons à «à diluer», cela signifie «pour ajouter plus de solvant sans ajouter de solutés». Cependant, après l'ajout du solvant, nous devons bien mélanger la solution afin d'obtenir une solution homogène.

Figure 01: Processus de dilution
Selon l'équation suivante, nous pouvons déterminer la concentration finale de la solution après le processus de dilution.
C1v1 = C2v2
Où, C1 est une concentration initiale, V1 est le volume initial de la solution, C2 est la concentration après dilution et V2 est la concentration finale de la solution. Par exemple, si nous ajoutons 5 ml d'eau à 95 ml d'une solution aqueuse de NaCl (1 mol / L), alors la dilution donne un 0.Solution 95 mol / L. Par conséquent la concentration est réduite.
Qu'est-ce que la concentration?
La concentration est le processus d'augmentation de la concentration de solutés dans une solution. En d'autres termes, il diminue la quantité de solvant ou augmente la quantité de solutés. Par conséquent, c'est le processus d'augmentation de la quantité de solutés présents dans un volume unitaire de la solution.

Figure 02: Le processus de concentration assombrit la solution '
Une solution concentrée contient une quantité élevée de solutés par rapport à une solution diluée. Nous pouvons déterminer la concentration de la solution après l'avoir concentrée en utilisant la même équation donnée ci-dessus (sous la dilution subtopique).
Quelle est la différence entre la dilution et la concentration?
La dilution est le processus de diminution de la concentration de solutés dans une solution en ajoutant plus de solvant tandis que la concentration est le processus d'augmentation de la concentration de solutés dans une solution. Ainsi, la principale différence entre la dilution et la concentration est que la dilution se réfère à l'ajout de plus de solvant alors que la concentration se réfère à l'élimination du solvant. Nous pouvons diluer une solution en ajoutant plus de solvant ou en éliminant les solutés tandis que le processus de concentration implique soit l'ajout de plus de solutés, soit l'élimination du solvant.
L'infographie ci-dessous fournit plus de détails sur la différence entre la dilution et la concentration.

Résumé - Dilution vs concentration
La dilution et la concentration sont très importantes en chimie pour préparer une solution avec la concentration souhaitée. De plus, ces processus de dilution et de concentration sont très importants en chimie analytique. La principale différence entre la dilution et la concentration est que la dilution se réfère à l'ajout de plus de solvant alors que la concentration se réfère à l'élimination du solvant.
Référence:
1. «Dilution (équation).»Wikipedia, Wikimedia Foundation, 22 septembre. 2018. Disponible ici
Image gracieuseté:
1.«Dilution» par Theislikerice - Propre travaux, (CC BY-SA 4.0) via Commons Wikimedia
2.«Dilution-Concentration Exemple simple» par les premierspricles (domaine public) via Commons Wikimedia


