Différence entre le cypionate et le propionate
Le différence clé entre le cypionate et le propionate est que le cypionate est la base conjuguée de l'acide cypionique, tandis que le propionate est la base conjuguée de l'acide propionique.
L'acide cypionique et l'acide propionique sont des composés organiques. Les formes anioniques ou la base conjuguée de ces molécules acides sont des ions cypionates et des ions propionate, respectivement. L'acide cypionique et l'acide propionique sont des composés d'acide carboxylique contenant des groupes fonctionnels -coh.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le cypionate
3. Qu'est-ce que le propionate
4. Similitudes - cypionate et propionate
5. Cypionate vs propionate sous forme tabulaire
6. Résumé - Cypionate vs propionate
Qu'est-ce que le cypionate?
Le cypionate est la base conjuguée de l'acide cypionique. L'acide cypionique est un acide carboxylique aliphatique ayant la formule chimique C8H14O2. L'anion formé à partir de cet acide est du cypionate, mais les sels et les esters de l'acide cypionique sont également connus sous le nom de cypionate, sous le nom de nom collectif.
L'acide cypionique a ses principales utilisations dans les formulations pharmaceutiques. Il est important de préparer des promédicaments ester, ayant une demi-vie accrue par rapport au composé parent. Dans la molécule d'acide cypionique, le groupe cypionate permet au promédicament de subir une séquestration dans les dépôts de graisse après les injections de message. Les médicaments les plus courants contenant l'anion cypionate comprennent le cypionate de testostérone, le cypionate d'estradiol, le cypionate d'hydrocortisone, le cypionate d'oxabolone, etc.
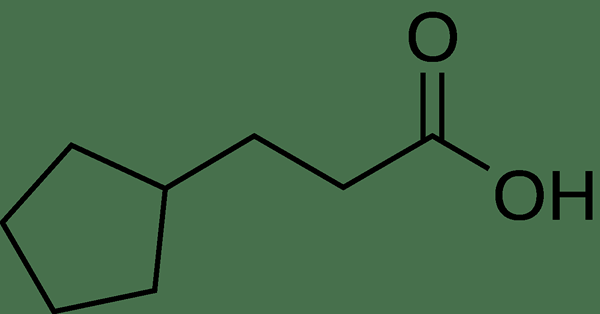
Figure 01: La structure chimique de la molécule d'acide cypionique
La formule chimique de l'anion cypionate est C8H13O2-. Il se forme à partir de l'élimination d'un atome d'hydrogène de l'acide cypionique. Cet atome d'hydrogène élimine le -COOH (groupe carboxylique) de la molécule d'acide cypionique. La masse molaire de cet anion est 141.2 g / mol. Lorsque l'on considère la nature chimique du cypionate, il a une structure cyclique liée à une courte chaîne de carbone où la fraction chimique -coo se produit à la borne de cette chaîne de carbone.
Qu'est-ce que le propionate?
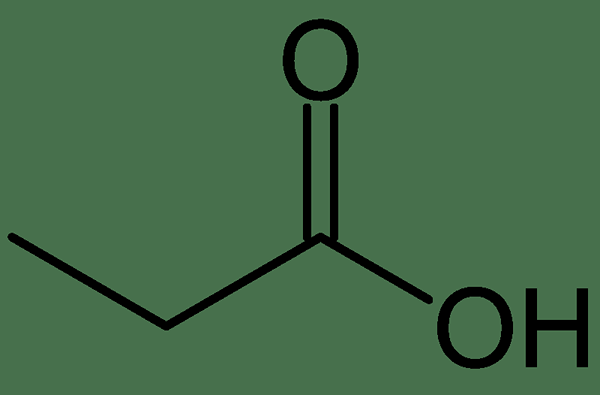
Le propionate est la base conjuguée de l'acide propionique. C'est un composé acide carboxylique naturel ayant la formule chimique ch3Ch2COOH. C'est un composé aliphatique, et il n'y a pas de structures aromatiques ou cycliques dans cette molécule. Par conséquent, l'anion propionate est également une structure aliphatique. Les sels et les esters de l'acide propionique sont collectivement nommés propionates. Ces propionates se produisent généralement à l'état liquide et ont également une odeur piquante.

Figure 02: Structure chimique de l'acide propionique
La formule chimique de l'anion propionate est C3H5O2-. La masse molaire de cet anion est 73.1 g / mol. Il est formé à partir de l'élimination d'un atome d'hydrogène de la molécule d'acide propionique où l'atome d'hydrogène lié au groupe acide carboxylique (-COOH) se sépare, laissant une charge négative.
Quelles sont les similitudes entre le cypionate et le propionate?
- Le cypionate et le propionate sont des bases conjuguées.
- Les deux anions se forment à partir d'un acide carboxylique.
- Ils se forment à travers l'élimination d'un atome d'hydrogène du groupe fonctionnel -COOH.
Quelle est la différence entre le cypionate et le propionate?
Le cypionate et le propionate sont des anions formés à partir de l'acide cypionique et de l'acide propionique. Par conséquent, la principale différence entre le cypionate et le propionate est que le cypionate est la base conjuguée de l'acide cypionique, tandis que le propionate est la base conjuguée de l'acide propionique. De plus, le cypionate contient une structure cyclique dans l'anion, tandis que le propionate est une structure linéaire.
L'infographie suivante présente la différence entre le cypionate et le propionate sous forme tabulaire.
Résumé - Cypionate vs propionate
L'acide cypionique et l'acide propionique sont des composés organiques que nous pouvons catégoriser les composés d'acide carboxylique. La principale différence entre le cypionate et le propionate est que le cypionate est la base conjuguée de l'acide cypionique, tandis que le propionate est la base conjuguée de l'acide propionique.
Référence:
1. «Propionate." Centre national d'information sur la biotechnologie. Base de données de composés PubChem, U.S. Bibliothèque nationale de médecine.
Image gracieuseté:
1. «Cypionic Acid» par Ed (Edgar181) - Propre travaux (domaine public) via Commons Wikimedia
2. «Structure chimique en acide propionique» par хорев сергей - propre travail (domaine public) via Commons Wikimedia


