Différence entre cuprous et cuprique
Différence clé - Cuprous contre Cuprique
Les cations stables formées par le cuivre, qui est un élément de bloc D, sont un cation cupreux et un cation cuprique. Les ions cuprous et cupriques sont différents les uns des autres en fonction de leurs configurations électroniques. Le différence clé entre cuprous et cuprique Cuprous est cuivre 1+ cation tandis que le Cupric est du cuivre +2 cation.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que Cuprous
3. Qu'est-ce que Cupric
4. Similitudes entre cuprous et cuprique
5. Comparaison côte à côte - Cuprous vs Cupric sous forme tabulaire
6. Résumé
Qu'est-ce que Cuprous?
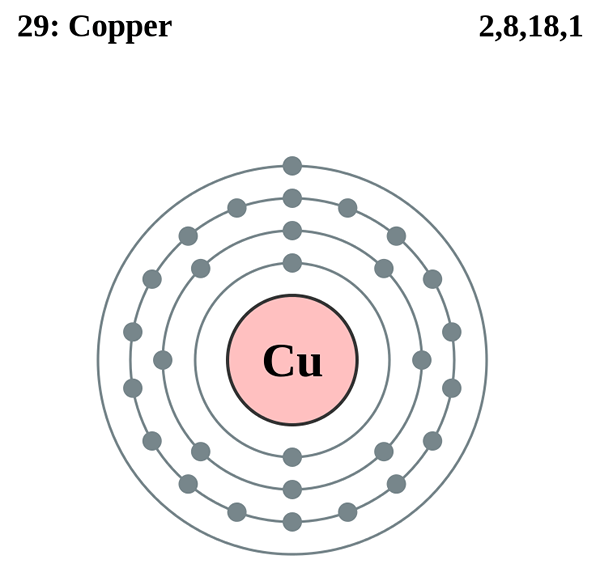
Le nom Cuprous est donné au +1 cation formé par l'atome de cuivre. Il est indiqué par Cu+1. La configuration électronique de l'atome de cuivre est [ar] 3ddix 4s1. Lorsque le cation cuprous est formé, la configuration d'électrons est [ar] 3Ddix 4s0. Par conséquent, le cation cuprume est formé lorsqu'un électron est retiré de l'atome de cuivre. Étant donné que le cation cuprume peut se lier avec un seul autre anion avec un état d'oxydation -1, le cation cuprume est connu comme un cation monovalent. La configuration électronique de Cuprous Cation est très stable. Il y a donc, de nombreux composés formés par ce cation. Quelques exemples sont présentés ci-dessous:
- Oxyde cuprume (Cu2O)
- Iodure cuprous (CUI)
- Sulfure cuprume (Cu2S)
L'énergie d'hydratation d'une molécule ou d'une ion est la quantité d'énergie libérée lorsqu'une mole de ce composé Hydratation U8ndergo (dissolution dans l'eau).

Figure 01: La structure atomique du cuivre
L'ion cuprume a une faible énergie d'hydratation par rapport à l'ion cuprique car le Ddix La configuration d'électrons dans un ion cuprume est stable que le D9 Configuration d'électrons en ion cuprique.
Qu'est-ce que Cupric?
Le nom Cupric est donné au cation +2 formé par l'atome de cuivre. Il est indiqué par Cu2+. La configuration électronique de l'atome de cuivre est [ar] 3ddix 4s1. Lorsque le cation cuprique est formé, la configuration d'électrons est [ar] 3D9 4s0. Le cation cuprique est formé lorsque deux électrons sont retirés d'un atome de cuivre, donnant à l'atome une charge électrique 2+. Le cation cuprique peut se lier avec deux anions ayant un état d'oxydation -1 ou un anion ayant un état d'oxydation -2. Par conséquent, le cation cuprique est un cation divalent. Les composés formés avec ce cation comprennent des suites:
- Oxyde cuprique (CUO)
- Iodure de cuprique (CUI)
- Sulfure de cuprique (CUS)
Quelles sont les similitudes entre Cuprous et Cupric?
- Cuprous et Cupric sont des cations formées à partir de la perte d'électrons d'un atome de cuivre.
- Les deux sont des cations stables.
- Les deux ont une charge électrique positive.
- Les deux ont la même masse atomique (car la masse d'un électron est négligeable).
Quelle est la différence entre Cuprous et Cupric?
Cuprous vs Cupric | |
| Le nom Cuprous est donné au +1 cation formé par l'atome de cuivre. | Le nom Cupric est donné au cation +2 formé par l'atome de cuivre. |
| Catégorie | |
| Les ions cuprous sont des cations monovalentes. | Les ions cupriques sont des cations divalents. |
| Configuration d'électrons | |
| La configuration électronique de l'ion cuprous est [ar] 3ddix 4s0. | La configuration électronique de l'ion cuprique est [ar] 3d9 4s0. |
| L'électron perdu pour former un atome de cuivre | |
| L'ion cuprous est formé lorsqu'un électron est perdu de l'atome de cuivre. | L'ion cuprique est formé lorsque deux électrons sont perdus de l'atome de cuivre. |
| La stabilité | |
| La stabilité de l'ion cupreux est élevée en raison du Ddix configuration d'électrons. | La stabilité de l'ion cuprique est faible en raison du D9 configuration d'électrons. |
| Dénotation | |
| L'ion cuprous est indiqué par Cu+1. | L'ion cuprique est indiqué par Cu2+. |
| Charge électrique | |
| L'ion cuprous a +1 charge électrique. | L'ion cuprique a une charge électrique +2. |
| Énergie d'hydratation | |
| L'énergie d'hydratation de l'ion cuprume est faible par rapport à l'ion cuprique. | L'énergie d'hydratation de l'ion cuprique est élevée par rapport à l'ion cuprume. |
Résumé - Cuprous contre Cuprique
L'ion cuprous et l'ion cuprique sont des cations formées à partir d'atome de cuivre en raison de la perte d'électrons. La différence entre le cuprous et le cuprique est que le cuprous est un cation cuivre 1+ tandis que le Cupric est du cuivre +2 cation.
Référence:
1. "Cuivre.»Wikipedia, Wikimedia Foundation, 3 avril. 2018. Disponible ici
2. «Cation cuprique.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine. Disponible ici
Image gracieuseté:
1.'Electron Shell 029 Copper' (CC BY-SA 2.0 UK) via Commons Wikimedia


