Différence entre l'acide carbonique et l'acide carbolique
Le différence clé entre l'acide carbonique et l'acide carbolique est que L'acide carbonique est un composé d'acide carboxylique, tandis que l'acide carbolique est un alcool.
Bien que les termes de l'acide carbonique et de l'acide carbolique semble similaire, ils se réfèrent à deux composés chimiques différents. L'acide carbonique est H2CO3 tandis que l'acide carbolique est c6H5OH. Ils ont des propriétés chimiques et physiques différentes.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acide carbonique
3. Qu'est-ce que l'acide carbolique
4. Comparaison côte à côte - acide carbonique vs acide carbolique sous forme tabulaire
5. Résumé
Qu'est-ce que l'acide carbonique?
L'acide carbonique est H2CO3. Parfois, nous donnons ce nom aux solutions ayant un dioxyde de carbone dissous dans l'eau ou l'eau gazeuse. C'est parce que l'eau gazeuse contient une petite quantité de h2CO3. De plus, il s'agit d'un acide faible, et il peut former deux types de sels en tant que carbonates et bicarbonates. La masse molaire du composé est 62.024 g / mol.
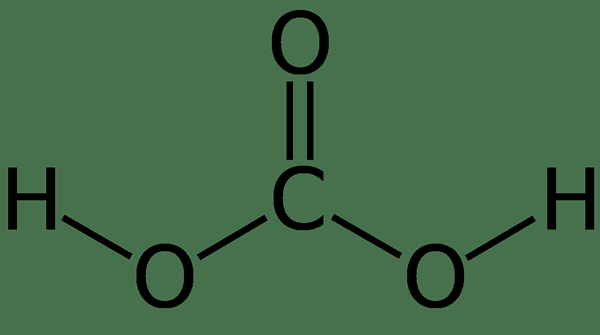
Lorsque le dioxyde de carbone se dissout dans l'eau, ce composé entre un équilibre entre le dioxyde de carbone et l'acide carbonique. L'équilibre est le suivant;
CO2 + H2O ⟷ H2CO3

Figure 01: Structure de l'acide carbonique
Si nous ajoutons un excès d'acide carbonique à une base, il donne du bicarbonate. Mais, s'il y a un excès de base, alors l'acide carbonique a tendance à donner des sels gazeux. Plus précisément, l'acide carbonique est un composé d'acide carboxylique qui a deux substituants de groupe hydroxyle attachées au carbone carbonyle. De plus, c'est un acide polyprotique, qui est capable de donner des protons. Il a deux protons amovibles; Ainsi, c'est spécifiquement diprotique.
Qu'est-ce que l'acide carbolique?
L'acide carbolique est C6H5OH. C'est un composé organique. Le nom commun de ce composé est le «phénol». Il a un anneau de benzène avec l'un de ses atomes d'hydrogène remplacé par un groupe hydroxyle. Il se produit comme un solide cristallin blanc volatil. L'acidité de ce composé est légère, mais nous devons faire attention lors de la manipulation en raison des brûlures chimiques qu'elle peut provoquer. La masse molaire du composé est 94.13 g / mol. Il a une odeur douce car c'est un composé aromatique.
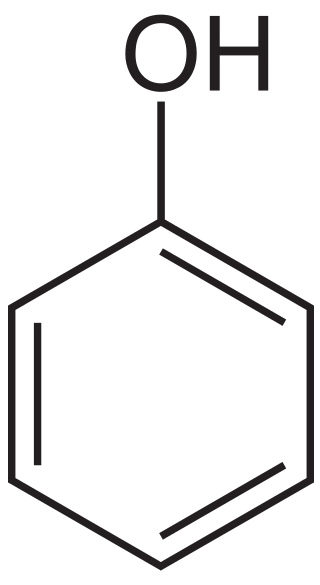
Figure 02: Structure de l'acide carbolique
De plus, c'est un acide faible et en solution aqueuse, il existe en équilibre avec des anions phénolat. Le pH de cette solution aqueuse peut aller de 8 à 12. En raison de la stabilisation de résonance de ce composé, le phénol est plus acide que les acides faibles aliphatiques correspondants.
Quelle est la différence entre l'acide carbonique et l'acide carbolique?
L'acide carbonique est H2CO3 tandis que l'acide carbolique est c6H5OH. La principale différence entre l'acide carbonique et l'acide carbolique est que l'acide carbonique est un composé d'acide carboxylique, tandis que l'acide carbolique est un alcool.
De plus, une autre différence entre l'acide carbonique et l'acide carbolique est que bien que les deux soient des acides faibles, l'acide carbolique est plus acide que l'acide carbonique en raison de l'effet de stabilisation de résonance dans le composé.
L'infographie ci-dessous montre plus de comparaisons liées à la différence entre l'acide carbonique et l'acide carbolique.
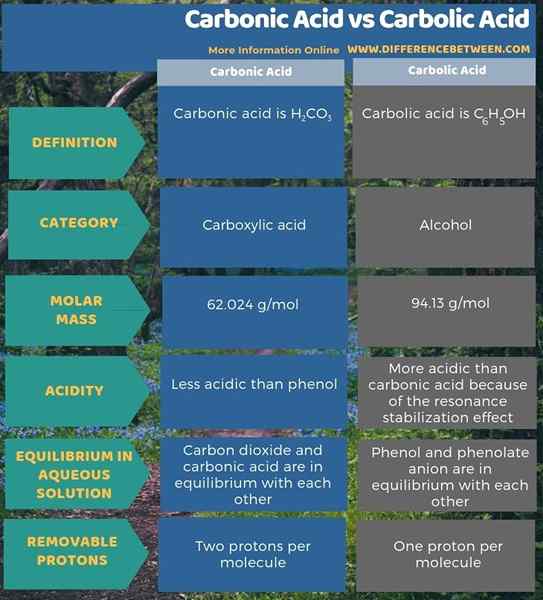
Résumé - Acide carbonique vs acide carbolique
L'acide carbonique est H2CO3 tandis que l'acide carbolique est c6H5OH. La principale différence entre l'acide carbonique et l'acide carbolique est que l'acide carbonique est un composé d'acide carboxylique, tandis que l'acide carbolique est un alcool.
Référence:
1. "Phénol." Wikipédia, Fondation Wikimedia, 10 juillet 2019, disponible ici.
Image gracieuseté:
1. «Carbonic-acid-2d» par Eetwartti - propre travail basé sur l'image: carbonic-acid-2d.PNG (domaine public) via Commons Wikimedia
2. «PHENOL2» par Neurotiker - Propre travaux (domaine public) via Commons Wikimedia


