Différence entre le bore et le borax

Le différence clé entre le bore et le borax est que le Le bore est un élément chimique tandis que le borax est un composé chimique. De plus, Borax est un composé contenant du bore, et c'est un minéral.
Bien que les noms boron et borax semblent presque similaires, ils sont différents les uns des autres selon la nature chimique. Discutons de plus de détails sur eux.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le boron
3. Qu'est-ce que Borax
4. Comparaison côte à côte - bore vs borax sous forme tabulaire
5. Résumé
Qu'est-ce que le boron?
Le bore est un élément chimique ayant le symbole B et le numéro atomique 5. Son abondance dans la croûte terrestre est très faible, et c'est aussi un élément trace du système solaire. C'est un métalloïde et la plupart du temps, et il ne se produit pas naturellement. De plus, le boron est dans le groupe 13 et la période 2 du tableau périodique. Par conséquent, c'est le premier membre du bloc P. C'est parce qu'il a un seul électron dans l'orbital 2p. À la pression et à la température standard, il existe comme un solide. Le point de fusion et le point d'ébullition sont respectivement de 2076 ° C et 3927 ° C.

Figure 01: Structures moléculaires du bore
Le bore peut former des réseaux moléculaires similaires au carbone. Ces structures ont des liaisons covalentes entre les atomes de bore. Ces structures sont les allotropes du bore. Le comportement chimique de cet élément ressemble au silicium. Le bore cristallin est très peu réactif; Ainsi, il ne réagit pas avec HF ou HCl lors du chauffage. De plus, le bore forme des oxydes, des sulfures, des nitrures et des halogénures avec son état d'oxydation le plus courant; +3 État d'oxydation.
Qu'est-ce que Borax?
Le borax est un composé inorganique ayant la formule chimique na2B4O7· 10h2O. C'est un sel d'acide borique. Il existe comme un solide blanc composé de cristaux doux et incolores. Ces cristaux sont solubles dans l'eau. Habituellement, ce composé existe comme la forme decahydrate. Le nom IUPAC de ce composé est le décahydrate tétraboré de sodium. La masse molaire de la forme de décahydrate est 381.4 g / mol. Le point de fusion et les points d'ébullition sont respectivement de 743 ° C et 1 575 ° C.

Figure 02: cristaux borax
Le nom Borax fait référence à une collection de composés qui comprend des formes anhydres et hydratées de borax. Ex: forme pentahydrate, forme de décahydrate. Il réagit avec l'acide borique formant des acides HCl.
N / A2B4O7· 10h2O + 2 HCl → 4 H3Bêle3 + 2 NaCl + 5 H2O
Ce composé se produit naturellement dans les dépôts d'évaporite; Ces dépôts se forment en raison de l'évaporation répétée des lacs saisonniers. Nous pouvons affiner ce composé via la recristallisation. En plus de cela, ce composé est utile en tant qu'agent de nettoyage, pour faire des tampons, comme source d'ions borate pour agir comme agent de co-complexe, etc.
Quelle est la différence entre le boron et le borax?
Le bore est un élément chimique ayant le symbole B et le numéro atomique 5 tandis que le borax est un composé inorganique ayant la formule chimique2B4O7· 10h2O. Par conséquent, la principale différence est que le bore est un élément chimique tandis que le borax est un composé chimique. De plus, le point de fusion et les points d'ébullition du bore sont respectivement de 2076 ° C et 3927 ° C. En revanche, le point de fusion et les points d'ébullition de Borax sont respectivement de 743 ° C et 1 575 ° C. L'infographie ci-dessous présente plus de détails sur la différence entre le boron et le borax.
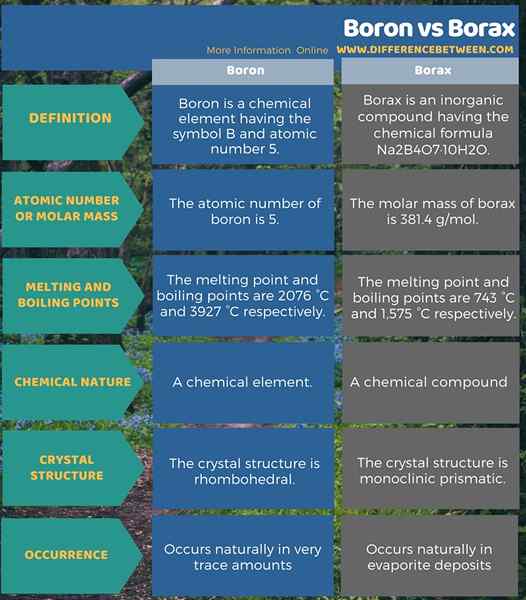
Résumé - Boron vs Borax
Borax est un composé de bore. Cependant, ils sont très différents les uns des autres dans la nature chimique. La principale différence entre le bore et le borax est que le bore est un élément chimique tandis que le borax est un composé chimique.
Référence:
1. "Bore.»Wikipedia, Wikimedia Foundation, 24 juillet 2018. Disponible ici
2. "Borax.»Wikipedia, Wikimedia Foundation, 23 juillet 2018. Disponible ici
Image gracieuseté:
1.'Boron R105' par James L Marshall (CC par 3.0) via Commons Wikimedia
2.«Borax Crystals» par Aram Dulyan (utilisateur: aramgutang) - propre travail, (domaine public) via Commons Wikimedia


