Différence entre l'acide benzoïque et l'éthyle benzoate
Le différence clé entre l'acide benzoïque et l'éthyle benzoate est que le L'acide benzoïque contient un anneau de benzène attaché à un groupe d'acide carboxylique, tandis que l'éthyle benzoate contient un anneau de benzène attaché à un groupe d'ester.
L'acide benzoïque est un acide carboxylique aromatique tandis que l'éthyle benzoate est un ester aromatique. Comme ce sont des composés aromatiques, ces deux composés ont une odeur douce et agréable.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acide benzoïque
3. Qu'est-ce que le benzoate d'éthyle
4. Comparaison côte à côte - acide benzoïque vs benzoate d'éthyle sous forme tabulaire
5. Résumé
Qu'est-ce que l'acide benzoïque?
L'acide benzoïque est un acide carboxylique avec la formule chimique C7H6O2. C'est l'acide carboxylique aromatique le plus simple, et il se produit comme un solide cristallin incolore. En outre, ce composé se produit naturellement dans de nombreuses plantes car il agit comme intermédiaire dans la production de métabolites secondaires.
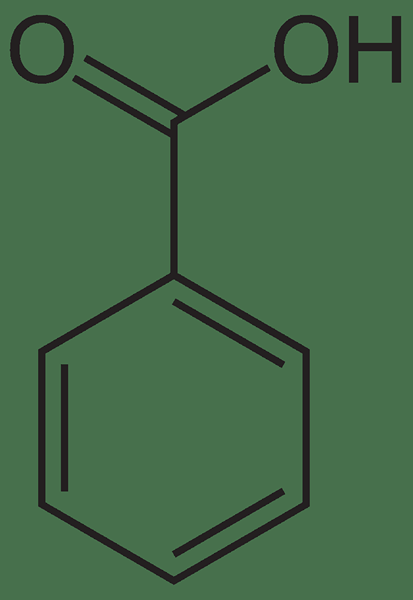
Figure 01: Structure chimique de l'acide benzoïque
De plus, la masse molaire est de 122.12 g / mol. Il a une odeur agréable. Son point de fusion est de 122 ° C, tandis que le point d'ébullition est de 250 ° C. Pour les besoins industriels, nous pouvons produire ce matériau via une oxydation partielle du toluène en présence d'oxygène. De plus, le nom de ce composé provient de sa structure, qui a un anneau de benzène avec un groupe d'acide carboxylique attaché.
Lorsque vous envisagez les utilisations de l'acide benzoïque, il est important dans la production de phénol, comme précurseur de la production de plastifiants, un précurseur de la production de benzoate de sodium, qui est un conservateur alimentaire utile, etc.
Qu'est-ce que le benzoate d'éthyle?
Le benzoate d'éthyle est un ester aromatique avec la formule chimique C9HdixO2. Le composé est formé à partir de la condensation de l'acide benzoïque et de l'éthanol. Il se produit comme un liquide incolore qui a une odeur de WinterGreen douce. La masse molaire est de 150.177 g / mol. Son point de fusion est de -34 ° C tandis que le point d'ébullition varie de 211 à 213 ° C.

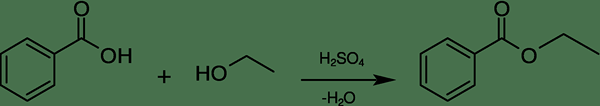
Figure 02: Préparation du benzoate d'éthyle
De plus, ce composé est presque insoluble dans l'eau mais se dissout dans des solvants organiques. En raison de son odeur douce, ce composé est utilisé comme composant dans les parfums et comme faveur des fruits artificiels. La méthode de préparation la plus courante de benzoate d'éthyle est l'estérification acide de l'acide benzoïque avec de l'éthanol en présence d'acide sulfurique comme catalyseur.
Quelle est la différence entre l'acide benzoïque et le benzoate d'éthyle?
L'acide benzoïque est un acide carboxylique avec la formule chimique C7H6O2 tandis que l'éthyle benzoate est un ester aromatique avec la formule chimique C9HdixO2. La principale différence entre l'acide benzoïque et le benzoate d'éthyle est que l'acide benzoïque contient un anneau de benzène attaché à un groupe d'acide carboxylique, tandis que le benzoate d'éthyle contient un anneau de benzène attaché à un groupe d'ester.
De plus, nous pouvons également identifier une différence entre l'acide benzoïque et le benzoate d'éthyle en fonction de leurs propriétés physiques. L'acide benzoïque se produit comme un solide cristallin incolore, tandis que le benzoate d'éthyle se produit comme un liquide incolore. De plus, si l'on considère l'odeur de ces composés, l'acide benzoïque a une odeur faible et agréable tandis que le benzoate d'éthyle a une odeur douce et hivernale. En outre, l'acide benzoïque est mal soluble dans l'eau, mais le benzoate d'éthyle est presque insoluble dans l'eau, et il est soluble dans la plupart des solvants organiques.
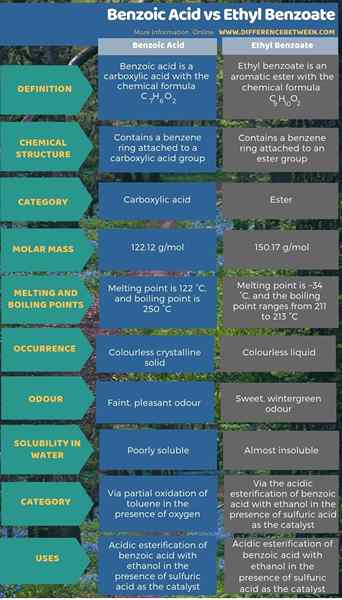
Résumé - Acide benzoïque vs benzoate d'éthyle
L'acide benzoïque est un acide carboxylique qui a la formule chimique C7H6O2 tandis que l'éthyle benzoate est un ester aromatique qui a la formule chimique C9HdixO2. Surtout, la principale différence entre l'acide benzoïque et le benzoate d'éthyle est que l'acide benzoïque contient un anneau de benzène attaché avec un groupe d'acide carboxylique, tandis que le benzoate d'éthyle contient un anneau de benzène attaché avec un groupe d'ester.
Référence:
1. "Acide benzoique.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine, disponible ici.
Image gracieuseté:
1. «Benzoesäure» par Neurotiker - Propre travaux (domaine public) via Commons Wikimedia
2. «Estérification d'éthyle du benzoate» par Minihaa - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


