Différence entre l'anisole et l'éther diéthylique
Le différence clé entre l'anisole et l'éther diéthylique est que L'anisole contient un groupe méthyle et un groupe phényle attaché au même atome d'oxygène, tandis que l'éther diéthylique contient deux groupes éthyliques attachés au même atome d'oxygène.
L'anisole et l'éther diéthylique sont des composés organiques. Ce sont des composés d'éther qui contiennent un atome d'oxygène central avec deux groupes aryle ou alkyle attachés. Ils ont différentes structures chimiques en fonction des types de groupes alkyle ou aryle attachés à l'atome d'oxygène.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce qu'anisole
3. Qu'est-ce que l'éther diéthylique
4. Comparaison côte à côte - Anisole vs éther diéthylique sous forme tabulaire
5. Résumé
Qu'est-ce qu'anisole?
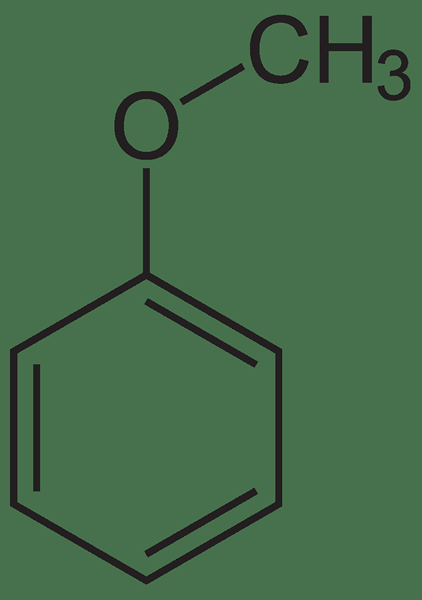
L'anisole est un composé organique ayant la formule chimique ch3OC6H5. Il s'agit d'un composé d'éther ayant un groupe méthyle et un groupe phényle attaché au même atome d'oxygène central. Il se produit comme un liquide incolore et a une odeur qui ressemble à l'odeur d'anis. Nous pouvons observer la présence de ce composé dans de nombreux parfums naturels et artificiels. C'est principalement un composé synthétique que nous pouvons utiliser pour la synthèse d'autres composés organiques comme précurseur. L'anisole peut être produit par méthylation du phénoxyde de sodium en présence de diméthyl sulfate ou de chlorure de méthyle.

Figure 01: Structure de l'anisole
L'anisole peut subir des réactions de substitution aromatique électrophile. Le groupe méthoxy du composé est un groupe de mise en scène ortho / para. Ce groupe de méthoxy a un impact élevé sur le nuage d'électrons de la structure de l'anneau attachée à l'atome d'oxygène. De plus, l'anisole est également capable de subir des réactions électrophiles. Par exemple, l'anisole réagit avec l'anhydride acétique, formant la 4-méthoxyacétophénone. La liaison éther de ce composé est très stable, mais le groupe méthyle est facilement remplacé par l'acide chlorhydrique. L'anisole est généralement classé comme un composé non toxique, mais c'est un liquide inflammable.
Qu'est-ce que l'éther diéthylique?
L'éther diéthylique est un composé organique ayant la formule chimique C2H5OC2H5. C'est un éther ayant deux groupes éthyliques attachés au même atome d'oxygène central. C'est un liquide incolore qui est très volatil et inflammable. De plus, il a une odeur de rhum et douce. Ce liquide est très utile comme solvant, anesthésique général, un médicament récréatif dû à sa non-toxicité, etc.
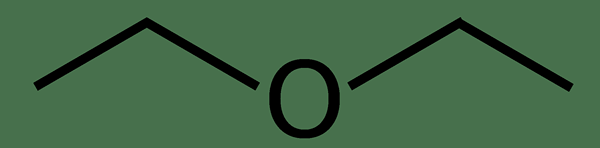
Figure 02: Structure générale de l'éther diéthylique
L'éther diéthylique est un isomère de groupe fonctionnel du butanol. Cela signifie que l'éther diéthylique et le butanol ont la même formule chimique, mais l'éther diéthylique a un groupe fonctionnel d'éther tandis que le butanol a un groupe fonctionnel de l'alcool.
Lorsque l'on considère la production d'éther diéthylique, elle est principalement formée comme un sous-produit d'hydratation de l'éthylène pendant la production d'éthanol. De plus, nous pouvons préparer de l'éther diéthylique via la synthèse de l'éther acide. Dans ce processus, nous devons mélanger l'éthanol avec de l'acide sulfurique fortement acide.
Il existe de nombreuses utilisations de l'éther diéthylique. Par exemple, il est important principalement en tant que solvant dans les laboratoires, comme un carburant ou un liquide de départ, comme anesthésie générale, en tant que composante des formulations pharmaceutiques, etc. Cependant, malgré les nombreuses utilisations de ce composé, elle est extrêmement volatile et inflammable. Ce liquide est également sensible à la lumière et à l'air; Il a tendance à former des peroxydes explosifs sur l'explosion à la lumière et à l'air.
Quelle est la différence entre l'anisole et l'éther diéthylique?
La principale différence entre l'anisole et l'éther diéthylique est que l'anisole contient un groupe méthyle et un groupe phényle attaché au même atome d'oxygène, tandis que dans l'éther diéthylique, il y a deux groupes d'éthyle attachés au même atome d'oxygène. Une autre différence entre l'anisole et l'éther diéthylique est que l'anisole est modérément inflammable, tandis que l'éther diéthylique est extrêmement inflammable.
Le tableau suivant résume les différences entre l'anisole et l'éther diéthylique.

Résumé - Anisole vs éther diéthylique
L'anisole et l'éther diéthylique sont des composés organiques. La principale différence entre l'anisole et l'éther diéthylique est que l'anisole contient un groupe méthyle et un groupe phényle attaché au même atome d'oxygène, tandis que dans l'éther diéthylique, il y a deux groupes d'éthyle attachés au même atome d'oxygène.
Référence:
1. Helmenstine, Anne Marie, «Définition de l'éther en chimie."Thoughtco, février. 11, 2020, disponible ici.
Image gracieuseté:
1. «Anisol» par Neurotiker - Propre travaux (domaine public) via Commons Wikimedia
2. «Structure chimique de l'éther diéthylique» par Wolfmankurd à l'anglais Wikipedia (CC BY-SA 3.0) via Commons Wikimedia


