Différence entre l'aniline et l'acétanilide
Différence clé - Aniline vs acétanilide
L'aniline et l'acétanilide sont deux dérivés de benzène avec deux groupes fonctionnels différents. L'aniline est une amine aromatique (avec -nh2 groupe), et l'acétanilide est un amide aromatique (avec -conh- groupe). La différence dans leur groupe fonctionnel conduit à d'autres variations subtiles des propriétés physiques et chimiques entre ces deux composés. Ils sont tous deux utilisés dans de nombreuses applications industrielles, mais dans divers domaines à des fins différentes. Le différence clé est-ce, En termes de basicité, l'acétanilide est beaucoup plus faible que l'aniline.
Qu'est-ce que Aniline?
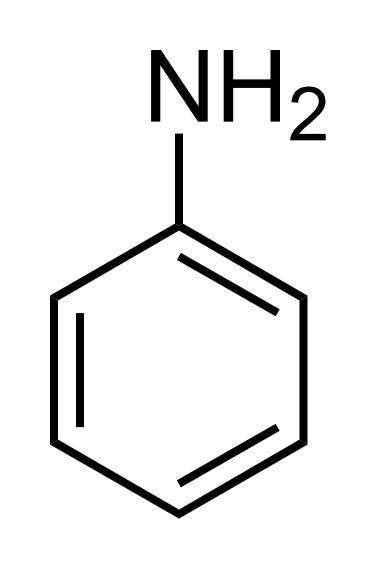
L'aniline est un dérivé benzène avec la formule chimique de C6H5NH2. C'est une amine aromatique également connue sous le nom aminobenzène ou phénylamine. L'aniline est un incolore à brun liquide avec une caractéristique odeur âcre. C'est un inflammable, légèrement soluble dans l'eau et c'est huileux. Son point de fusion et son point d'ébullition sont -6 0C et 1840C respectivement. Sa densité est supérieure à celle de l'eau, et la vapeur est plus lourde que l'air. L'aniline est considérée comme un produit chimique toxique et provoque des effets nocifs par l'absorption et l'inhalation cutanées. Il produit des oxydes d'azote toxiques pendant la combustion.

Qu'est-ce que Acétanilide?
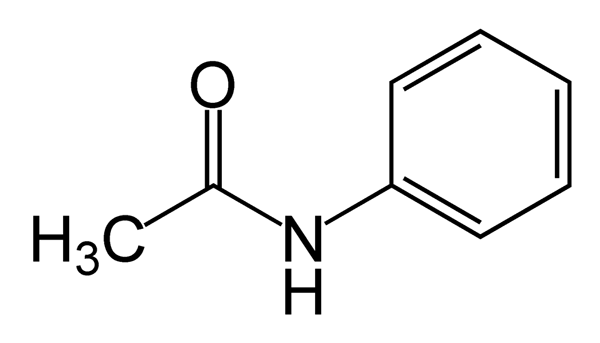
L'acétanilide est un amide aromatique avec la formule moléculaire C6H5NH (Coch3). C'est un inodore, Solide de flocon blanc à gris ou un poudre cristalline à température ambiante. L'acétanilide est soluble dans quelques solvants, notamment l'eau chaude, l'alcool, l'éther, le chloroforme, l'acétone, le glycérol et le benzène. Son point de fusion et son point d'ébullition sont 114 0C et 304 0C respectivement. Il peut subir une auto-ingnition à 545 0C, mais stable dans la plupart des autres conditions.
L'acétanilide est utilisé dans plusieurs industries à différentes fins; Par exemple, il est principalement utilisé comme intermédiaire dans la synthèse des produits pharmaceutiques et des colorants, comme additif dans le peroxyde d'hydrogène, les vernis et l'ester de cellulose. Il est également utilisé comme plastifiant dans l'industrie du polymère et comme accélérateur dans l'industrie du caoutchouc.
Quelle est la différence entre l'aniline et l'acétanilide?
Structure:
Aniline: L'aniline est une amine aromatique; a -nh2 le groupe est attaché à l'anneau de benzène.
Acétanilide: L'acétanilide est un amide aromatique avec un -nh-co-ch3 groupe attaché à l'anneau de benzène.
Les usages:
Aniline: Aniline a plusieurs applications industrielles. Il est utilisé pour préparer d'autres substances chimiques telles que les produits chimiques photographiques et agricoles, les polymères et l'industrie des colorants et l'industrie du caoutchouc. De plus, il est également utilisé comme solvant et composé d'antiknock pour l'essence. Il est également utilisé comme précurseur dans la fabrication de la pénicilline.
Acétanilide: L'acétanilide est principalement utilisé comme inhibiteur des peroxydes et comme stabilisateur pour les vernis à ester de cellulose. Il est également utilisé comme intermédiaire pour la synthèse des accélérateurs en caoutchouc, des colorants et des colorants intermédiaires et camphre. De plus, il est utilisé comme précurseur de la synthèse de la pénicilline et d'autres produits pharmaceutiques, y compris les analgésiques.
Basicité:
Aniline: L'aniline est une base faible qui réagit avec des acides forts produisant de l'ion anilinium (c6H5-NH3+). Il a une base beaucoup plus faible par rapport aux amines aliphatiques en raison de l'effet de retrait de l'électron sur l'anneau de benzène. En dépit d'être une base faible, l'aniline peut précipiter le zinc, l'aluminium et les sels ferriques. De plus, il expulse l'ammoniac des sels d'ammonium lors du chauffage.
Acétanilide: L'acétanilide est un amide et les amides sont des bases très faibles; Ils sont encore moins basiques que l'eau. Cela est dû au groupe carbonyle (c = o) dans les amides; C = O est un dipôle fort que le dipôle N-C. Par conséquent, la capacité du groupe N-C à agir en tant qu'accepteur de la liaison H (comme base) est limitée en présence d'un dipôle C = O.
Image gracieuseté:
1. Aniline par Calvero. (Selfmade avec ChemDraw.) [Domaine public], via Wikimedia Commons
2. Acétanilide par rune.Welsh at English Wikipedia [Domaine public, GFDL, CC-BY-SA-3.0 ou cc par 2.5], via Wikimedia Commons


