Différence entre l'ammoniac et l'azote ammoniacal
Le différence clé entre l'ammoniac et l'azote ammoniacal est que le L'ammoniac est un composé inorganique ayant la formule chimique NH3 tandis que l'azote ammoniacal est une mesure de la quantité d'ammoniac dans un échantillon.
L'ammoniac est un composé gazeux avec une odeur caractéristique et piquante. Bien qu'il soit utile à plusieurs reprises, c'est également un composé toxique. C'est un polluant toxique courant dans les déchets tels que les eaux usées, le fumier, etc. Nous utilisons de l'azote ammoniacal pour mesurer la quantité de ce composé toxique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'ammoniac
3. Qu'est-ce que l'azote ammoniacal
4. Comparaison côte à côte - ammoniac vs azote ammoniacal sous forme tabulaire
5. Résumé
Qu'est-ce que l'ammoniac?
L'ammoniac est un composé inorganique ayant la formule chimique NH3. Par conséquent, c'est un composé gazeux avec une odeur caractéristique et piquante. Le nom IUPAC de ce composé est Azane. La masse molaire est de 17 g / mol et le point d'ébullition est -33.34 ° C. Une molécule d'ammoniac a un atome d'azote lié à trois autres atomes d'hydrogène via des liaisons covalentes. De plus, cette molécule a une forme pyramidale trigonale, et c'est un gaz incolore qui est plus léger que l'air normal.
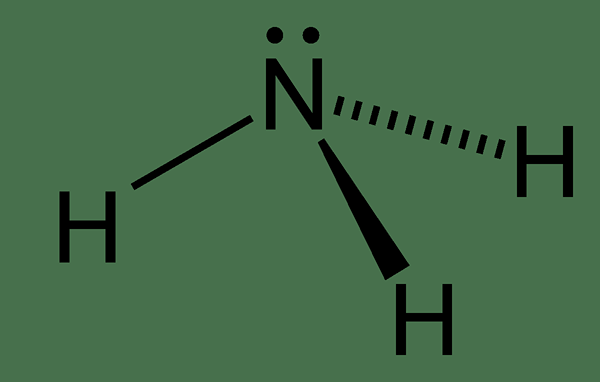
Figure 01: Structure chimique de l'ammoniac
Il existe des liaisons hydrogène entre les molécules d'ammoniac. Par conséquent, nous pouvons facilement liquéfier ce gaz. Ce composé est courant dans les déchets azotés des organismes aquatiques. De plus, il contribue aux besoins nutritionnels des organismes terrestres; En fournissant des besoins en nourriture et en engrais. Cependant, dans sa forme concentrée, l'ammoniac est dangereux et caustique.
Qu'est-ce que l'azote ammoniacal?
L'azote ammoniacal est une mesure de la quantité d'ammoniac dans un échantillon. Ici, nous déterminons l'effet toxique de l'ammoniac dans les lixiviats de décharge, les déchets tels que le fumier, etc. Par conséquent, nous mesurons la santé des plans d'eau naturels car l'ammoniac peut nous empoisonner directement à des concentrations élevées. Nous désignons l'azote ammoniacal comme NH3-N.

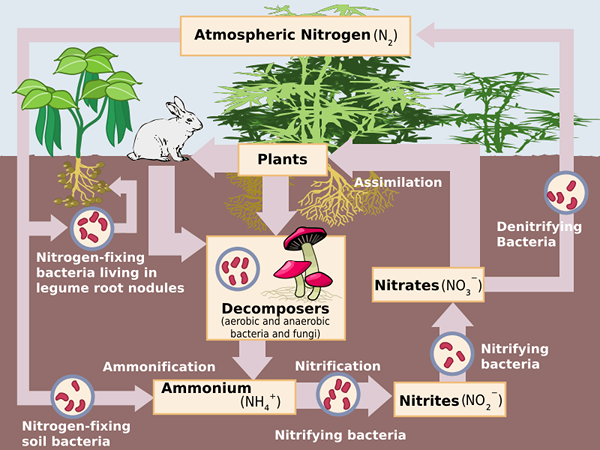
Figure 02: Le cycle d'azote montre les formes d'azote ammoniacales dans l'environnement
L'unité de mesure est Mg / L. Dans cette mesure, nous mesurons toutes les formes d'ammoniac; ammoniac (NH3), ammonium (NH4+), azote gazeux (n2), nitrates (non3-), nitrites (non2-), azote organique comme les protéines, l'ADN, etc.
Quelle est la différence entre l'ammoniac et l'azote ammoniacal?
L'ammoniac est un composé inorganique ayant la formule chimique NH3. Il est utile à faible concentration et toxique à des concentrations élevées. L'azote ammoniacal est une mesure de la quantité d'ammoniac dans un échantillon. Il mesure la quantité d'ammoniac à ses niveaux toxiques. De plus, il fait référence à toutes les formes d'ammoniac telles que l'ammoniac (NH3), ammonium (NH4+), azote gazeux (n2), nitrates (non3-), nitrites (non2-), azote organique comme les protéines, l'ADN, etc.

Résumé - Ammoniac vs azote ammoniacal
L'ammoniac et l'azote ammoniacal sont deux termes connexes. La différence entre l'ammoniac et l'azote ammoniacal est que l'ammoniac est un composé inorganique ayant la formule chimique NH3 tandis que l'azote ammoniaque est une mesure de la quantité d'ammoniac dans un échantillon.
Référence:
1. "Ammoniac.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine. Disponible ici
2. «Azote ammoniacal.»Wikipedia, Wikimedia Foundation, 10 juillet 2018. Disponible ici
Image gracieuseté:
1.'Ammoniac-2D'By Radio89 - Propre travaux, (CC BY-SA 3.0) via Commons Wikimedia
2.'Cycle d'azote' par Burkhard (CC BY-SA 3.0) via Commons Wikimedia


