Différence entre l'alcalinité et la basicité
Différence clé - Alcalinité vs. Basicité
Les deux termes «alcalinité» et «bascicité» sont assez déroutants. La plupart des gens savent qu'il y a une différence entre ces deux paramètres, mais seuls quelques-uns sont capables de le définir correctement. Le différence clé entre ces deux termes est mieux expliqué dans leurs définitions. La basicité est une mesure qui dépend directement de l'échelle de pH et L'alcalinité est la quantité d'acide nécessaire pour abaisser le pH dans une valeur acide significative; il est également connu comme le Tamponner la capacité d'un plan d'eau. En d'autres termes, la valeur de pH des solutions de base varie de 7 à 14; où les solutions avec des valeurs de pH élevées sont plus basiques. Tous deux ont plusieurs définitions, mais l'idée générale est similaire.
Qu'est-ce que l'alcalinité?
L'alcalinité est L'un des paramètres les plus importants des corps aquatiques, et il est très essentiel aux organismes aquatiques. L'alcalinité mesure la capacité des plans d'eau à neutraliser les acides et les bases. En d'autres termes, c'est la capacité tampon d'un plan d'eau à maintenir la valeur du pH à une valeur assez stable. Eau contenant des bicarbonates (HCO3-), Carbonates (CO32-) et les hydroxydes (oh-) est un bon tampon; ils peuvent se combiner avec H+ ions dans l'eau pour élever le pH (devient plus basique) de l'eau. Lorsque l'alcalinité est trop faible (la capacité tampon est faible), tout acide ajouté au corps d'eau abaisse son pH à une valeur acide plus élevée.
 Qu'est-ce que la basicité?
Qu'est-ce que la basicité?
La basicité est une propriété de bases, mesurée à l'échelle du pH. Les bases sont les composés contenant du pH supérieur à 7; de pH = 8 (moins de base) à pH = 18 (plus basique). La basicité d'un composé peut être définie de trois manières différentes. Selon la théorie d'Arrhenius, les bases sont les substances qui se dissocient dans un milieu aqueux produisant OH- ions. Dans la théorie de Bronsted-Lowry, les accepteurs de protons sont appelés bases. Selon Lewis Theory, un donateur de paire d'électrons est appelé une base. La basicité est l'ionisation de force pour produire OH- ions, capacité à accepter les protons ou la capacité de donner des électrons.

Thomas Martine Lowry - théorie de la lowry brronsted
Quelle est la différence entre l'alcalinité et la basicité?
Définition de l'alcalinité et de la basicité:
Alcalinité: Plusieurs définitions sont là.
L'alcalinité est la capacité de neutralisation acide des solutés dans un échantillon d'eau mesuré en milliéquivalisants par litre.
La somme des espèces chimiques carbonatées et non carbonates titrables dans un échantillon d'eau filtré.
La capacité de l'eau à neutraliser une solution acide.
La capacité tampon de l'eau à maintenir un pH assez stable, sans modifier sa valeur de pH, lorsque l'acide est ajouté.
Basicité: Trois théories sont utilisées pour définir l'acidité et la basicité.
Arrenhius: Les bases sont les espèces qui ionisent pour produire OH- dans l'eau. La basicité augmente en ionisant plus, donnant oh- dans l'eau.
Bronsted-Lowry: Proton (h+) Les accepteurs sont appelés bases.
Lewis: Les donateurs de paires d'électrons sont appelés bases.
Facteurs affectant l'alcalinité et la basicité:
Alcalinité: L'alcalinité ne dépend pas de la valeur de pH; Les corps d'eau peuvent avoir une valeur de pH inférieure (très acide) ou supérieure (de base) avec une valeur plus élevée pour l'alcalinité. L'alcalinité est déterminée par plusieurs facteurs tels que Roches, sol, sels et certaines activités industrielles (les eaux usées contenant du savon et des détergents sont alcalines) par l'homme. Par exemple, les zones où le calcaire (Caco3) est considérablement disponible peut avoir plus d'eau alcaline.
Basicité: Les facteurs affectant la basicité d'un composé varient en fonction de la définition de la basicité. Par exemple, la disponibilité des paires d'électrons d'une base dépend de trois facteurs.
Électronégativité: Ch3-> nh2-> ho-> f-
Lorsque vous envisagez les atomes dans la même rangée dans le tableau périodique, l'atome le plus électronégatif a la basicité plus élevée.
Taille: F-> cl-> br-> i-
Lorsque vous envisagez une ligne du tableau périodique, plus l'atome a moins de densité d'électrons et il est moins basique.
Résonance: Ro-> rco2-
Les molécules ayant plus de structures de résonance sont moins basiques, car moins la disponibilité des électrons qu'une charge négative localisée.
Image gracieuseté:
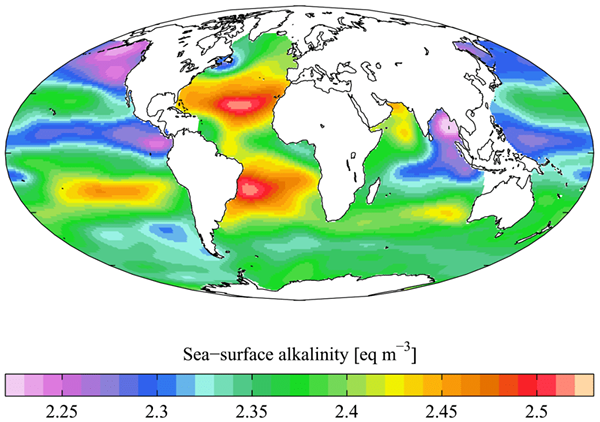
1. «WOA05 Glodap Pd alk Ayool» par Plumbago - Propre travaux. [CC BY-SA 3.0] via les communes
2. «Thomas Martin Lowry2» par Anonymous - nécrologie par le Faraday Soc. (1936). [Domaine public] via les biens communs


