Différence entre l'aldéhyde et le formaldéhyde
Le différence clé entre l'aldéhyde et le formaldéhyde est que le L'aldéhyde contient un groupe R attaché à un groupe -cho mais le formaldéhyde n'a pas de groupe R comme autres aldéhydes.
La principale différence entre l'aldéhyde et le formaldéhyde réside sur la structure chimique de ces composés. Ce sont des composés organiques contenant des atomes de carbone, d'hydrogène et d'oxygène. De plus, ils possèdent un groupe fonctionnel carbonyle, qui est un groupe -cho. Comme son nom l'indique, le formaldéhyde est également une forme d'aldéhyde.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'aldéhyde
3. Qu'est-ce que le formaldéhyde
4. Comparaison côte à côte - Aldéhyde vs formaldéhyde sous forme tabulaire
5. Résumé
Qu'est-ce que l'aldéhyde?
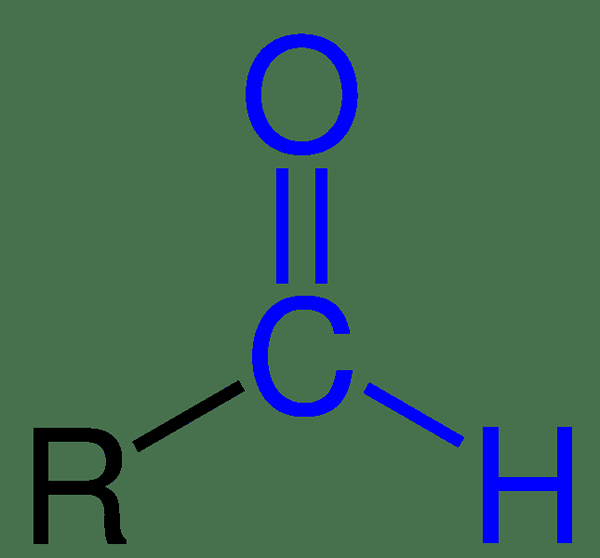
Les aldéhydes ont un groupe carbonyle. Ce groupe carbonyle se lie à un autre carbone d'un côté, et de l'autre extrémité, il se connecte à un atome d'hydrogène. De plus, dans un groupe carbonyle, l'atome de carbone a essentiellement une double liaison à l'oxygène. Par conséquent, nous pouvons caractériser les aldéhydes avec le groupe -cho, dans lequel l'atome d'oxygène a une double liaison avec l'atome de carbone.
Dans la nomenclature des aldéhydes, selon le système IUPAC, nous utilisons le terme «Al» pour désigner un aldéhyde. Pour les aldéhydes aliphatiques, le «E» de l'alcane correspondant est remplacé par «Al». Par exemple, nous pouvons nommer le composé ch3Cho comme l'éthanol et ch3Ch2Cho comme propanol. Les aldéhydes avec des systèmes d'anneau, où le groupe aldéhyde s'attache directement à l'anneau, nous pouvons utiliser le terme «carbaldehyde» comme suffixe pour les nommer. Cependant, C6H6CHO est communément appelé benzaldéhyde plutôt que d'utiliser du benzenecaldéhyde.

Figure 01: Structure chimique de l'aldéhyde
De plus, nous pouvons synthétiser ces composés organiques par diverses méthodes. Une méthode est via des alcools oxydants primaires. De plus, nous pouvons les synthétiser en réduisant les esters, les nitriles et les chlorures d'acyle.
Structure
L'atome de carbonyle carboné a SP2 hybridation. Ainsi, les aldéhydes ont un arrangement plan trigonal autour de l'atome de carbone carbonyle. Un groupe carbonyle est un groupe polaire; Ainsi, ces molécules ont des points d'ébullition plus élevés par rapport aux hydrocarbures ayant le même poids.
Cependant, ces composés ne peuvent pas faire de liaisons hydrogène plus fortes comme des alcools, ce qui entraîne des points d'ébullition plus bas que les alcools correspondants. En raison de la capacité de formation de liaison hydrogène, les aldéhydes de faible poids moléculaire sont solubles dans l'eau. Quoi qu'il en soit, lorsque le poids moléculaire augmente, ils deviennent hydrophobes.
L'atome de carbonyle carboné a une charge positive partielle; Par conséquent, il peut agir comme un électrophile. Par conséquent, ces molécules sont facilement soumises à des réactions de substitution nucléophile. Les hydrogènes attachés au carbone à côté du groupe carbonyle ont une nature acide, qui explique diverses réactions d'aldéhydes.
Qu'est-ce que le formaldéhyde?
L'aldéhyde le plus simple est le formaldéhyde. Cependant, la structure de ce composé s'écarte de la formule générale d'un aldéhyde en ayant un atome d'hydrogène au lieu d'un groupe R. Par conséquent, le formaldéhyde a la formule générale de H-cho.
De plus, le formaldéhyde est un gaz incolore à température ambiante, qui est également inflammable. Son nom IUPAC est méthanal, avec le suffixe -al, qui montre qu'il s'agit d'un aldéhyde. Ce composé a une forte odeur, et il est très toxique pour le corps humain. Cependant, il se forme naturellement dans le corps en tant que sous-produit des voies du métabolisme. Par exemple, le méthanol se décompose dans le foie produisant du formaldéhyde. Quoi qu'il en soit, il ne s'accumule pas à l'intérieur car il se transforme rapidement en acide formique.
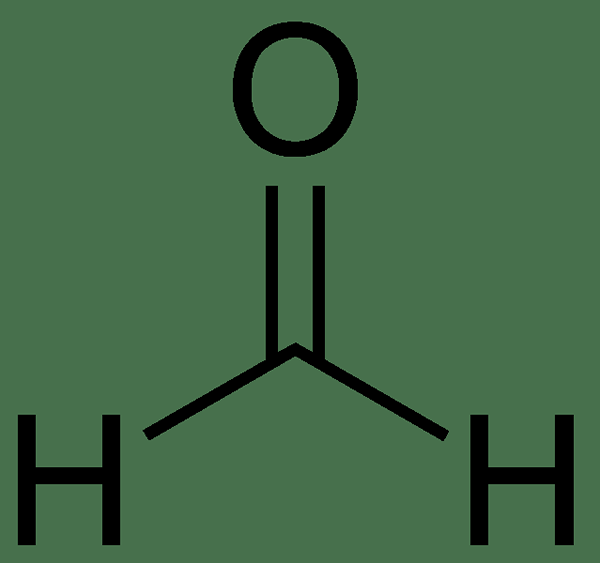
Figure 02: Structure chimique du formaldéhyde
De plus, le formaldéhyde se forme naturellement dans l'atmosphère lorsque l'oxygène, le méthane et d'autres hydrocarbures réagissent sous la lumière du soleil. Le formaldéhyde a tellement d'utilisations comme un produit chimique majeur dans les industries. Il est utile de produire des désinfectants, des engrais, des automobiles, du papier, des cosmétiques, une conservation du bois, etc.
Quelle est la différence entre l'aldéhyde et le formaldéhyde?
Le formaldéhyde est la forme la plus simple d'aldéhydes. Mais, la principale différence entre l'aldéhyde et le formaldéhyde est que les aldéhydes contiennent un groupe R attaché à un groupe -cho mais le formaldéhyde n'a pas de groupe R comme d'autres aldéhydes. Par conséquent, la formule chimique générale des aldéhydes est r-cho, mais pour le formaldéhyde, c'est H-cho.
Comme autre différence importante entre l'aldéhyde et le formaldéhyde, nous pouvons prendre la phase de matière dont ils existent à la température et à la pression standard; Les aldéhydes peuvent se produire dans des phases gazeuses ou liquides tandis que le formaldéhyde se produit dans la phase gazeuse. De plus, une différence facilement observable entre l'aldéhyde et le formaldéhyde est leur odeur. C'est-à-dire; La plupart des aldéhydes ont une odeur agréable mais le formaldéhyde a une odeur piquante.

Résumé - Aldéhyde vs formaldéhyde
Les aldéhydes sont des composés organiques. Le formaldéhyde est l'aldéhyde le plus simple. Par conséquent, la principale différence entre l'aldéhyde et le formaldéhyde est que l'aldéhyde contient un groupe R attaché à un groupe -cho mais le formaldéhyde n'a pas de groupe R comme autres aldéhydes.
Référence:
1. Brown, William H., et Jerry March. "Aldéhyde.»Encyclopædia Britannica, Encyclopædia Britannica, Inc., 31 décembre. 2015. Disponible ici
2. "Formaldéhyde.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine. Disponible ici
Image gracieuseté:
1.«Funktionellegruppen Aldehyde» par Mache (Talk) - Propre travaux, (domaine public) via Commons Wikimedia
2."Formaldéhyde 200" par Emeldir (Talk) - Propre travaux, (domaine public) via Commons Wikimedia


