Différence entre l'acidimétrie et l'alcalimétrie

Le différence clé entre l'acidimétrie et l'alcalimétrie est que L'acidimétrie est la mesure de la force des acides, tandis que l'alcalimétrie est la mesure de la résistance des composés alcalins.
L'acidimétrie et l'alcalimétrie sont deux types de techniques d'analyse volumétriques où la réaction fondamentale de l'analyse est un type de réaction de neutralisation.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acidimétrie
3. Qu'est-ce que l'alcalimétrie
4. Comparaison côte à côte - acidimétrie vs alcalimétrie sous forme tabulaire
5. Résumé
Qu'est-ce que l'acidimétrie?
L'acidimétrie est une technique analytique spécialisée utilisée pour déterminer la force d'un acide. Nous pouvons utiliser cette technique dans un titrage acide-base pour déterminer la concentration d'une substance de base ou alcaline. Cependant, nous devons utiliser une solution acide standard pour cette détermination. Il implique une réaction de neutralisation. Ce type de techniques de réaction est utile dans les processus d'analyse volumétrique.
Dans l'acidimétrie, l'acide standard que nous utilisons devrait avoir une concentration connue; Sinon, nous ne pouvons pas déterminer la concentration de la base. Étant donné que presque tous les acides et bases que nous utilisons généralement dans un processus de titration acide-base sont incolores, nous devons utiliser un indicateur qui aide à déterminer le point final du titrage.
Après avoir effectué le titrage acide-base, nous pouvons utiliser la relation suivante pour la détermination de la concentration de la base.
C1V1= C2V2
Lorsque C1 est la concentration de l'acide standard, le v1 est le volume de l'acide réagi avec l'échantillon d'analyte, C2 est la concentration inconnue de la base (que nous allons découvrir), et V2 est le volume de l'échantillon d'analyte (base).
Qu'est-ce que l'alcalimétrie?
L'alcalimétrie est une technique analytique spéciale que nous pouvons utiliser pour déterminer la résistance d'une base ou d'un composé alcalin. Dans cette technique, nous pouvons déterminer la concentration d'une substance basique ou alcaline si nous utilisons la réaction dans un processus de titrage acide-base. Il implique une réaction de neutralisation.

Figure 01: L'utilisation d'un indicateur de phénolphtaleine pour déterminer le point final d'un titrage acide-base donne une couleur rose
Dans l'alcalimétrie, la base standard que nous utilisons devrait avoir une concentration connue; Sinon, nous ne pouvons pas déterminer la concentration de l'acide. Étant donné que presque tous les acides et bases que nous utilisons généralement dans un processus de titration acide-base sont incolores, nous devons utiliser un indicateur qui aide à déterminer le point final du titrage.
Quelle est la différence entre l'acidimétrie et l'alcalimétrie?
En chimie analytique, il est très important de connaître la force des acides et des bases que nous utilisons dans une analyse. L'acidimétrie et l'alcalimétrie sont utiles pour déterminer ces forces. La principale différence entre l'acidimétrie et l'alcalimétrie est que l'acidimétrie est la mesure de la force des acides, tandis que l'alcalimétrie est la mesure de la résistance des composés alcalins. De plus, l'acidimétrie mesure la tendance d'un acide à se dissocier, formant des protons et un anion, tandis que l'alcalimétrie mesure la tendance d'une base à accepter les protons d'une autre espèce chimique.
De plus, l'infographie suivante résume la différence entre l'acidimétrie et l'alcalimétrie sous forme tabulaire.
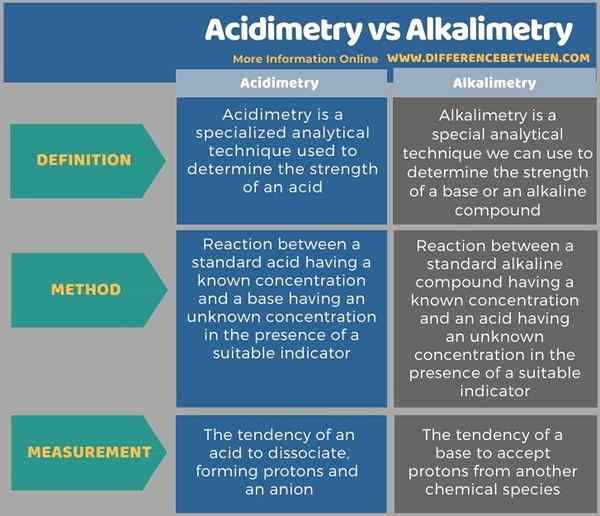
Résumé - acidimétrie vs alcalimétrie
En chimie analytique, il est très important de connaître la force des acides et des bases que nous utilisons dans une analyse. L'acidimétrie et l'alcalimétrie sont deux types de techniques d'analyse volumétriques où la réaction fondamentale de l'analyse est une sorte de réaction de neutralisation. La principale différence entre l'acidimétrie et l'alcalimétrie est que l'acidimétrie est la mesure de la force des acides, tandis que l'alcalimétrie est la mesure de la résistance des composés alcalins.
Référence:
1. «Force de base." Chemistry LibreTexts, LibreTexts, 24 août. 2020, disponible ici.
Image gracieuseté:
1. «Phenolphthalein in Flask» par 384 - propre travail (CC BY-SA 4.0) via Commons Wikimedia


