Quelle est la différence entre l'acide citrique et l'acide acétique

Le différence clé entre l'acide citrique et l'acétique L'acide est que l'acide citrique a trois groupes d'acide carboxylique, tandis que l'acide acétique a un groupe d'acide carboxylique.
L'acide citrique et l'acide acétique sont des composés d'acide carboxylique organiques ayant le groupe fonctionnel de l'acide carboxylique (-COOH). Cependant, ils diffèrent les uns des autres en fonction du nombre de groupes d'acide carboxylique dans ces molécules.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acide citrique
3. Qu'est-ce que l'acide acétique
4. Acide citrique vs acide acétique sous forme tabulaire
5. Résumé - acide citrique vs acide acétique
Qu'est-ce que l'acide citrique?
L'acide citrique est un composé organique ayant la formule chimique HOC (COOH). C'est un acide organique faible incolore et se produit naturellement chez les agrumes. En termes biochimiques, l'acide citrique est un intermédiaire dans le cycle de l'acide citrique pendant le métabolisme de tous les organismes aérobies. En règle générale, environ 2 millions de tonnes d'acide citrique sont fabriquées chaque année. Cette substance est largement importante en tant qu'acidificateur et en tant qu'agent arôme. C'est également important en tant qu'agent chélatant.
La masse molaire de ce composé est de 192 g / mol dans son état anhydre. Lorsqu'il est isolé, l'acide citrique apparaît comme un solide blanc qui est inodore. La densité de la forme anhydre est d'environ 1.66 g / cm3. Son point de fusion est de 156 degrés Celsius, et son point d'ébullition est de 310 degrés Celsius. Cependant, il commence à se décomposer à environ 175 degrés Celsius. De plus, l'acide citrique est soluble dans l'acétone, l'alcool, l'éther, l'acétate d'éthyle, mais il est insoluble dans le toluène. La structure cristalline de l'acide citrique solide est monoclinique.

Figure 01: Fruits d'agrumes
En règle générale, cet acide peut être trouvé dans de nombreux fruits et légumes différents, mais principalement chez les agrumes. Par exemple, le citron et la chaux ont une teneur très élevée d'acide citrique. Lors de la préparation industrielle de cette substance, il a d'abord été fait en traitant le jus avec de la chaux hydratée (hydroxyde de calcium) pour obtenir le précipité du citrate de calcium, qui est ensuite isolé et converti en acide citrique à l'aide d'acide sulfurique. Cependant, dans les industries modernes, l'acide citrique est préparé par des méthodes de fermentation fongique.
Qu'est-ce que l'acide acétique?
L'acide acétique est un composé organique ayant la formule chimique ch3COOH. Il est également connu sous le nom acide éthanoique et se produit comme un liquide acide et incolore ayant une odeur fortement de vinaigre. La masse molaire de ce composé est de 60 g / mol. La densité peut être donnée comme 1.05 g / cm3. Le point de fusion varie de 61 à 62 degrés Celsius, et le point d'ébullition peut aller de 118 à 119 degrés Celsius. Il est miscible avec l'eau.
On peut dire que l'acide acétique est le deuxième acide carboxylique le plus simple car il a un groupe fonctionnel d'acide carboxylique attaché à un atome de carbone. (L'acide carboxylique le plus simple est l'acide formique - HCOOH, le groupe d'acide carboxylique n'est attaché à aucun atome de carbone). L'acide acétique est important dans de nombreuses industries différentes, comme la production d'acétate de cellulose, d'acétate de polyvinyle, de fibres synthétiques, etc. Dans l'industrie alimentaire, ce produit chimique est utile en tant qu'additif alimentaire avec le numéro E 260.
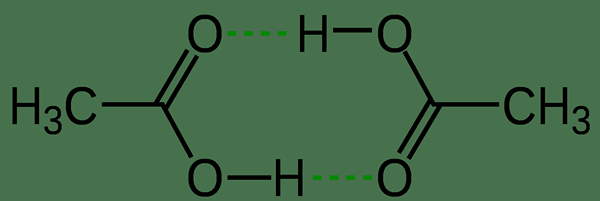
Figure 02: Dimères de l'acide acétique dans la phase de vapeur
Le groupe fonctionnel de l'acide carboxylique dans une molécule d'acide acétique peut subir une ionisation partielle pour former des ions acétate et un cation hydrogène (proton). La libération de ce proton provoque la nature acide de l'acide acétique. Par conséquent, nous pouvons nommer ce produit chimique comme un acide monoprotique faible (ce qui signifie qu'il se dissocie partiellement et donne un proton par molécule). En règle générale, l'acide acétique solide a des chaînes de molécules, et ces molécules sont interconnectées par liaison hydrogène. Dans sa phase de vapeur, nous pouvons détecter les dimères des molécules d'acide acétique. Dans son état liquide, c'est un solvant protéique hydrophile.
Quelle est la différence entre l'acide citrique et l'acide acétique?
L'acide citrique et l'acide acétique sont des composés organiques importants ayant des groupes fonctionnels d'acide carboxylique. Ces deux composés sont différents les uns des autres en fonction du nombre de groupes fonctionnels par molécule et, par conséquent, leurs propriétés chimiques et physiques. La principale différence entre l'acide citrique et l'acide acétique est que l'acide citrique a trois groupes d'acide carboxylique, tandis que l'acide acétique a un groupe d'acide carboxylique.
Résumé - acide citrique vs acide acétique
Le groupe fonctionnel de l'acide carboxylique a la formule chimique -COOH. L'acide citrique et l'acide acétique contiennent ce type de groupe fonctionnel dans leurs molécules. La principale différence entre l'acide citrique et l'acide acétique est que l'acide citrique a trois groupes d'acide carboxylique, tandis que l'acide acétique a un groupe d'acide carboxylique.
Référence:
1. «Acide acétique: informations générales." Gouvernement.ROYAUME-UNI.
Image gracieuseté:
1. «Citrus Fruits» de Scott Bauer, USDA - L'Agence de recherche du Département de l'agriculture des États-Unis, avec l'ID K7226-29 (domaine public) via Commons Wikimedia
2. «Hydrogenbridge V acide acétique V.1 ”par Jü - propre travail (domaine public) via Commons Wikimedia


