Différence entre la tonique et l'osmolarité
Le différence clé entre la tonique et l'osmolarité est que le La tonicicité ne mesure que la concentration de solutés non pénétrants à travers une membrane semi-perméable tandis que L'osmolarité mesure la concentration totale de solutés pénétrants et non pénétrants.
L'osmolarité est la mesure de la pression osmotique d'une solution. En termes plus simples, c'est à peu près la mesure de la quantité de soluté dans la solution. Au contraire, la tonicité fait référence à la concentration relative de particules de soluté à l'intérieur d'une cellule par rapport à la concentration à l'extérieur de la cellule. Ainsi, la tonique et l'osmolarité semblent être des concepts similaires. Cependant, il y a des différences dont nous discuterons dans cet article.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la tonique
3. Qu'est-ce que l'osmolarité
4. Comparaison côte à côte - Tonicité vs osmolarité sous forme tabulaire
5. Résumé
Qu'est-ce que la tonique?
La tonicité est une mesure du gradient de pression osmotique au moyen du potentiel d'eau de deux solutions séparées par une membrane semi-perméable. Ça veut dire; Le terme tonicicité décrit la concentration relative de la solution de solutés I qui détermine la direction et l'étendue de la diffusion. Cette mesure est importante pour déterminer la réponse des cellules immergées dans une solution externe.

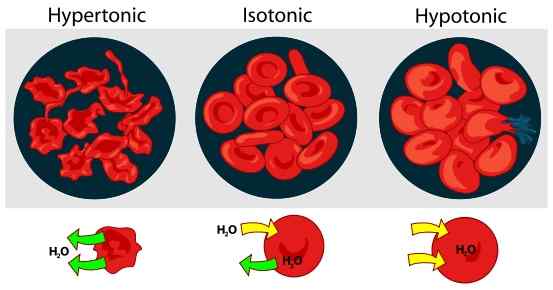
Figure 01: Effet de la tonique sur les globules rouges dans une solution externe
Contrairement à la pression osmotique, la tonicité n'est influencée que par des solutés qui ne peuvent pas traverser la membrane. Les solutés qui peuvent passer librement par la membrane n'ont aucune influence sur la tonique. C'est parce que la concentration de ces solutés restera toujours la même dans les deux côtés de la membrane. Habituellement, nous exprimons la tonicité par rapport à une autre solution. En conséquence, il existe trois types de solutions basées sur la tonique; Solutions hypertoniques, solutions hypotoniques et solutions isotoniques. Les solutions hypertoniques ont une concentration de soluté élevée qu'une autre solution tandis que la solution hypotonique a une concentration de soluté plus faible. Une solution devient isotonique si la concentration d'osmole efficace de cette solution est la même que celle d'une autre solution.
Qu'est-ce que l'osmolarité?
L'osmolarité ou la concentration osmotique est une mesure de la concentration de soluté donnée par l'unité osmole des solutés par litre de solution. Nous pouvons désigner l'unité comme OSM / L. De même, nous pouvons utiliser cette valeur pour mesurer la pression osmotique d'une solution. Ainsi, la tonicité de la solution aussi. L'équation que nous pouvons utiliser pour mesurer ce paramètre est la suivante:
Osmolarité = ∑ψjenjeCje
Ici, ψ est le coefficient osmotique, n est le nombre de particules dans lesquelles une molécule se dissocie, et c est la concentration molaire du soluté. De même, il existe trois types de solutions selon l'osmolarité; isosmotique, hyperosmotique et hypoosmotique.
Quelle est la différence entre la tonicité et l'osmolarité?
Les termes tonicicité et osmolarité sont des concepts liés mais distincts. La raison pour laquelle ils sont liés les uns aux autres est que ces deux termes comparent les concentrations de soluté de deux solutions séparées d'une membrane semi-perméable. Ces termes diffèrent les uns des autres en fonction du type de soluté qu'ils prennent en compte lors de la mesure. Par conséquent, la principale différence entre la tonique et l'osmolarité est que la tonicité ne mesure que la concentration de solutés non pénétrants à travers une membrane semi-perméable tandis que l'osmolarité mesure la concentration totale de solutés pénétrants et non pénétrants.
L'infographie ci-dessous donne des faits supplémentaires sur la différence entre la tonicité et l'osmolarité.

Résumé - Tonicité vs osmolarité
Les termes osmolarité et tonicicité sont interdépendants car ces deux termes comparent les concentrations de soluté dans une solution. Mais, en même temps, les termes sont des concepts chimiques distincts en fonction des types de solutés qu'ils prennent en compte dans leurs mesures. Par conséquent, la principale différence entre la tonique et l'osmolarité est que la tonicité ne mesure que la concentration de solutés non pénétrants à travers une membrane semi-perméable tandis que l'osmolarité mesure la concentration totale de solutés pénétrants et non pénétrants.
Référence:
1. "Tonicité.»Wikipedia, Wikimedia Foundation, 8 février. 2018. Disponible ici
2. «Concentration osmotique.»Wikipedia, Wikimedia Foundation, 15 octobre. 2018. Disponible ici
Image gracieuseté:
1.«Pression osmotique sur le diagramme des cellules sanguines» par LadyOfhats - propre travail (domaine public) via Commons Wikimedia


