Différence entre le fluorure stanneux et le fluorure de sodium

Le différence clé entre le fluorure stanneux et le fluorure de sodium est que le Le fluorure stanneux peut agir contre gingivite, plaque, sensibilité des dents et protéger des cavités tandis que le fluorure de sodium ne protège nos dents que contre les cavités.
Le fluorure stanneux est le nom commercial du composé chimique, Tin (II) fluorure. Il est très courant comme ingrédient dans les liquides de dentifrice et de rince-bouche. Il peut agir contre de nombreuses maladies dentaires. Par conséquent, c'est relativement cher. Le fluorure de sodium est également un ingrédient commun du dentifrice qui peut protéger notre dent contre les cavités, mais il n'a pas une large gamme d'activité comme pour le fluorure stanique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le fluorure stanneux
3. Qu'est-ce que le fluorde de sodium
4. Comparaison côte à côte - fluorure stanneuse vs fluorure de sodium sous forme tabulaire
5. Résumé
Qu'est-ce que le fluorure stanneux?
Le fluorure stanneux est le nom commercial du fluorure d'étain qui a la formule chimique SNF2. La masse molaire de ce composé est de 156.69 g / mol, et il apparaît comme un solide incolore. Le point de fusion de ce composé est de 213 ° C et le point d'ébullition est de 850 ° C. La structure cristalline est monoclinique. Nous pouvons produire ce composé en évaporant une solution SNO dans HF (40%).
En outre, ce composé est un ingrédient important dans un dentifrice car il peut agir contre la gingivite, la plaque, la sensibilité des dents et se protéger des cavités. Par conséquent, il est généralement plus cher que les autres fluorures. De plus, il peut agir comme un agent réducteur. Là, les ions fluorures peuvent être oxydés. De plus, ces molécules SNF2 forment des dimères et des trimères en se combinant entre eux.
Qu'est-ce que le fluorde de sodium?
Le fluorure de sodium est un composé inorganique ayant la formule chimique NAF. C'est un solide incolore qui se dissout facilement dans l'eau. Un autre nom pour ce composé est Florocid. La masse molaire de ce composé est 41.98 g / mol. Le point de fusion est de 993 ° C et le point d'ébullition est de 1 704 ° C. La structure cristalline est cubique.

Figure 01: Le fluorure stanneux et le fluorure de sodium sont des ingrédients importants dans le dentifrice
De plus, nous pouvons produire ce composé via la neutralisation de l'acide HF. Cet acide HF est un sous-produit de la production d'engrais à l'aide de fluorapatite. Nous pouvons utiliser des alcools pour précipiter NAF. C'est un ingrédient important dans les produits pharmaceutiques et le dentifrice. Il peut protéger contre les cavités dans la dent.
Quelle est la différence entre le fluorure stanneux et le fluorde de sodium?
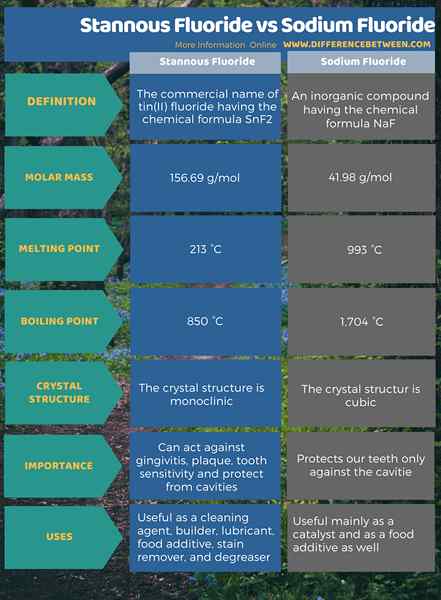
Le fluorure stanneux est le nom commercial du fluorure d'étain (ii) qui a la formule chimique SNF2. La masse molaire de ce composé est de 156.69 g / mol. De plus, son point de fusion et ses points d'ébullition sont respectivement de 213 ° C et 850 ° C. Le fluorure de sodium est un composé inorganique ayant la formule chimique NAF. La masse molaire de ce composé est 41.98 g / mol. De plus, le point de fusion et le point d'ébullition de ce composé sont de 993 ° C et 1 704 ° C. La principale différence entre le fluorure stanneux et le fluorure de sodium est que le fluorure stanneux peut agir contre la gingivite, la plaque, la sensibilité des dents et se protéger des cavités tandis que le fluorure de sodium protège nos dents uniquement contre les cavités.
Résumé - fluorure stanneux vs fluorure de sodium
Le fluorure stanneux et le fluorure de sodium sont des ingrédients importants dans le dentifrice. La différence entre le fluorure stanneuse et le fluorure de sodium est que le fluorure stanneux peut agir contre la gingivite, la plaque, la sensibilité des dents et se protéger des cavités tandis que le fluorure de sodium protège nos dents uniquement contre les cavités.
Référence:
1. «Tin (ii) fluorure.»Wikipedia, Wikimedia Foundation, 8 juillet 2018. Disponible ici
2. "Le fluorure de sodium.»Wikipedia, Wikimedia Foundation, 10 juillet 2018. Disponible ici
Image gracieuseté:
1.'Pasteonbrush'By theGreenj - Ain Wirk, (CC By-Sa 3.0) via Commons Wikimedia


