Différence entre le solvant et le soluté

Le différence clé entre le solvant et le soluté est que le Le soluté est celui à dissoudre pendant que le solvant est responsable de la dissolution.
Une solution est un mélange homogène de deux ou plusieurs substances. Nous l'appelons un mélange homogène car la composition est uniforme tout au long de la solution. De plus, les composants d'une solution sont principalement de deux types, solutés et solvants. Le solvant dissout les solutés et forme une solution uniforme. Ainsi, normalement la quantité de solvant est supérieure à la quantité de soluté.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le solvant
3. Qu'est-ce que le soluté
4. Comparaison côte à côte - solvant vs soluté sous forme tabulaire
5. Résumé
Qu'est-ce que le solvant?
Le solvant est une substance avec une capacité de dissolution. Ainsi, il peut dissoudre une autre substance. De plus, des solvants peuvent se produire à l'état liquide, gazeux ou solide. Cependant, le plus souvent, nous utilisons des liquides comme solvants. De plus, parmi les liquides, l'eau est commune en tant que solvant universel, car il peut dissoudre de nombreuses substances que tout autre solvant. De plus, nous pouvons dissoudre le gaz, solide ou tout autre soluté liquide dans les solvants liquides. Mais, dans les solvants à gaz, seuls les solutés à gaz se dissoudront.

Figure 01: L'acide acétique est utile comme solvant organique
De plus, il y a une limite à la quantité de solutés que nous pouvons ajouter à une certaine quantité de solvant. Nous disons que la solution est devenue saturée si nous avons ajouté la quantité maximale de solutés au solvant. Il existe des solvants dans deux types en tant que solvants organiques ou inorganiques. Par exemple, l'éther, l'hexane et le chlorure de méthylène sont des solvants organiques, tandis que l'eau est un solvant inorganique.
Solvants polaires et non polaires
Il existe deux grandes catégories de solvants en tant que solvants polaires et solvants non polaires.
Solvant polaire Les molécules ont donc une séparation de charges capable de dissoudre les solutés polaires. Dans le processus de dissolution, des interactions dipol-dipole ou des interactions dipolaires induites par dipôle peuvent se produire. Nous pouvons diviser davantage les solvants polaires en tant que solvants protique et polaire polaire. Les solvants protiques polaires sont capables de formation de liaisons hydrogène avec les solutés. Par conséquent, ils résolvent les anions par liaison hydrogène. L'eau et le méthanol sont des solvants protiques polaires. Les solvants aprotiques polaires ne peuvent pas former des liaisons hydrogène. Cependant, ils ont de grands moments dipolaires, donc forment des interactions dipol-dipole avec les solutés ioniques, par conséquent, solvatez-les. L'acétone est un solvant d'aprotique polaire.
Solvants non polaires dissoudre les solutés non polaires. L'hexane, le benzène et le toluène sont des solvants non polaires courants.
Outre les solvants ci-dessus, il existe des solvants, qui ont des propriétés polaires et non polaires intermédiaires. Selon le phénomène «comme dissoudre comme», les solvants dissolvent des solutés, qui les correspondent.
Propriétés
Les propriétés des solvants sont essentielles pour savoir quand nous les utilisons dans les laboratoires. Par exemple, la connaissance des points d'ébullition des solvants nous aide à déterminer comment utiliser les méthodes de distillation pour les séparer. Alternativement, la densité des solvants est importante dans les techniques d'extraction des solvants. La volatilité, la toxicité et l'inflammabilité sont quelques-uns des autres paramètres, que nous devons nous concentrer lorsque nous travaillons avec différents solvants.
Qu'est-ce que le soluté?
Le soluté est une substance qui se dissout dans un solvant afin de former une solution. Des solutés peuvent se produire en phase liquide, gazeuse ou solide. Normalement, dans une solution, les solutés sont en moindre quantité que les solvants.

Figure 02: L'eau saline contient du sel comme soluté
Lorsqu'une solution a la quantité maximale de solutés qu'il peut se dissoudre, alors nous disons que la solution est devenue saturée. La dissolution du soluté dans le solvant modifie les propriétés des solvants.
Quelle est la différence entre le solvant et le soluté?
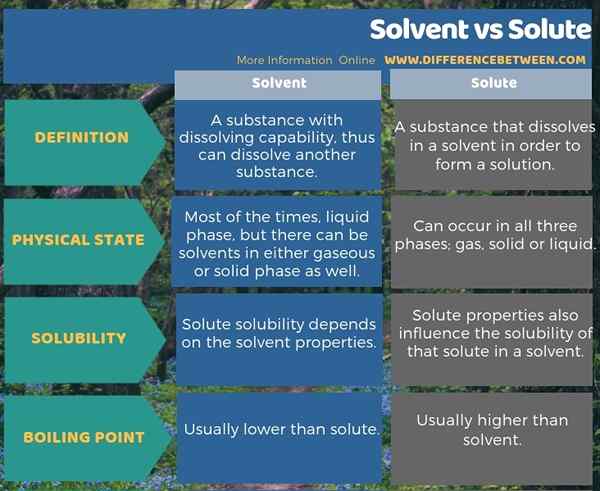
Le solvant est une substance avec une capacité de dissolution, peut donc dissoudre une autre substance tandis que le soluté est une substance qui se dissout dans un solvant afin de former une solution. C'est la principale différence entre le solvant et le soluté. De plus, il existe d'autres différences entre le solvant et le soluté dans leurs états physiques, leur solubilité et leurs points d'ébullition. Par exemple, compte tenu du point d'ébullition, le point d'ébullition d'un soluté est généralement plus élevé que celui d'un solvant.
L'infographie ci-dessous montre plus de détails sur la différence entre le solvant et le soluté.
Résumé - Solvent vs Soluté
Les solutés sont des substances qui se dissolvent dans un solvant pour former une solution. Par conséquent, la différence entre le solvant et le soluté est que le soluté est celui à dissoudre, et le solvant est responsable de la dissolution.
Référence:
1. "Solvant.»Wikipedia, Wikimedia Foundation, 6 septembre. 2018. Disponible ici
2. "Solution.»Wikipedia, Wikimedia Foundation, 21 septembre. 2018. Disponible ici
Image gracieuseté:
1.«Acide acétique» par w. Oelen (CC BY-SA 3.0) via Commons Wikimedia
2.«SaltinwatersolutionLiquid» par Chris 73 (CC By-SA 3.0) via Commons Wikimedia


