Différence entre SO2 et SO3
Le différence clé entre SO2 et SO3 est que DONC2 est un gaz incolore à température ambiante, alors que ça3 est un solide cristallin incolore à blanc.
DONC2 est le dioxyde de soufre tout en3 est le trioxyde de soufre. Les deux sont des oxydes de soufre.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que SO2
3. Qu'est-ce que SO3
4. Comparaison côte à côte - SO2 vs SO3 sous forme tabulaire
5. Résumé
Qu'est-ce que SO2?
DONC2 est le dioxyde de soufre. C'est un composé gazeux incolore contenant des atomes de soufre et d'oxygène. DONC2 est la formule chimique de ce composé. Par conséquent, il contient un atome de soufre lié à deux atomes d'oxygène via des liaisons covalentes. Un atome d'oxygène peut former une double liaison avec l'atome de soufre. Par conséquent, l'atome de soufre est l'atome central du composé. L'atome de soufre possède 6 électrons dans son orbitale la plus externe. Par conséquent, après avoir formé deux doubles liaisons avec les atomes d'oxygène, il reste deux autres électrons; Ces électrons existent comme une paire d'électrons solitaires.
Par conséquent, nous pouvons déterminer la géométrie du SO2 molécule; c'est la géométrie angulaire. DONC2 est polaire en raison de sa géométrie (angulaire) et de la présence d'une paire d'électrons solitaires.
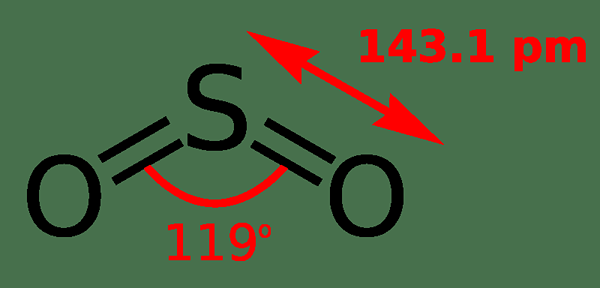
Figure 01: Structure du dioxyde de soufre
Le dioxyde de soufre est considéré comme un gaz toxique. Par conséquent, s'il y a SO2 dans l'atmosphère, ce sera une indication de la pollution de l'air. De plus, ce gaz a une odeur très irritante. La masse moléculaire du dioxyde de soufre est de 64 g / mol. C'est un gaz incolore à température ambiante. Le point de fusion est d'environ -71 ° C, tandis que le point d'ébullition est de -10 ° C.
L'état d'oxydation du soufre dans le dioxyde de soufre est +4. Par conséquent, le dioxyde de soufre peut également être produit par la réduction des composés composés d'atomes de soufre qui sont dans un état d'oxydation plus élevé. Un tel exemple est la réaction entre le cuivre et l'acide sulfurique. Ici, le soufre dans l'acide sulfurique est à l'état d'oxydation de +6. Par conséquent, il peut être réduit à l'état d'oxydation +4 du dioxyde de soufre.
Le dioxyde de soufre peut être utilisé dans la production d'acide sulfurique, qui a un certain nombre d'applications à l'échelle industrielle et à l'échelle de laboratoire. Le dioxyde de soufre est également un bon agent réducteur. Étant donné que l'état d'oxydation du soufre est de +4 dans le dioxyde de soufre, il peut facilement être oxydé à un état d'oxydation +6, ce qui permet à un autre composé d'être réduit.
Qu'est-ce que SO3?
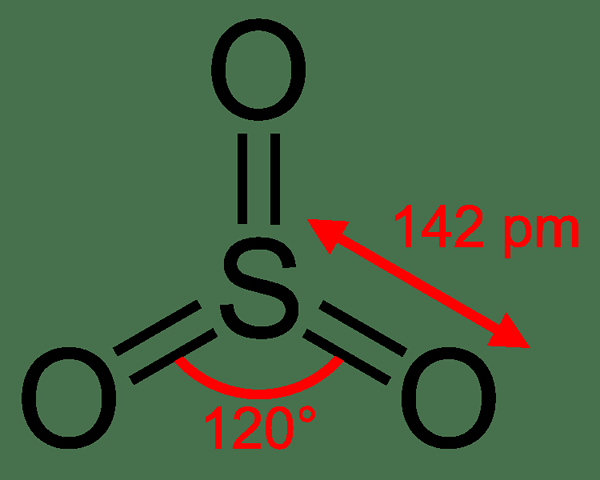
DONC3 est le trioxyde de soufre. C'est un composé solide contenant un atome de soufre qui se lie à trois atomes d'oxygène. DONC3 est la formule chimique de ce composé. Ici, chaque atome d'oxygène a une double liaison avec l'atome de soufre. L'atome de soufre est au centre de la molécule. Un atome de soufre a 6 électrons dans son orbitale la plus externe. Par conséquent, après avoir formé trois doubles liaisons avec les atomes d'oxygène, il ne reste plus d'électrons sur l'atome de soufre comme dans le dioxyde de soufre. Ainsi, cela détermine la géométrie du SO3 molécule; il a une géométrie planaire trigonale. DONC3 est non polaire en raison de sa géométrie (planaire trigonal) et de l'absence d'une paire d'électrons solitaires.

Figure 02: Géométrie du trioxyde de soufre
La masse moléculaire du trioxyde de soufre est de 80.057 g / mol. Le point de fusion de SO3 est environ 16.9 ° C, tandis que le point d'ébullition est de 45 oC. À température ambiante et à la pression, le trioxyde de soufre est un composé solide cristallin blanc qui fumera dans l'air. Il a une odeur piquante. L'état d'oxydation du soufre dans le trioxyde de soufre est +6.
Dans sa forme gazeuse, le trioxyde de soufre est un polluant atmosphérique et est un composant majeur des pluies acides. Cependant, le trioxyde de soufre est très important dans la production d'acide sulfurique à l'échelle industrielle. C'est parce que le trioxyde de soufre est la forme d'anhydride d'acide sulfurique.
DONC3 (l) + H2O(l) → H2DONC4 (l)
La réaction ci-dessus est très rapide et exothermique. Par conséquent, les méthodes de contrôle doivent être utilisées lors de l'utilisation du trioxyde de soufre pour la production d'acide sulfurique industriel. En outre, le trioxyde de soufre est un réactif essentiel du processus de sulfonation.
Quelle est la différence entre SO2 et SO3?
DONC2 est le dioxyde de soufre tout en3 est le trioxyde de soufre. Les deux sont des oxydes de soufre. La principale différence entre SO2 et SO3 est que SO2 est un gaz incolore à température ambiante, alors que ça3 est un solide cristallin incolore à blanc. De plus, l'état d'oxydation du soufre dans le dioxyde de soufre est +4 tandis que dans le trioxyde de soufre, il est +6. En raison de la présence d'une paire d'électrons solitaires et de leur géométrie, le dioxyde de soufre est un composé polaire, tandis que le trioxyde de soufre est un composé non polaire. L'infographie suivante résume la différence entre SO2 et SO3.

Résumé - SO2 vs SO3
DONC2 est le dioxyde de soufre, et donc3 est le trioxyde de soufre. Les deux sont des oxydes de soufre. La principale différence entre SO2 et SO3 est que SO2 est un gaz incolore à température ambiante, alors que ça3 est un solide cristallin incolore à blanc.
Référence:
1. Brandt, Malcolm J., et al. «Stockage chimique, dosage et contrôle.»Tworts Water Supply, 2017, pp. 513-552., doi: 10.1016 / B978-0-08-100025-0.00012-0.
Image gracieuseté:
1. «Sulphur-dioxyde-2d» par le téléchargeur d'origine était Richtom80 à English Wikipedia. - Transféré de EN.Wikipedia à Commons (domaine public) via Commons Wikimedia
2. «Sulphur-Trioxide-2D-Dimensions» par Jynto - Propre travaux, basé sur le dossier: Sulfur-Trioxide-2D-Dimensions.PNG (domaine public) via Commons Wikimedia


