Différence entre le silane et le siloxane
Le différence clé entre le silane et le siloxane est que Le silane est un composé chimique tandis que le siloxane est un groupe fonctionnel dans l'organosilicon.
Le silane et le siloxane sont des composés contenant du silicone. Ces deux matériaux sont importants en tant que scellants. Ici, le scellant Silane a tendance à pénétrer profondément pour la protection sous la surface tandis que le scellant Siloxane travaille à la surface pour une répulsion en eau.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le silane
3. Qu'est-ce que le siloxane
4. Comparaison côte à côte - Silane vs Siloxane sous forme tabulaire
5. Résumé
Qu'est-ce que le silane?
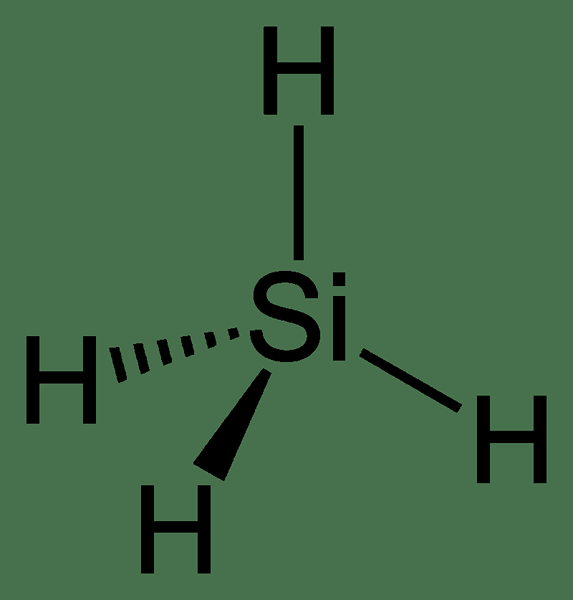
Le silane est un composé inorganique ayant la formule chimique sih4. C'est un hydrure du groupe 14. De plus, cette substance se produit comme un gaz incolore ayant une odeur répulsive. L'odeur est similaire à l'odeur de l'acide acétique. Sa masse molaire est de 32.11 g / mol. De plus, la voie la plus courante à l'échelle commerciale pour la production de silane est la réaction du chlorure d'hydrogène avec le silicide en magnésium.

Figure 01: Structure de la molécule de silane
La forme de la molécule de silane est tétraédrique, similaire à la molécule de méthane. En raison de la grande différence entre les valeurs d'électronégativité du silicone et de l'hydrogène, il a une polarité opposée à celle du méthane. En raison de cette polarité inversée, le silane peut former des complexes avec des métaux de transition. De plus, le silane peut subir une combustion spontanée dans l'air. Cela signifie; il ne nécessite aucune source d'allumage externe. De plus, l'application dominante du silane est un précurseur pour la production de silicium élémentaire. Ceci est important dans la production de semi-conducteurs. Il est également utile comme scellant.
Qu'est-ce que le siloxane?
Siloxane est un groupe fonctionnel ayant la liaison SI-O-SI. Le groupe fonctionnel est présent dans les composés organosilicon. Les composés siloxane peuvent être soit des composés à chaîne droite, soit des composés ramifiés. Ces liens forment l'épine dorsale du polymère en silicone, i.e. polydiméthylsiloxane.
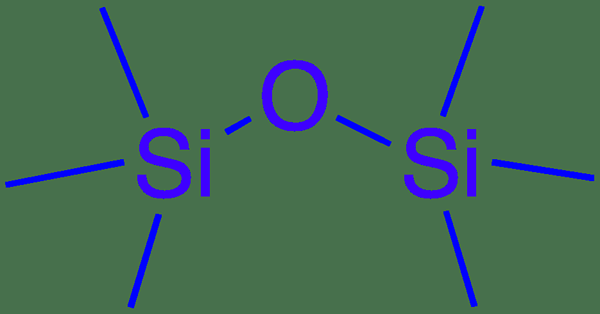
Figure 02: Lien de siloxane
De plus, la principale voie de formation d'une liaison de siloxane est par condensation de deux silanols. Nous pouvons produire du silanol par hydrolyse du chlorure de silyle. Ce composé est également important pour fabriquer du carbure de silicium lors de l'allumage dans une atmosphère inerte. De plus, les polymères de siloxane sont utiles comme scellants pour les surfaces d'étanchéité.
Quelle est la différence entre le silane et le siloxane?
Le silane est un composé inorganique ayant la formule chimique sih4 tandis que Siloxane est un groupe fonctionnel ayant le lien SI-O-SI. La principale différence entre le silane et le siloxane est que le silane est un composé chimique tandis que le siloxane est un groupe fonctionnel dans l'organosilicon. De plus, l'application dominante du silane l'utilise comme précurseur pour la production de silicium élémentaire, tandis que le siloxane est important pour faire du carbure de silicium.
L'infographie ci-dessous montre plus de comparaisons liées à la différence entre le silane et le siloxane.
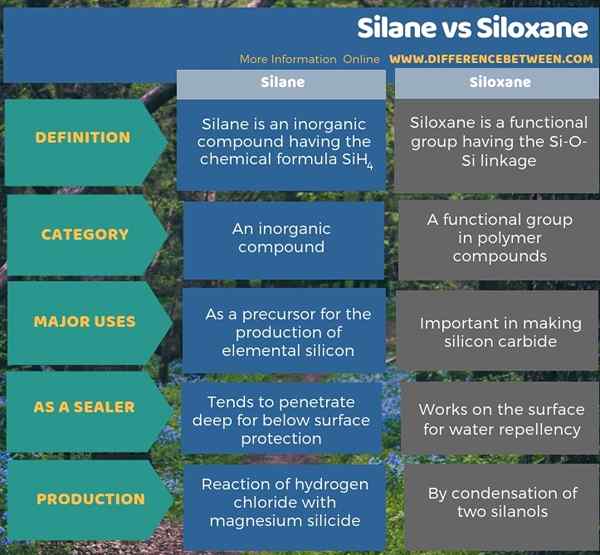
Résumé - Silane vs Siloxane
Le silane est un composé inorganique ayant la formule chimique sih4 tandis que Siloxane est un groupe fonctionnel ayant le lien SI-O-SI. La principale différence entre le silane et le siloxane est que le silane est un composé chimique tandis que le siloxane est un groupe fonctionnel dans l'organosilicon.
Référence:
1. «Silane.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine, disponible ici.
2. Tilley, Sloane K., et Rebecca C. Frire. «Contaminants environnementaux prioritaires.»Systèmes Biology in Toxicology and Environmental Health, 2015, PP. 117-169., doi: 10.1016 / B978-0-12-801564-3.00006-7.
Image gracieuseté:
1. «Silane-2d» (domaine public) via Commons Wikimedia
2. «SiloxaneFxnlgp» par Smokefoot - Propre travaux (CC By-SA 3.0) via Commons Wikimedia


