Différence entre la résonance et la conjugaison π
Le différence clé entre la résonance et la conjugaison π est que La résonance fait référence à la stabilité d'une molécule en présence d'électrons délocalisés, tandis que la conjugaison π fait référence au concept d'électrons Pi distribué dans toute la zone d'une molécule plutôt que d'appartenir à un seul atome de la molécule.
La résonance et la conjugaison π sont des termes étroitement liés car la conjugaison π provoque une résonance dans les composés chimiques.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la résonance
3. Qu'est-ce que la conjugaison π
4. Comparaison côte à côte - Resonance vs π conjugaison sous forme tabulaire
5. Résumé
Qu'est-ce que la résonance?
La résonance est un concept chimique qui décrit l'interaction entre les paires d'électrons solitaires et les paires d'électrons de liaison d'un composé. Généralement, l'effet de la résonance est utile pour déterminer la structure chimique réelle de ce composé organique ou inorganique. Cet effet apparaît également dans des composés chimiques contenant des doubles liaisons et des paires d'électrons solitaires. De plus, cet effet provoque la polarité des molécules.
La résonance montre la stabilisation d'un composé chimique via la délocalisation des électrons dans les liaisons PI. Ici, les électrons dans les molécules peuvent se déplacer autour des noyaux atomiques car un électron n'a pas de position fixe à l'intérieur des atomes. Par conséquent, les paires d'électrons solitaires sont capables de passer à des liaisons PI et vice versa. Cela se produit pour obtenir un état stable. Ce processus de mouvement d'électrons est connu sous le nom de résonance. De plus, nous pouvons utiliser des structures de résonance afin d'obtenir la structure la plus stable d'une molécule.

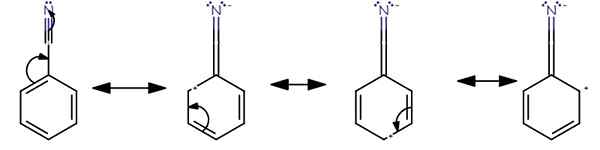
Figure 01: Résonance dans le benzonitrile
Une molécule peut avoir plusieurs structures de résonance basées sur le nombre de paires solitaires et de liaisons Pi présente dans cette molécule. Toutes les structures de résonance d'une molécule ont le même nombre d'électrons et le même arrangement d'atomes. La structure réelle de cette molécule est une structure hybride dans toutes les structures de résonance. Il existe deux types d'effet de résonance: l'effet de résonance positive et l'effet de résonance négatif.
L'effet de résonance positive explique la résonance qui peut être trouvée dans les composés ayant une charge positive. L'effet de résonance positive aide à stabiliser la charge positive dans cette molécule. L'effet de résonance négative explique la stabilisation d'une charge négative dans une molécule. Cependant, la structure hybride obtenue compte tenu de la résonance a une énergie plus faible que toutes les structures de résonance.
Qu'est-ce que la conjugaison π?
Le terme conjugaison π fait référence à la délocalisation dans des composés organiques où nous pouvons observer la distribution des électrons Pi sans liaison à travers une molécule. Par conséquent, nous pouvons décrire les électrons dans un système de conjugaison π comme les électrons sans liaison dans ce composé chimique. De plus, ce terme fait référence à des électrons qui ne sont pas associés à un seul atome ou à une liaison covalente.
À titre d'exemple simple, nous pouvons donner du benzène comme système aromatique ayant des électrons délocalisés. Généralement, un anneau de benzène a six électrons Pi dans la molécule de benzène; Nous les indiquons souvent en utilisant graphiquement un cercle. Ce cercle signifie que les électrons Pi sont associés à tous les atomes de la molécule. Cette délocalisation fait que l'anneau de benzène a des liaisons chimiques avec des longueurs de liaison similaires.
Quelle est la différence entre la résonance et la conjugaison π?
La résonance et la conjugaison PI sont des termes étroitement liés. La principale différence entre la résonance et la conjugaison π est que la résonance se réfère à la stabilité d'une molécule en présence d'électrons délocalisés tandis que la conjugaison π se réfère au concept d'électrons Pi distribué dans toute la zone d'une molécule plutôt que d'appartenir à un seul atome d'atome dans la molécule.
L'infographie ci-dessous résume la différence entre la résonance et la conjugaison π sous forme tabulaire.
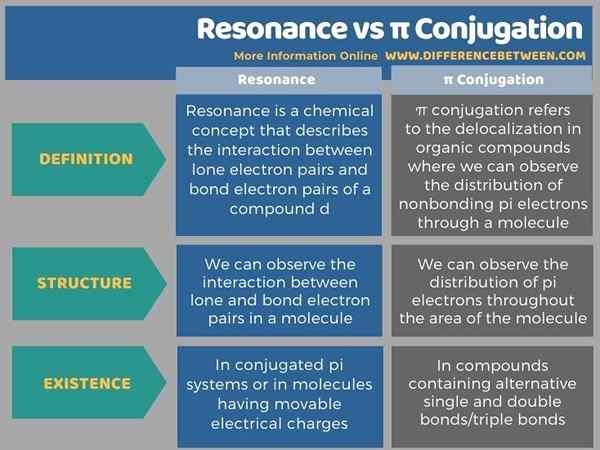
Résumé - Resonance vs π conjugaison
La résonance et la conjugaison π sont des termes étroitement liés où la conjugaison π provoque la résonance dans les composés chimiques. La principale différence entre la résonance et la conjugaison π est que la résonance se réfère à la stabilité d'une molécule en présence d'électrons délocalisés tandis que la conjugaison π se réfère au concept d'électrons Pi distribué dans toute la zone d'une molécule plutôt que d'appartenir à un seul atome d'atome dans la molécule.
Référence:
1. «Conjugaison et résonance en chimie organique." Maître chimie organique, 26 janvier. 2020, disponible ici.
Image gracieuseté:
1. «Benzonitrile Resonance» par Fung06831 - Propre travaux (CC BY-SA 4.0) via Commons Wikimedia


