Différence entre NF3 et NH3
Le différence clé entre NF3 et NH3 est que NF3 contient trois atomes de fluor liés à un atome d'azote central, tandis que NH3 contient trois atomes d'hydrogène liés à un atome d'azote central.
NF3 est le trifluorure d'azote tandis que le NH3 est de l'ammoniac. Les deux sont des composés inorganiques, et les deux composés ont la même géométrie moléculaire. Cependant, ils ont des propriétés chimiques et physiques différentes en raison de différentes compositions atomiques.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que NF3
3. Qu'est-ce que NH3
4. Similitudes entre NF3 et NH3
5. Comparaison côte à côte - NF3 vs NH3 sous forme tabulaire
6. Résumé
Qu'est-ce que NF3?
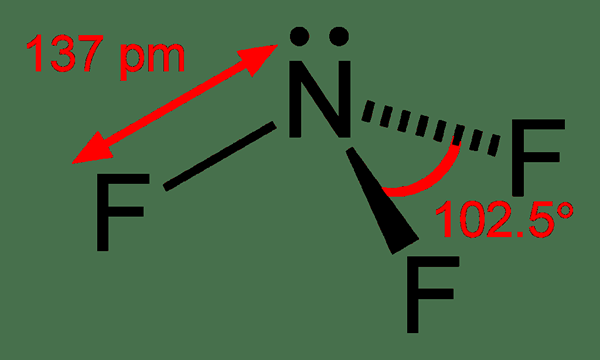
NF3 est un trifluorure d'azote. Son nom commun est trifluoramine. Il a trois atomes de fluor liés au même atome d'azote via une liaison chimique covalente. Étant donné que l'azote a cinq électrons de valence et que les trois atomes de fluor n'utilisent que trois de ces électrons pour faire des liaisons chimiques, il y a une paire d'électrons solitaires sur l'atome d'azote. La paire d'électrons et trois liaisons covalentes font que la molécule NF3 a une géométrie pyramidale trigonale. La structure est la suivante:

Figure 01: Structure du trifluorure d'azote
La masse molaire du trifluorure d'azote est de 71 g / mol. Il apparaît comme un gaz incolore, et il a une odeur moisi. De plus, il s'agit d'un gaz non inflammable. Cependant, ce gaz est un gaz à effet de serre fort. En présence de décharges électriques, nous pouvons préparer ce composé en utilisant ses éléments chimiques; Ainsi, c'est un composé rare que nous pouvons préparer directement en utilisant ses éléments chimiques (azote et atomes de fluor).
D'ailleurs, ce composé montre une solubilité importante dans l'eau. De plus, le trifluoride d'azote n'est pas basique et il a un moment dipolaire faible car les atomes de fluor agissent comme des groupes de tire-éléments; Ainsi, ils peuvent attirer la paire d'électrons solitaires sur l'atome d'azote. De plus, ce composé est également un puissant oxydant. Lorsque vous envisagez les utilisations de ce composé, il est utile dans la gravure du plasma des plaquettes de silicium dans les applications électrochimiques.
Qu'est-ce que NH3?
NH3 est l'ammoniac. Il a trois atomes d'hydrogène liés au même atome d'azote. Comme le trifluorure d'azote, ce composé a également une paire d'électrons solitaires. C'est un halogénure binaire. De plus, ce composé se produit comme un gaz incolore, et il a une odeur piquante et irritante. La géométrie de ce composé est pyramidale trigonale.
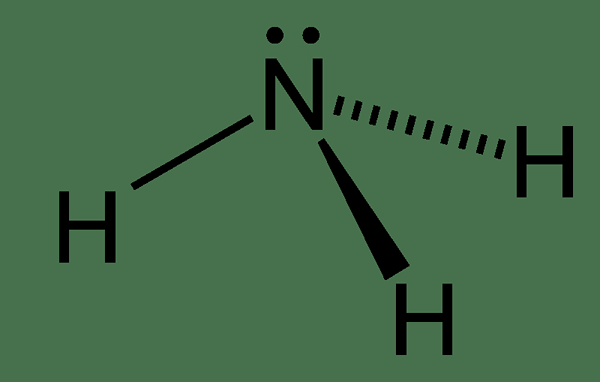
Figure 02: Structure de la molécule d'ammoniac
La masse molaire d'ammoniac est de 17 g / mol. Dans la nature, nous pouvons trouver ce gaz comme un composé de trace formé à partir de déchets azotés et d'animaux azotés et végétaux. Lorsque vous envisagez ses utilisations, environ 88% de l'ammoniac est utilisé pour la production d'engrais. Il est également utile comme précurseur pour les composés azotés. Dans les processus de fermentation, l'ammoniac est utile comme source d'azote pour les micro-organismes. L'ammoniac aqueux est également important en tant que plus propre dans les applications ménagers.
Quelles sont les similitudes entre NF3 et NH3?
- NF3 et NH3 sont des composés binaires.
- Ils ont la même géométrie - trigonal pyramidal
- De plus, les deux se produisent sous forme de gaz incolores
- En plus de ceux-ci, les deux molécules ont des paires d'électrons solitaires sur les atomes d'azote.
Quelle est la différence entre NF3 et NH3?
NF3 est le trifluorure d'azote tandis que le NH3 est de l'ammoniac. La principale différence entre NF3 et NH3 est que le NF3 contient trois atomes de fluor liés à un atome d'azote central, tandis que le NH3 contient trois atomes d'hydrogène liés à un atome d'azote central. La masse molaire du trifluorure d'azote est de 71 g / mol tandis que la masse molaire d'ammoniac est 17 g / mol. De plus, NF3 est non basique tandis que NH3 est un composé de base; NF3 a un moment dipolaire faible, mais NH3 a un moment dipolaire élevé. NF3 est principalement utile dans la gravure du plasma des plaquettes de silicium dans les applications électrochimiques. En revanche, le NH3 est utile pour la production d'engrais, pour la fermentation comme source d'azote, en tant que nettoyant dans les applications ménagères, etc.
L'infographie ci-dessous résume la différence entre NF3 et NH3.
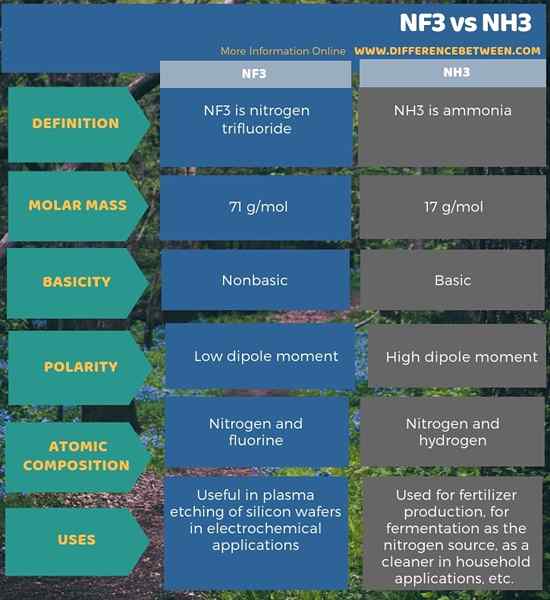
Résumé - NF3 vs NH3
NF3 est le trifluorure d'azote tandis que le NH3 est de l'ammoniac. Les deux sont des composés inorganiques. La principale différence entre NF3 et NH3 est que le NF3 contient trois atomes de fluor liés à un atome d'azote central, tandis que le NH3 contient trois atomes d'hydrogène liés à un atome d'azote central.
Référence:
1.«Trifluorure d'azote.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine, disponible ici.
2. "Ammoniac.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine, disponible ici.
3. «Trifluorure d'azote.»Wikipedia, Wikimedia Foundation, 23 septembre. 2019, disponible ici.
Image gracieuseté:
1. «Nitrogen-Trifluorride-2d-Dimensions» par Benjah-BMM27 - propre travail (domaine public) via Commons Wikimedia
2. «Ammoniac-2d» par Radio89 - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


