Différence entre molécule et atome
Le différence clé entre la molécule et l'atome est que La molécule est une combinaison de deux atomes ou plus via la liaison chimique tandis que l'atome est une espèce chimique individuelle qui peut se combiner pour former des molécules et des ions.
Toute la matière dans le monde est composée d'atomes et de molécules, donc nous pouvons les considérer comme les éléments constitutifs de tout sur cette planète, y compris nous. En termes simples, nous pouvons dire que la plus basique et aussi la plus petite unité de tout élément chimique est un atome. Un élément chimique est une espèce d'atomes. Par exemple, la plus petite unité d'oxygène est l'atome d'oxygène; Nous pouvons le représenter par lettre o. Cependant, cet atome d'oxygène n'existe pas indépendamment, et ce n'est que lorsqu'il se combine chimiquement avec un autre atome d'oxygène qu'il devient stable. Il devient alors une molécule, et nous pouvons le représenter par la formule chimique O2.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce qu'une molécule
3. Qu'est-ce qu'un atome
4. Comparaison côte à côte - molécule vs atome sous forme tabulaire
5. Résumé
Qu'est-ce qu'une molécule?
Une molécule est un groupe d'atomes qui se combinent entre eux via des liaisons chimiques. Ces atomes peuvent être du même élément chimique ou différents éléments chimiques. Une molécule homonucléaire se forme lorsque les atomes du même élément chimique constituent la molécule. Une molécule hétéronucléaire se forme lorsque des atomes de différents éléments chimiques se combinent les uns avec les autres.
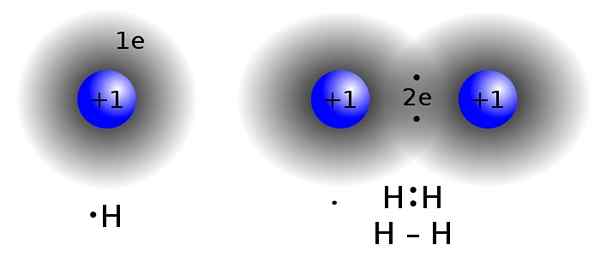
Les atomes d'une molécule peuvent se lier entre eux via des liaisons covalentes ou des liaisons ioniques. Une liaison chimique covalente se forme lorsque les atomes partagent leurs électrons entre eux pour compléter l'octet de la configuration d'électrons. Les liaisons ioniques se forment lorsque les électrons échangent complètement entre les atomes. Cela forme des cations (ions chargés positivement) et des anions (ions chargés négativement) qui sont maintenus ensemble par des forces d'attraction électrostatique ou des liaisons ioniques.

Figure 01: Formation d'une molécule d'hydrogène
Pour comprendre les atomes présents dans une molécule, nous pouvons utiliser sa formule chimique. La formule chimique est un ensemble de symboles qui donnent les atomes et les rapports entre eux qui se combinent pour former la molécule. Parfois, à part le symbole chimique des atomes et des nombres, nous utilisons également d'autres symboles; parenthèses, tirets, supports et plus (+) et moins (-) Signes. Nous pouvons calculer la masse moléculaire de la molécule en utilisant cette formule chimique. De plus, nous pouvons utiliser une formule structurelle qui donne la disposition des atomes dans la molécule.
Différentes molécules ont des géométries différentes. Par conséquent, la géométrie affiche la disposition spatiale des atomes. Il donne ainsi les longueurs de liaison et les angles de liaison entre ces atomes. Certaines molécules ont une géométrie symétrique tandis que d'autres ont des géométries non symétriques.
Qu'est-ce qu'un atome?
Un atome est la plus petite unité de répétition qui constitue toute la matière. Un élément chimique est une espèce d'atomes; Ainsi, les atomes ont des propriétés chimiques et physiques de son élément chimique particulier. Un atome est extrêmement petit; La taille est environ 100 h. Il se compose d'un noyau atomique contenant des protons et des neutrons. Ce noyau est entouré d'un nuage d'électrons. Les protons, les neutrons et les électrons sont des particules subatomiques d'un atome.
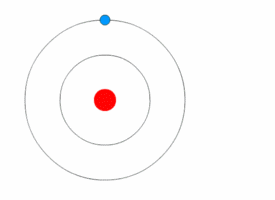
Figure 02: Modèle de Bohr d'un atome
En règle générale, le nombre de protons est égal au nombre d'électrons et de neutrons. Parfois, il y a des atomes qui ont un nombre élevé ou un faible nombre de neutrons que le nombre de protons, par conséquent, nous les nommons comme des isotopes du même élément chimique. De plus, le terme nucléons fait référence aux unités de protons et de neutrons. Ces nucléons déterminent la masse de l'atome car la masse d'un électron est négligeable par rapport aux protons et aux neutrons. Il existe de nombreuses théories qui sont entrées sur la scène afin de montrer la structure des atomes. je.e. Théorie de Dalton, J.J. La théorie du pudding de la prune de Thompson, la structure atomique de Bohr et la théorie atomique moderne.
Quelle est la différence entre la molécule et l'atome?
Les molécules sont constituées d'atomes. Par conséquent, la principale différence entre la molécule et l'atome est qu'une molécule est une combinaison de deux atomes ou plus via la liaison chimique alors qu'un atome est une espèce chimique individuelle qui peut se combiner entre elles pour former des molécules et des ions. De plus, nous pouvons utiliser des symboles chimiques pour représenter une molécule; Nous le nommez comme une formule chimique. En conséquence, une formule chimique montre les symboles des atomes présents dans la molécule. Cependant, pour les atomes, une lettre anglaise montre le symbole d'un élément chimique auquel appartient l'atome. Par conséquent, la formule chimique d'une molécule a un ensemble de lettres anglaises ainsi que le nombre et certains autres symboles tels que les parenthèses, les tirets, les supports et plus (+) et moins (-) Signes. Un seul atome ne peut pas exister indépendamment, sauf pour les gaz nobles tandis que les molécules existent indépendamment car elles ont une faible énergie.
De plus, sur la base de l'existence, la différence entre la molécule et l'atome est que la molécule a une existence stable alors que les atomes individuels sont instables. L'infographie ci-dessous fournit plus de faits sur la différence entre la molécule et l'atome.

Résumé - molécule vs atome
Les molécules et les ions se forment des atomes. Par conséquent, la principale différence entre la molécule et l'atome est qu'une molécule est une combinaison de deux atomes ou plus via le corps chimique tandis qu'un atome est une espèce chimique individuelle qui peut se combiner entre elles pour former des molécules et des ions.
Référence:
1. Helmenstine, Anne Marie, Ph.D. «Qu'est-ce qu'une molécule?”Thoughtco, Jun. 11, 2018. Disponible ici
2. "Atome.»Wikipedia, Wikimedia Foundation, 10 octobre. 2018. Disponible ici
Image gracieuseté:
1.«Hydrogène de liaison covalente» par Jacek FH - Propre travaux, (CC BY-SA 3.0) via Commons Wikimedia
2."Bohr Atom Animation 2" par Kurzon - Propre travaux, (CC BY-SA 3.0) via Commons Wikimedia


