Différence entre électrons localisés et délocalisés
Le différence clé entre les électrons localisés et délocalisés est que Les électrons localisés sont situés entre les atomes, tandis que les électrons délocalisés sont situés au-dessus et au-dessous des atomes.
En chimie générale, les électrons localisés et les électrons délocalisés sont des termes qui décrivent les structures chimiques des composés chimiques. Les électrons localisés sont les électrons de liaison dans les molécules tandis que les électrons délocalisés sont des électrons sans liaison qui se produisent sous forme de nuages d'électrons au-dessus et en dessous de la molécule.
CONTENU
1. Aperçu et différence clé
2. Que sont les électrons localisés
3. Que sont les électrons délocalisés
4. Comparaison côte à côte - électrons localisés vs délocalisés sous forme tabulaire
5. Résumé
Que sont les électrons localisés?
Les électrons localisés sont les électrons de liaison dans des composés chimiques. Ces électrons sont situés entre les atomes où des liaisons sigma peuvent être trouvées. Les obligations Sigma sont les obligations formées par le chevauchement axial des orbitales atomiques à moitié remplies d'atomes.
Par conséquent, des électrons localisés se produisent dans des composés covalents ayant des liaisons chimiques covalentes. Ces électrons localisés appartiennent à deux atomes particuliers, contrairement aux électrons délocalisés, qui sont communs à tous les atomes de la molécule. Les électrons localisés sont partagés entre les atomes formant des liaisons covalentes, des liaisons de coordination, etc.
Que sont les électrons délocalisés?
Les électrons délocalisés sont les électrons sans liaison dans les composés chimiques. Ce terme fait référence aux électrons qui ne sont pas associés à un seul atome ou à une liaison covalente. Cependant, le terme électron délocalisé a des significations différentes dans différents champs. Par exemple, en chimie organique, les électrons délocalisés sont dans les structures de résonance des systèmes conjugués dans des composés aromatiques. En physique à l'état solide, les électrons délocalisés sont les électrons libres qui facilitent la conduction électrique. De plus, la physique quantique utilise le terme électrons délocalisés pour désigner les électrons orbitaux moléculaires qui se sont étendus sur plusieurs atomes.

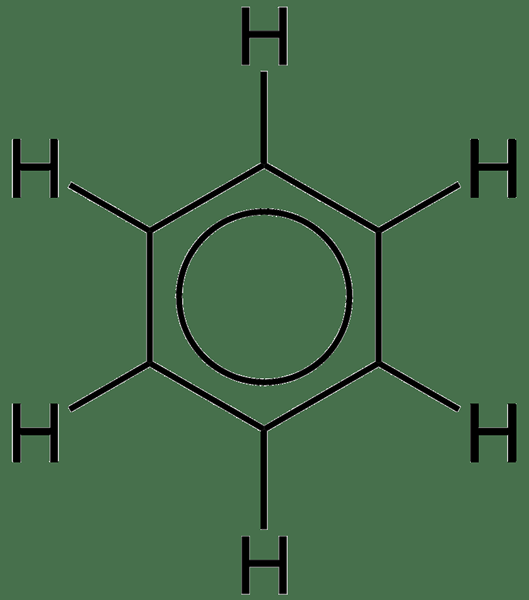
Figure 01: Benzène, (la délocalisation des électrons est indiquée par le cercle)
L'anneau de benzène est l'exemple le plus simple d'un système aromatique ayant des électrons délocalisés. Il y a six électrons Pi dans la molécule de benzène; Nous les indiquons souvent en utilisant graphiquement un cercle. Ce cercle signifie que les électrons Pi sont associés à tous les atomes de la molécule. Cette délocalisation fait que l'anneau de benzène a des liaisons chimiques avec des longueurs de liaison similaires.
Quelle est la différence entre les électrons localisés et délocalisés?
Nous utilisons des termes électrons localisés et délocalisés sous la branche de la chimie générale, concernant la structure chimique des composés. Un atome localisé est un électron qui appartient à un atome particulier tandis qu'un électron délocalisé est un électron non associé à un seul atome ou à une seule liaison covalente. La principale différence entre les électrons localisés et délocalisés est que les électrons localisés sont situés entre les atomes, tandis que les électrons délocalisés sont situés au-dessus et en dessous des atomes. En d'autres termes, les électrons localisés se limitent à une région particulière entre deux atomes tandis que les électrons délocalisés sont répartis sur plusieurs atomes.
De plus, une autre différence significative entre les électrons localisés et délocalisés est que les électrons localisés sont associés à des atomes particuliers dans un composé tandis que les électrons délocalisés sont associés à tous les atomes de la molécule. En outre, les électrons localisés sont graphiquement indiqués par des lignes droites, tandis que les électrons délocalisés sont graphiquement indiqués par des cercles.
Le tableau suivant résume les différences entre les électrons localisés et délocalisés.

Résumé - électron localisé et délocalisé
Les termes électrons localisés et délocalisés sont discutés sous chimie générale. La principale différence entre les électrons localisés et délocalisés est que les électrons localisés sont situés entre les atomes, tandis que les électrons délocalisés sont situés au-dessus et en dessous des atomes. De plus, les électrons délocalisés sont associés à des atomes particuliers dans un composé tandis que les électrons délocalisés sont associés à tous les atomes de la molécule.
Référence:
1. «Paires et liens solitaires et délocalisés." Étapes de chimie, 22 août. 2020, disponible ici.
2. «Electron délocalisé.»Wikipedia, Wikimedia Foundation, 13 juillet 2020, disponible ici.
Image gracieuseté:
1. «Benz4» par Selfmade par Cacycle, Leyo - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


