Différence entre la masse atomique du Gram et la masse moléculaire du gramme
Le différence clé entre la masse atomique du Gram et la masse moléculaire du gram La masse atomique du gramme donne la masse d'un atome individuel tandis que la masse moléculaire de Gram donne la masse d'un groupe d'atomes.
La masse atomique et la masse moléculaire (ou masse molaire) sont très importantes en ce qui concerne les atomes et les molécules. Lorsque nous exprimons ces valeurs en unités de Gram, alors c'est la masse atomique / moléculaire Gram.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que la masse atomique Gram
3. Qu'est-ce que la masse moléculaire de Gram
4. Comparaison côte à côte - GRAM MASSE ATOMIQUE VS GRAM MASSUR MOLUCulaire sous forme tabulaire
5. Résumé
Qu'est-ce que la masse atomique Gram?
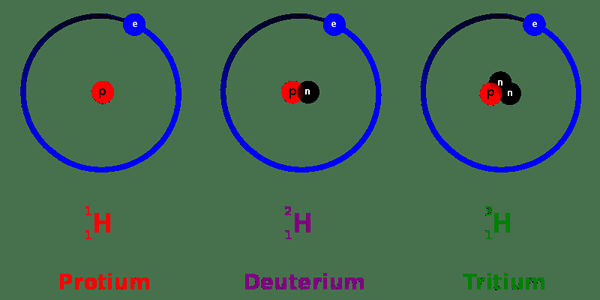
La masse atomique du Gram est la masse atomique exprimée avec l'unité «Grams». La valeur de ce paramètre est numériquement égale à la masse atomique donnée par l'unité «u». Ce terme est très étroitement lié au numéro de masse. Cela signifie en fait la même chose littéralement; Cependant, dans ce cas, les formes isotopiques de chaque élément sont également comptées. Les éléments peuvent exister sous diverses formes dans la nature. Ces différentes formes sont généralement appelées isotopes, et elles ont la même identité que la forme la plus abondante / stable de l'élément. Par conséquent, les isotopes ont le même nombre atomique, mais ils ont des nombres de masse différents. On peut conclure que les isotopes transportent la même quantité de protons et d'électrons; ce n'est que le nombre de neutrons qui diffèrent. Par conséquent, ce qui diffère entre eux, c'est le poids.

Figure 01: Isotopes de l'hydrogène
Lors de la prise en considération de chaque forme isotopique, la masse d'une forme élémentaire peut être exprimée comme une valeur moyenne, où les masses individuelles de chaque forme isotopique sont moyennées. De plus, ceci est appelé la «masse atomique» d'un élément. Par conséquent, la masse atomique a presque la même valeur numérique que le nombre de masse, avec seulement un changement de quelques valeurs décimales. Chaque numéro est utilisé à ses fins de commodité en fonction du contexte d'utilisation.
Qu'est-ce que la masse moléculaire de Gram?
La masse moléculaire de gramme d'une molécule est la masse d'une mole de cette molécule donnée de l'unité «Grams». Cela signifie; C'est la somme des masses de molécules présentes dans une taupe. Il est calculé en utilisant la formule moléculaire d'une molécule. Ici, les poids atomiques de chaque atome en unité G / mol sont ajoutés pour obtenir la masse moléculaire.
Une mole d'une molécule est composée de 6.023 x 1023 molécules. Par conséquent, la masse moléculaire est le poids de 6.023 x 1023 molécules. Étant donné que les masses atomiques de chaque élément sont connues, il est facile de calculer la masse moléculaire plutôt que de penser à un 6.023 x 1023 de molécules.
Quelle est la différence entre la masse atomique du Gram et la masse moléculaire du Gram?
La masse atomique du Gram et la masse moléculaire de gramme sont les mêmes que la masse atomique et la masse moléculaire, exprimée dans l'unité «Grams». Par conséquent, la principale différence entre la masse atomique du Gram et la masse moléculaire du Gram est que la masse atomique du Gram donne la masse d'un atome individuel, tandis que la masse moléculaire de gramme donne la masse d'un groupe d'atomes.
L'infographie ci-dessous résume la différence entre la masse atomique du Gram et la masse moléculaire de Gram.
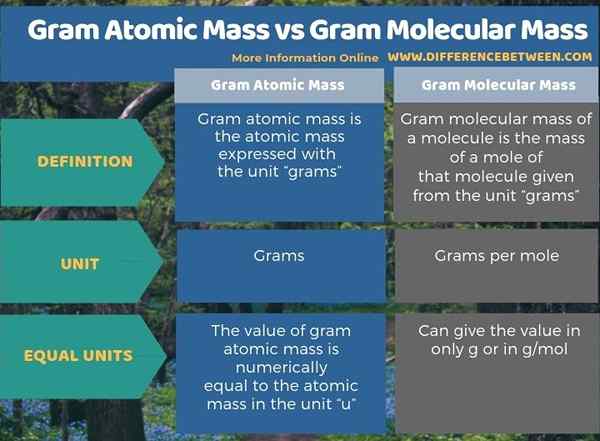
Résumé - Gram Masse atomique vs Gram Masse moléculaire
La masse atomique du Gram et la masse moléculaire de gramme sont les mêmes que la masse atomique et la masse moléculaire, exprimée dans l'unité «Grams». Par conséquent, la principale différence entre la masse atomique du Gram et la masse moléculaire du Gram est que la masse atomique du Gram donne la masse d'un atome individuel, tandis que la masse moléculaire de gramme donne la masse d'un groupe d'atomes.
Référence:
1. Helmenstine, Anne Marie. «Définition de masse moléculaire de Gram."Thoughtco, juil. 3, 2019, disponible ici.
Image gracieuseté:
1. «Hydrogène Deuterium tritium noyaux Schmatic-en» par Dirk Hünniger; travail dérivé en anglais - balajijagadesh - Ce fichier a été dérivé de: Hydrogène Deuterium tritium noyaux Schmatic-de.SVG (CC BY-SA 3.0) via Commons Wikimedia


