Différence entre l'éthylène glycol et le diéthylène glycol
Différence clé - éthylène glycol vs Diéthylène Glycol
Le différence clé entre l'éthylène glycol et le diéthylène glycol est que Une molécule d'éthylène glycol est une molécule individuelle tandis que la molécule de diéthylène glycol est formée par la combinaison de deux molécules d'éthylène glycol via une liaison éther.
L'éthylène glycol et le diéthylène glycol sont des composés organiques qui ont des applications dans la production de refroidissement pour les moteurs. Ils ont des structures étroitement liées; Un diéthylène glycol est une combinaison de molécules à l'éthylène glycol.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'éthylène glycol
3. Qu'est-ce que le diéthylène glycol
4. Similitudes entre l'éthylène glycol et le diéthylène glycol
5. Comparaison côte à côte - éthylène glycol vs diéthylène glycol sous forme tabulaire
6. Résumé
Qu'est-ce que l'éthylène glycol?
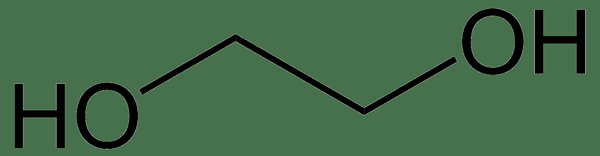
L'éthylène glycol est un alcool ayant le formulac chimique2H6O2. Le nom IUPAC de ce composé est éthane-1,2-diol. À température ambiante et à la pression, c'est un liquide incolore et inodore qui est une dégustation douce et visqueuse. Ce liquide est modérément toxique. La masse molaire d'éthylène glycol est de 62 g / mol. Le point de fusion de ce liquide est de -12.9 ° C et le point d'ébullition était 197.3 ° C. L'éthylène glycol est miscible avec l'eau car il a des groupes -OH capables de former des liaisons hydrogène.

Figure 01: Structure chimique de l'éthylène glycol
Il existe deux façons de produire de l'éthylène glycol; Production d'échelle industrielle et voie biologique pour la production d'éthylène glycol. Dans la production d'échelle industrielle, l'éthylène glycol est produit à partir de l'éthylène. L'éthylène est converti en oxyde d'éthylène qui est ensuite converti en éthylène glycol par réaction entre l'oxyde d'éthylène et l'eau. Cette réaction est catalysée par des acides ou des bases. Si la réaction est effectuée dans un milieu ayant un pH neutre, alors le mélange réactionnel doit être pourvu d'énergie thermique. La voie biologique de production d'éthylène glycol est via la dégradation du polyéthylène par les bactéries intestinales de la chenille de la plus grande cire.
Qu'est-ce que le diéthylène glycol?
Le diéthylène glycol est un composé organique ayant la formule chimique C4HdixO3. À température ambiante, c'est un liquide incolore et inodore. Cependant, c'est hygroscopique et toxique. Il a un goût sucré. Le diéthylène glycol est miscible avec l'eau et les alcools car il est capable de former des liaisons hydrogène. La masse molaire de ce composé est 106.12 g / mol. Le point de fusion du diéthylène glycol est -10.45 ° C et le point d'ébullition est de 245 ° C.
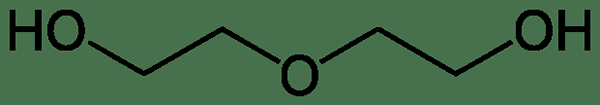
Figure 02: Structure chimique du diéthylène glycol
La voie la plus courante de la production de diéthylène glycol est par hydrolyse partielle de l'oxyde d'éthylène. L'éthylène est converti en oxyde d'éthylène; Ainsi, l'oxyde d'éthylène est un intermédiaire. La réaction de hydrolyse partielle donne du diéthylène glycol par la combinaison de deux molécules de glycol éthylène via une liaison éther.
Quelles sont les similitudes entre l'éthylène glycol et le diéthylène glycol?
- L'éthylène glycol et le diéthylène glycol sont des composés alcoolisés.
- Les deux sont capables de former des liaisons hydrogène.
- Les deux sont des liquides incolores à température ambiante.
Quelle est la différence entre l'éthylène glycol et le diéthylène glycol?
Éthylène glycol vs diéthylène glycol | |
| L'éthylène glycol est un alcool ayant la formule chimique C2H6O2. | Le diéthylène glycol est un composé organique ayant la formule chimique C4HdixO3. |
| Masse molaire | |
| La masse molaire d'éthylène glycol est de 62 g / mol. | La masse molaire de diéthylène glycol est 106.12 g / mol. |
| Structure moleculaire | |
| L'éthylène glycol est une molécule individuelle dérivée de l'oxyde d'éthylène. | Le diéthylène glycol est une combinaison de deux molécules d'éthylène glycol via une liaison éther. |
| Liaison éther | |
| Il n'y a pas de liaison éther dans l'éthylène glycol. | Bond éther relie les deux molécules d'éthylène glycol. |
| Point de fusion et point d'ébullition | |
| Le point de fusion de l'éthylène glycol est -12.9 ° C et le point d'ébullition était 197.3 ° C. | Le point de fusion du diéthylène glycol est -10.45 ° C et le point d'ébullition est de 245 ° C. |
| Production | |
| Premièrement, l'éthylène est converti en oxyde d'éthylène, qui à son tour est converti en éthylène glycol en réagissant avec l'eau. | Le diéthylène glycol est produit par hydrolyse partielle de l'oxyde d'éthylène. |
Résumé - Éthylène glycol vs Diéthylène Glycol
L'éthylène glycol et le diéthylène glycol sont produits à partir du même matériau de départ; éthylène. La différence entre l'éthylène glycol et le diéthylène glycol est qu'une molécule d'éthylène glycol est une molécule individuelle alors que la molécule de diéthylène glycol est formée par la combinaison de deux molécules de glycol éthylène via une liaison éther.
Référence:
1. "Diethylene glycol.»Wikipedia, Wikimedia Foundation, 3 avril. 2018. Disponible ici
2. «L'éthylène glycol.»Wikipedia, Wikimedia Foundation, 3 avril. 2018. Disponible ici
Image gracieuseté:
1.«Structure chimique de l'éthylène glycol» (CC BY-SA 3.0) via Commons Wikimedia
2.«Structure de diéthylène glycol» par yikrazuul - propre travail, (domaine public) via les communes Wikimedia


