Différence entre l'ester et l'éther

La principale différence entre l'ester et l'éther est que le Le groupe fonctionnel d'un ester est -coo, tandis que le groupe fonctionnel d'un éther est -O-.
L'ester et l'éther sont des molécules organiques avec des atomes d'oxygène. Les esters ont le groupe -coo. Ici, un atome d'oxygène est lié au carbone avec une double liaison, et l'autre oxygène est lié à une seule liaison. Étant donné que seulement trois atomes se connectent avec l'atome de carbone, il a une géométrie planaire trigonale autour. De plus, l'atome de carbone est SP2 hybridé. De plus, un ester est un dérivé acide carboxylique. Un éther, en revanche, a un atome d'oxygène avec deux liaisons uniques avec deux groupes alkyle ou aryle. L'atome d'oxygène a également deux paires d'électrons solitaires.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'ester
3. Qu'est-ce que l'éther
4. Comparaison côte à côte - ester vs éther sous forme tabulaire
5. Résumé
Qu'est-ce que l'ester?
Un ester est un composé organique qui se forme par la réaction d'un oxoacide avec un composé hydroxyle (comme l'alcool et le phénol). Il ressemble à un acide carboxylique ayant son atome d'hydrogène du groupe -COOH remplacé par un groupe alkyle ou aryle. Les esters sont des molécules polaires, mais leurs points d'ébullition sont inférieurs à ceux des acides carboxyliques de poids similaire. C'est parce que les esters ne peuvent pas former des liaisons hydrogène entre eux. Cependant, ils peuvent former des liaisons hydrogène entre leurs atomes d'oxygène et les atomes d'hydrogène des molécules d'eau. Par conséquent, les esters sont légèrement solubles dans l'eau.

Figure 01: Structure générale d'un ester
De plus, un ester a une odeur fruitée, qui est différente de l'acide carboxylique correspondant (les acides ont généralement une odeur désagréable). En fait, ces esters sont la raison de l'odeur de nombreux fruits; Par exemple, l'ananas obtient son odeur de l'éthanoate d'éthyle. Et, ce phénomène a conduit à l'utilisation d'esters dans l'industrie alimentaire.
Cependant, les esters que nous utilisons dans un produit particulier pour obtenir une odeur fruitée souhaitée n'est pas le même composé qui est présent dans la source naturelle. Néanmoins, les esters peuvent produire le même goût et l'odeur. De plus, bien que le composé ne soit pas le même que dans le fruit naturel, il n'est pas dangereux de manger ces produits alimentaires car la structure de l'ester est étroitement similaire à celle du composé naturel.
Qu'est-ce que l'éther
Un éther est un composé organique qui a un atome d'oxygène lié à deux groupes alkyle ou aryle. Nous pouvons nommer un éther simple comme éthers alkyles car ils contiennent deux petits groupes alkyle attachés à un atome d'oxygène. Dans sa nomenclature, nous devons énumérer les groupes alkyle par ordre alphabétique et ajouter le terme «éther» à la fin. Par exemple, si un éther a un groupe méthyle et un groupe N-butyle lié à l'atome d'oxygène, nous l'appelons «éther N-butylméthyl».
Les éthers peuvent dissoudre un large éventail de composés polaires et non polaires. C'est principalement parce que les éthers n'ont pas de réseau de liaison hydrogène qui doit être brisé afin de dissoudre un soluté. Par conséquent, les composés non polaires ont tendance à se dissoudre dans l'éther diéthylique mieux que les alcools.
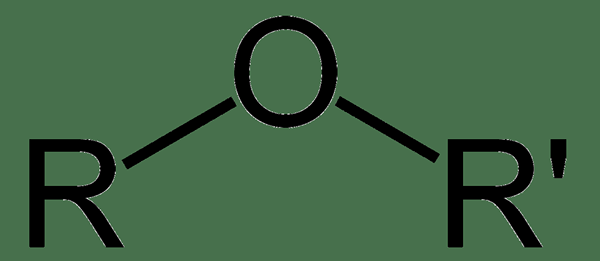
Figure 02: Structure générale de l'éther
Dans la structure générale de l'éther, l'oxygène a un SP3 L'hybridation et les deux paires solitaires sont en deux orbitales hybrides tandis que deux participent à des liens avec les groupes R. L'angle de liaison R-O-R est d'environ 104.5 °, qui est similaire à l'eau. Les points d'ébullition des éthers sont à peu près comparables à ceux des hydrocarbures ayant le même poids moléculaire, mais les points d'ébullition des éthers sont inférieurs à la valeur des alcools. Bien que les éthers ne puissent pas faire des liaisons hydrogène en eux, ils sont capables de former des liaisons hydrogène avec d'autres composés tels que l'eau. Par conséquent, les éthers sont solubles dans l'eau, mais la solubilité peut diminuer en fonction de la longueur des chaînes d'hydrocarbures attachées.
Quelle est la différence entre l'ester et l'éther?
Un ester est un composé organique formé par la réaction d'un oxoacide avec un composé hydroxyle. Un éther, en revanche, est un composé organique qui a un atome d'oxygène lié à deux groupes alkyle ou aryle. La principale différence entre l'ester et l'éther est que le groupe fonctionnel d'Ester est -coo, tandis que le groupe fonctionnel d'éther est -O-. La formule chimique générale de l'ester et de l'éther est RC (= o) ou «et r-o-r», respectivement. De plus, une autre différence significative entre l'ester et l'éther est que l'ester a un groupe carbonyle dans son groupe fonctionnel où l'éther ne.
Plus important encore, les esters ont une odeur fruitée, tandis que l'éther a une forte odeur éthérée. Par conséquent, nous pouvons considérer cela également comme une différence entre l'ester et l'éther. De plus, les esters ont des points d'ébullition plus bas que les acides carboxyliques et les alcools du même poids tandis que l'éther a des points d'ébullition inférieurs à ceux des esters, des acides carboxyliques et des alcools du même poids.
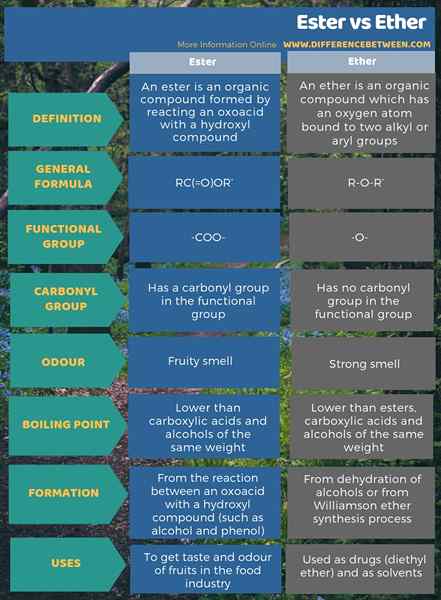
Résumé - Ester vs Ether
Un ester est un composé organique qui se forme en réagissant un oxoacide avec un composé hydroxyle. Un éther, en revanche, est un composé organique qui a un atome d'oxygène lié à deux groupes alkyle ou aryle. La principale différence entre l'ester et l'éther est que le groupe fonctionnel d'Ester est -coo, tandis que le groupe fonctionnel d'éther est -O-.
Référence:
1. Derosa, Thomas F. Progrès en chimie organique synthétique et méthodes rapportées aux brevets américains. Elsevier, 2006.
2. Ouellette, Robert J., et J. David Rawn. Chimie organique: structure, mécanisme et synthèse. Elsevier, 2014.
Image gracieuseté:
1. «Ester-General» par Sakurambo ~ Commonswiki a supposé. Propre travail assumé (sur la base des réclamations du droit d'auteur)., Domaine public) via les communes Wikimedia
2. «Ether- (général)» par Benjah-Bmm27 supposé. Propre travail assumé (basé sur les réclamations du droit d'auteur) (domaine public) via Commons Wikimedia


