Différence entre l'effet électrophorétique et asymétrique
Le différence clé entre l'effet électrophorétique et asymétrique est que L'effet électrophorétique est l'effet des forces d'attraction entre les espèces ioniques et les molécules de solvant sur le mouvement des ions tandis que l'effet asymétrique est l'effet de la concentration en ionique élevée dans la solution sur le mouvement des ions.
L'effet électrophorétique et l'effet asymétrique des termes sont généralement discutés dans le sujet de la «conductivité électrolytique». La conductivité électrolytique décrit le mouvement des espèces ioniques (cations et anions) dans une solution. Il existe deux principaux types d'effets qui peuvent apporter des modifications sur la conductivité ionique: l'effet électrophorétique et l'effet asymétrique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'effet électrophorétique
3. Quel est l'effet asymétrique
4. Comparaison côte à côte - effet électrophorétique vs asymétrique sous forme tabulaire
5. Résumé
Qu'est-ce que l'effet électrophorétique?
L'effet électrophorétique est l'effet des molécules de solvant sur le mouvement d'un ion particulier dans une solution. C'est un facteur important qui peut ralentir le mouvement des ions dans une solution. En raison des forces d'attraction entre les molécules de solvant et les espèces ioniques dans la solution, lorsqu'un potentiel électrique est appliqué sur la solution, il a tendance à déplacer l'atmosphère ionique autour d'un ion en mouvement particulier lui-même. Cet ion en mouvement est au centre de l'atmosphère ionique. En raison de cet effet électrophorétique, l'ion central est influencé pour se déplacer vers le poteau en face de son atmosphère ionique, ce qui provoque le lent mouvement de l'ion.

Figure 01: Une solution avec un potentiel électrique externe qui lui est appliqué
Quel est l'effet asymétrique?
L'effet asymétrique est l'effet d'autres ions sur le mouvement d'un ion particulier dans une solution. En d'autres termes, cela signifie qu'une solution contenant une concentration ionique élevée montre des changements dans le mouvement ionique que d'habitude. Lorsque nous appliquons un potentiel électrique sur une solution électrolytique, les ions positifs ou les cations de la solution se déplacent vers l'électrode négative et les ions négatifs ou les anions se déplacent vers l'électrode positive. Si la concentration de la solution est élevée, les ions négatifs se rapprochent des ions positifs. Ensuite, il y a une résistance sur les espèces ioniques, affectant la vitesse de l'ion mobile. Nous appelons cet effet l'effet asymétrique. Le nom «asymétrique» est donné car la sphère ionique autour de l'ion mobile n'est pas symétrique en raison de la concentration ionique élevée.
Dans une solution ionique hautement concentrée, les forces d'attraction entre les ions positives et négatives sont excellentes. Lorsqu'un potentiel électrique est appliqué à un ion particulier, la densité de charge des charges opposées à l'arrière est plus élevée que celles de l'avant. Par conséquent, il ralentit le mouvement de l'ion. Cela se produit en raison de la densité de charge asymétrique dans la solution électrolytique.
Quelle est la différence entre l'effet électrophorétique et asymétrique?
La conductivité électrolytique définit le mouvement des espèces ioniques (cations et anions) dans une solution. Il existe deux principaux types d'effets qui peuvent apporter des modifications à la conductivité ionique: l'effet électrophorétique et l'effet asymétrique. La principale différence entre l'effet électrophorétique et asymétrique est que l'effet électrophorétique est l'effet des forces d'attraction entre les espèces ioniques et les molécules de solvant sur le mouvement des ions tandis que l'effet asymétrique est l'effet de la concentration en ionique élevée dans la solution sur le mouvement des ions.
Vous trouverez ci-dessous une tabulation sommaire de la différence entre l'effet électrophorétique et asymétrique.
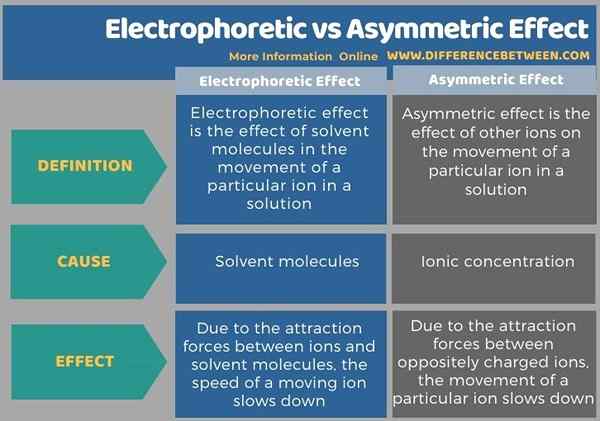
Résumé - Electrophorétique vs effet asymétrique
L'effet électrophorétique et l'effet asymétrique des termes sont discutés dans le sujet de la «conductivité électrolytique». La principale différence entre l'effet électrophorétique et asymétrique est que l'effet électrophorétique est l'effet des forces d'attraction entre les espèces ioniques et les molécules de solvant sur le mouvement des ions tandis que l'effet asymétrique est l'effet de la concentration ionique élevée dans la solution sur le mouvement des ions.
Référence:
1. «Atmosphère ionique." Wikipédia, Fondation Wikimedia, 21 octobre. 2019, disponible ici.
Image gracieuseté:
1. «GelelektrophoResEApparaturat» (CC BY-SA 3.0) via Commons Wikimedia


