Différence entre le cyclohexane et le cyclohexène

Le différence clé entre le cyclohexane et le cyclohexène est que le Le cyclohexane est un hydrocarbure saturé tandis que le cyclohexène est un hydrocarbure insaturé.
Il existe différents types de composés organiques fabriqués en rejoignant différents éléments avec des atomes de carbone. Le cyclohexane et le cyclohexène sont des hydrocarbures qui se composent uniquement d'atomes de carbone et d'hydrogène. Les hydrocarbures sont sous deux formes sous forme d'hydrocarbures aromatiques et aliphatiques. De plus, nous pouvons les classer comme des hydrocarbures saturés (alcanes) et insaturés (alcènes et alcynes). Toutes les liaisons entre les atomes de carbone et les hydrogènes sont des liaisons uniques dans des hydrocarbures saturés tandis qu'il y a des liaisons doubles ou triples entre les atomes de carbone sous des formes insaturées.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le cyclohexane
3. Qu'est-ce que le cyclohexène
4. Comparaison côte à côte - cyclohexane vs cyclohexène sous forme tabulaire
5. Résumé
Qu'est-ce que le cyclohexane?
Le cyclohexane est une molécule cyclique avec la formule de C6H12. C'est un cycloalkane. Bien qu'il ait le nombre similaire de carbones comme le benzène, le cyclohexane est un hydrocarbure saturé. Il n'y a donc pas de double liais. C'est un liquide incolore avec une odeur douce et douce. Nous pouvons produire ce composé par la réaction entre le benzène et l'hydrogène. Puisqu'il s'agit d'un cycloalkane, il est moins réactif comparativement.

Figure 01: CONFORMATION DE CHAISE DE CYCLOHEXANE
Le cyclohexane n'est pas polaire et hydrophobe. Par conséquent, cela est utile comme solvant non polaire dans le laboratoire de chimie. Nous considérons ce composé comme le cycloalkane le plus stable de tous parce que sa déformation annuelle totale est minimale. Par conséquent, il produit le moins de chaleur lors de la combustion par rapport aux autres cycloalcanes.
Cependant, c'est très inflammable. Le cyclohexane n'a pas de forme hexagone parfaite. Par conséquent, s'il est en forme hexagonale, il aurait une souche de torsion considérable. Pour minimiser autant que possible cette souche de torsion, le cyclohexane adopte une conformation de chaise tridimensionnelle. À cette conformation, les atomes de carbone sont à un angle de 109.5o. Six atomes d'hydrogène sont dans le plan équatorial, et les autres sont dans le plan axial. Cette conformation est la conformation la plus stable du cyclohexane.
Qu'est-ce que le cyclohexène?
Le cyclohexène est un cycloalcène avec la formule de C6Hdix. Il est presque similaire au cyclohexane, mais il y a une double liaison entre deux atomes de carbone dans l'anneau, ce qui en fait un hydrocarbone insaturé. Le cyclohexène est un liquide incolore, et il a une odeur nette.
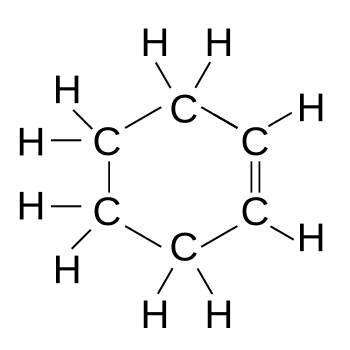
Figure 02: La double liaison entre deux atomes de carbone dans la structure de l'anneau du cyclohexène
De plus, ce n'est pas très stable. Lorsqu'il est exposé à la lumière et à l'air pendant une période plus longue, il forme des peroxydes. Nous pouvons produire ce composé par hydrogénation du benzène jusqu'à ce qu'une double liaison reste. En dehors de cela, c'est un liquide très inflammable. Étant donné que le cyclohexène a une double liaison, il peut subir des réactions caractéristiques des alcènes. Par exemple, avec du brome, il subira un ajout électrophile.
Quelle est la différence entre le cyclohexane et le cyclohexène?
Les cycloalcanes sont des composés organiques n'ayant que des liaisons covalentes uniques entre les atomes de carbone dans une structure d'anneau; Le cyclohexane est un bon exemple. Les cycloalcènes, en revanche, sont des composés organiques ayant des liaisons simples avec une ou plusieurs doubles liaisons entre les atomes de carbone dans la structure de l'anneau; Le cyclohexène est un bon exemple. Par conséquent, la principale différence entre le cyclohexane et le cyclohexène est que le cyclohexane est un hydrocarbure saturé alors que le cyclohexène est un hydrocarbure insaturé. Une autre différence entre le cyclohexane et le cyclohexène est que le cyclohexane est relativement stable.
L'infographie ci-dessous tabule la différence entre le cyclohexane et le cyclohexène comme comparaison côte à côte.
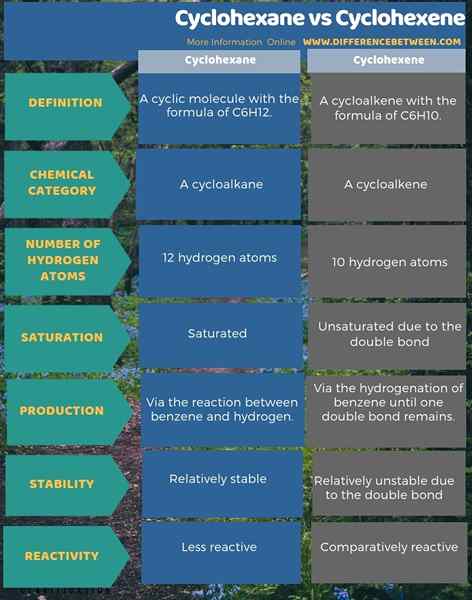
Résumé - Cyclohexane vs Cyclohexène
Le cyclohexane est un composé alcane cyclique tandis que le cyclohexène est un composé d'alcène cyclique. La principale différence entre le cyclohexane et le cyclohexène est que le cyclohexane est un hydrocarbure saturé tandis que le cyclohexène est un hydrocarbure insaturé.
Référence:
1. «Cyclohexane.»Wikipedia, Wikimedia Foundation, 17 septembre. 2018. Disponible ici
2. «Cyclohexène.»Wikipedia, Wikimedia Foundation, 4 déc. 2017. Disponible ici
Image gracieuseté:
1.«Cyclohexane-chair-2d-stéreo-squelettique» (domaine public) via Commons Wikimedia
2.«Cyclohexène pour Highscool» par すじにく シチュー シチュー シチュー シチュー シチュー シチュー シチュー シチュー シチュー シチュー シチュー - CC0) via Commons Wikimedia


