Différence entre le sel complexe et le double sel

Le différence clé entre le sel complexe et le double sel est que Le sel complexe est un composant chimique ayant un ou plusieurs ions complexes, tandis que le double sel est un composant chimique de deux composés de sel.
Un sel est un composé chimique ionique contenant un cation et un anion. Le nombre de cations dépend du nombre d'anions et vice versa. Par conséquent, le composé de sel est neutre.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce qu'un sel complexe
3. Qu'est-ce qu'un double sel
4. Comparaison côte à côte - sel complexe vs double sel sous forme tabulaire
5. Résumé
Qu'est-ce qu'un sel complexe?
Un sel complexe est un composé chimique ayant un atome métallique central avec des liaisons de coordination de ligands autour d'elle. Le composé complexe de coordination est un autre nom pour le sel complexe. Nous appelons cela un sel complexe dérive en raison de sa structure complexe, et la présence de cations et d'anions liés les uns aux autres.
Ce type de sel ne se dissocient pas complètement en ses ions lorsqu'il est ajouté à l'eau; Au lieu de cela, ils restent des structures complexes. Par conséquent, cette formation complexe est utile dans la chélation des ions métalliques. Pendant cette chélation, les ions métalliques se lient aux espèces chimiques nommées comme ligands à travers des liaisons de coordination, ce qui rend l'ion métallique indisponible pour toute autre réaction chimique qui a lieu dans un mélange réactionnel. Ceci est important dans les réactions chimiques où les interférences provenant de certains ions métalliques doivent être éliminées.
Cependant, un sel complexe ne peut pas être analysé en le dissolvant dans l'eau car le sel complexe ne donne pas d'ions simples. Un sel complexe est préparé en mélangeant deux sels différents dans un rapport stœchiométrique. Ensuite, la quantité correcte de ligands se liera avec l'ion métallique.
Qu'est-ce qu'un double sel?
Un double sel est un composé chimique que nous pouvons préparer à travers la combinaison de deux composés de sel différents. Par conséquent, un double sel contient plus d'un anion et cation. Nous pouvons préparer un double sel en dissolvant les composés de sel dans le même liquide, suivis d'une cristallisation à un schéma régulier.

Figure 01: Le sulfate d'ammonium en fer (II) est un double sel
Lorsqu'il est dissous dans l'eau, un double sel est complètement dissocié dans tous les ions. Une solution aqueuse d'un double sel est composée de cations et d'anions, qui étaient dans les deux composés de sel initiaux. Par conséquent, cette dissociation produit des ions simples dans la solution aqueuse.
Un double sel peut facilement être analysé en le dissolvant dans l'eau en raison de sa dissociation complète dans l'eau. Cependant, lors de la préparation d'un double sel, les composants (deux sels) doivent être mélangés dans un rapport équimolaire. En d'autres termes, la même quantité de moles doit être mélangée. Sinon, un réseau uniforme et régulier ne peut être obtenu.
Quelques exemples de doubles sels sont les alums, le sel de Tutton, le tartrate de sodium de potassium, la bromlite, etc. Les propriétés des cristaux à double sel sont différentes des propriétés des sels initiaux utilisés dans la préparation du double sel.
Quelle est la différence entre le sel complexe et le double sel?
Un sel complexe est un composé chimique ayant un atome métallique central avec des liaisons de coordination de ligands autour de lui tandis qu'un double sel est un composé chimique que nous pouvons préparer à travers la combinaison de deux composés de sel différents. La principale différence entre le sel complexe et le double sel est que le sel complexe est un composant chimique ayant un ou plusieurs ions complexes, tandis qu'un double sel est un composant chimique de deux composés de sel.
L'infographie ci-dessous montre plus de différences entre le sel complexe et le double sel sous forme tabulaire pour la comparaison côte à côte.
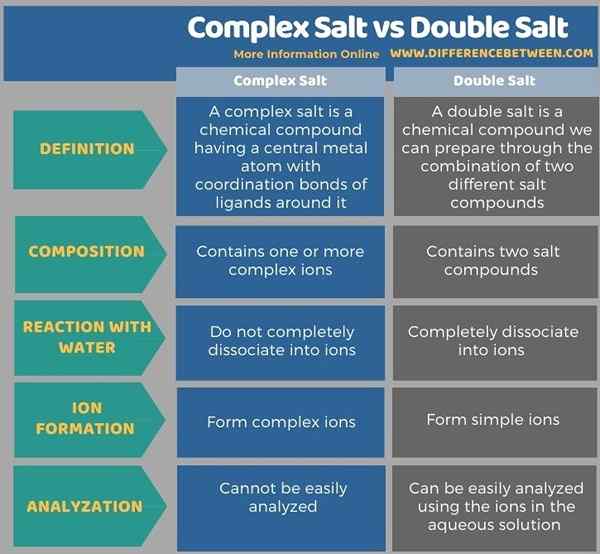
Résumé - Salt complexe vs double sel
La principale différence entre le sel complexe et le double sel est que le sel complexe est un composant chimique ayant un ou plusieurs ions complexes, tandis qu'un double sel est un composant chimique de deux composés de sel.
Référence:
1. Helmenstine, Anne Marie. «Définition du sel en chimie."Thoughtco, août. 28, 2020, disponible ici.
Image gracieuseté:
1. «Mohrs Zout» par Capaccio - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


