Différence entre le chlorobenzène et le chlorure de cyclohexyle
Le différence clé entre le chlorobenzène et le chlorure de cyclohexyle est que Le chlorobenzène a un nuage d'électrons délocalisé, alors qu'il n'y a pas de nuage d'électrons délocalisé dans le chlorure de cyclohexyle.
Le chlorobenzène a un anneau de benzène avec un atome de chlore attaché à l'anneau. Ici, l'atome de chlore a remplacé l'un des atomes d'hydrogène de l'anneau. Par conséquent, le nuage d'électrons délocalisé de l'anneau de benzène est également là. Cependant, le chlorure de cyclohexyle a un atome de chlore attaché à une molécule de cyclohexane. Ici aussi, l'atome de chlore remplace un atome d'hydrogène de l'anneau. Puisqu'il n'y a pas de nuage d'électrons délocalisé dans le cyclohexane, le chlorure de cyclohexyle n'a pas non plus de nuage d'électrons délocalisé.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le chlorobenzène
3. Qu'est-ce que le chlorure de cyclohexyle
4. Comparaison côte à côte - chlorobenzène vs chlorure de cyclohexyle sous forme tabulaire
5. Résumé
Qu'est-ce que le chlorobenzène?
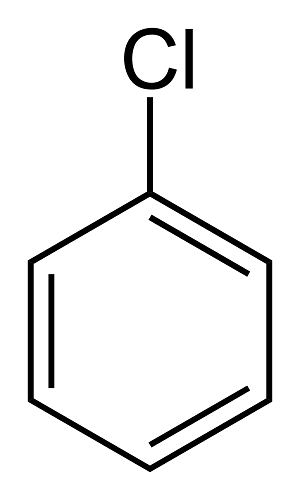
Le chlorobenzène est un composé organique aromatique qui a un anneau de benzène avec un atome de chlore attaché. La formule chimique de ce composé est C6H5CL. C'est un liquide incolore et inflammable. Mais il a une odeur d'amande. Sa masse molaire est 112.56 g / mol. De plus, le point de fusion de ce composé est de -45 ° C tandis que le point d'ébullition est de 131 ° C.
Lorsque vous envisagez les utilisations de ce composé, il est très important en tant qu'intermédiaire dans la production de composés tels que les herbicides, le caoutchouc, etc. De plus, c'est un solvant d'ébullition élevé que nous utilisons dans des applications industrielles.
Nous pouvons produire du chlorobenzène par chloration du benzène en présence d'acides Lewis tels que le chlorure ferrique et le dichlorure de soufre. Ici, Lewis Acid agit comme le catalyseur de la réaction. Il peut améliorer l'électrophilicité du chlore. De plus, puisque le chlore est électronégatif, le chlorobenzène a tendance à ne pas subir de chloration supplémentaire. Plus important encore, ce composé montre une toxicité «faible à modérée». Cependant, si ce composé entre dans notre corps en respirant, nos poumons et notre système urinaire peuvent l'excréter.
Qu'est-ce que le chlorure de cyclohexyle?
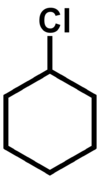
Le chlorure de cyclohexyle est un composé organique qui a une molécule de cyclohexane avec l'un de ses atomes d'hydrogène remplacé par un atome de chlore. La formule chimique de celui-ci est C6H11CL. Un autre nom commun pour ce composé est le chlorocyclohexane.

De plus, le chlorure de cyclohexyle est un liquide incolore et a une odeur suffocante. De plus, nous pouvons le préparer en traitant le cyclohexanol avec HCL. Son point de fusion est de -44 ° C tandis que le point d'ébullition est de 142 ° C.
Quelle est la différence entre le chlorobenzène et le chlorure de cyclohexyle?
Le chlorobenzène est un composé organique aromatique et a un anneau de benzène avec un atome de chlore attaché. Le chlorure de cyclohexyle est un composé organique et a une molécule de cyclohexane avec l'un de ses atomes d'hydrogène remplacé par un atome de chlore. La principale différence entre le chlorobenzène et le chlorure de cyclohexyle est que le chlorobenzène a un nuage d'électrons délocalisé, tandis que le chlorure de cyclohexyle n'a pas de nuage d'électrons délocalisé.
De plus, une autre différence entre le chlorobenzène et le chlorure de cyclohexyle est que le chlorobenzène est aromatique et présente une insaturation, tandis que le chlorure de cyclohexyle n'est pas aromatique et qu'il n'a aucune insaturation (toutes les liaisons chimiques sont saturées). Lorsque vous envisagez les points de fusion et d'ébullition, pour le point de fusion du chlorobenzène est de -45 ° C et le point d'ébullition est de 131 ° C, tandis que pour le point de fusion du chlorure de cyclohexyle est de -44 ° C et le point d'ébullition est de 142 ° C.
L'infographie ci-dessous montre plus de comparaisons liées à la différence entre le chlorobenzène et le chlorure de cyclohexyle.
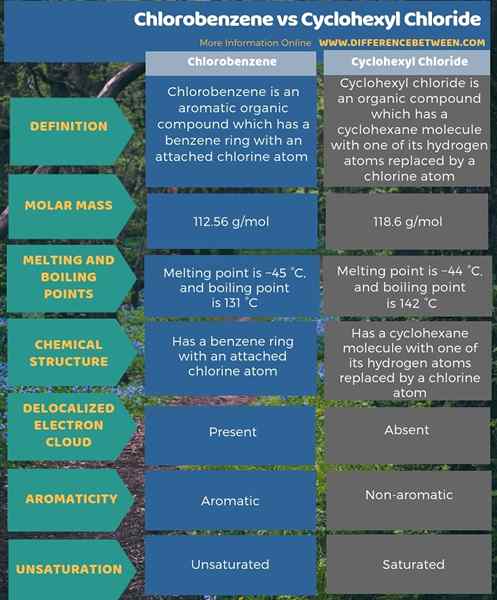
Résumé - chlorobenzène vs chlorure de cyclohexyle
Le chlorobenzène est un composé organique aromatique et a un anneau de benzène avec un atome de chlore attaché. Le chlorure de cyclohexyle est un composé organique et a une molécule de cyclohexane avec l'un de ses atomes d'hydrogène remplacé par un atome de chlore. En résumé, la principale différence entre le chlorobenzène et le chlorure de cyclohexyle est que le chlorobenzène a un nuage d'électrons délocalisé, alors qu'il n'y a pas de nuage d'électrons délocalisé.
Référence:
1.«Chlorocyclohexane.»Information du Centre national pour la biotechnologie. Base de données de composés PubChem, u.S. Bibliothèque nationale de médecine, disponible ici.
Image gracieuseté:
1. «Chlorobenzene2» par l'utilisateur: Bryan Derksen - propre travail (domaine public) via Commons Wikimedia
2. «Chlorocyclohexane» par Struthief.Wikipedia à Commons (CC0) via Commons Wikimedia


